よむ、つかう、まなぶ。
別紙1○先進医療Bに係る新規技術の科学的評価等について (28 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00069.html |
| 出典情報 | 先進医療会議(第131回 4/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
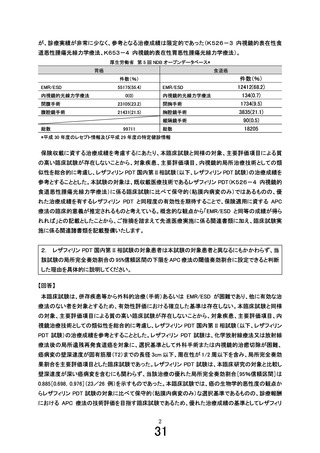
本試験が EMR/ESD の実施が困難である患者を対象としていることを踏まえると、
効能効果として「食道表在癌、早期胃癌」という表現が認められる可能性は低いと
考えるが、期待される適応症として、これらのがん種を設定しておくことは差し支
えないと考え「適」と判断した。
【有効性及び安全性の評価方法:主要評価項目、仮説の妥当性について】
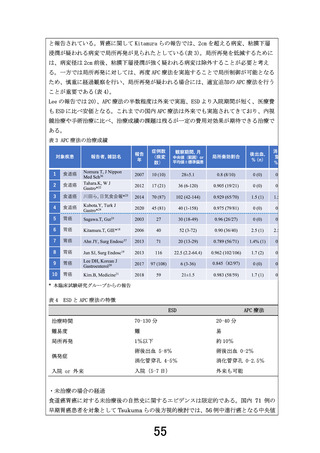
事前照会事項に対する回答においては、本試験における APC 療法対象者に対す
る比較対照となる標準治療は存在しないことから、対象疾患、主要評価項目、内視
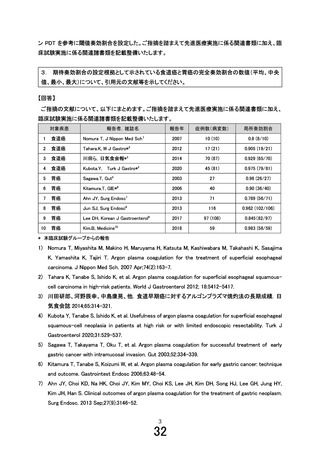
鏡治療技術として類似性を総合的に考慮して、レザフィリン PDT 試験の成績(術
後 6 か月の局所完全奏効割合:0.885 [95%CI: 0.689, 0.976])を参考に、本試験
の主要評価項目である 12 週の局所完全奏効割合の閾値奏効率を 0.7 に設定した旨
が説明されている。
しかしながら、レザフィリン PDT 試験と本試験では主要評価項目の評価時点が
異なるにも関わらず当該試験の成績を参照できると考えた根拠、また 95%CI の下
限値を本試験の閾値に設定できると考えた根拠については、明確な回答が得られ
ていない。したがって、本試験で対象とする患者集団おいて、12 週の局所完全奏
効割合の 95%CI の下限が 0.7 を超えることが、APC 療法の保険収載に資するエビデ
ンスと見なされるのか判断が困難である。
他方で、照会回答にあるように、本試験の対象集団に対する標準治療は存在せ
ず、また本試験と同様の対象集団・主要評価項目を用いた質の高い臨床試験が実施
されていないのであれば、本試験成績が APC 療法のエビデンスを評価する重要な
データになると考える。当該回答の主張の臨床的妥当性については臨床の評価委
員に委ねることとし、ここでは当該回答の主張に臨床的妥当性があるという前提
で、試験デザイン・統計解析計画そのものには特段の問題は認められないことか
ら、統計学的観点から「適」と判断した。
その他の項目については、特段の問題は認められないことから、
「適」と判断した。
被験者の適格基準及び選定方法、治療計画の内容については、専門外の項目であり
判断が困難であることから、主担当に委ねることとした。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数 54 例
適
条件付き適
継続審議
予定試験期間
実施条件:下記コメントを参照のこと。
28
4
4年6か月
不適
効能効果として「食道表在癌、早期胃癌」という表現が認められる可能性は低いと
考えるが、期待される適応症として、これらのがん種を設定しておくことは差し支
えないと考え「適」と判断した。
【有効性及び安全性の評価方法:主要評価項目、仮説の妥当性について】
事前照会事項に対する回答においては、本試験における APC 療法対象者に対す
る比較対照となる標準治療は存在しないことから、対象疾患、主要評価項目、内視
鏡治療技術として類似性を総合的に考慮して、レザフィリン PDT 試験の成績(術
後 6 か月の局所完全奏効割合:0.885 [95%CI: 0.689, 0.976])を参考に、本試験
の主要評価項目である 12 週の局所完全奏効割合の閾値奏効率を 0.7 に設定した旨
が説明されている。
しかしながら、レザフィリン PDT 試験と本試験では主要評価項目の評価時点が
異なるにも関わらず当該試験の成績を参照できると考えた根拠、また 95%CI の下
限値を本試験の閾値に設定できると考えた根拠については、明確な回答が得られ
ていない。したがって、本試験で対象とする患者集団おいて、12 週の局所完全奏
効割合の 95%CI の下限が 0.7 を超えることが、APC 療法の保険収載に資するエビデ
ンスと見なされるのか判断が困難である。
他方で、照会回答にあるように、本試験の対象集団に対する標準治療は存在せ
ず、また本試験と同様の対象集団・主要評価項目を用いた質の高い臨床試験が実施
されていないのであれば、本試験成績が APC 療法のエビデンスを評価する重要な
データになると考える。当該回答の主張の臨床的妥当性については臨床の評価委
員に委ねることとし、ここでは当該回答の主張に臨床的妥当性があるという前提
で、試験デザイン・統計解析計画そのものには特段の問題は認められないことか
ら、統計学的観点から「適」と判断した。
その他の項目については、特段の問題は認められないことから、
「適」と判断した。
被験者の適格基準及び選定方法、治療計画の内容については、専門外の項目であり
判断が困難であることから、主担当に委ねることとした。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数 54 例
適
条件付き適
継続審議
予定試験期間
実施条件:下記コメントを参照のこと。
28
4
4年6か月
不適