よむ、つかう、まなぶ。
別紙1○先進医療Bに係る新規技術の科学的評価等について (72 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00069.html |
| 出典情報 | 先進医療会議(第131回 4/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3.説明文書 11 項(2)予想される不利益の箇所に、再発した場合に改めて APC 療法
で治療ができる旨加筆されているが、再発を早期に発見するための手立てについて説明
がないため被験者の不安への応えになっていないと考えます。再発した場合に治療がで
きることに加え、再発の早期発見のためにどのような手立てが用意されているのか、被
験者は自身で何ができるのか等を具体的に加筆する必要があると考えます。
【回答】
ご指摘いただきありがとうございます。
APC 療法後の遺残再発病変に対して可能な限り治療機会を確保するため、術後 12
週、24 週、48 週、72 週に上部消化管内視鏡検査を実施する旨について、不利益の
箇所に追記致しました。本臨床試験で対象とする非常に初期段階の癌や遺残再発
病変の初期は自覚症状に乏しく、研究対象者自身ができることはないと考えます。
研究計画書、説明同意書において、有害事象に関連する術後症状については「病状
チェックシート(研究計画書 別添 1)」を用いて記録いただくよう定めています。
4.説明文書をより理解しやすくするために以下の点について対応してください。
①説明文書7頁(ウ)の3行目から「F1 以下の食道静脈瘤を合併している方…」は
「食道静脈瘤が F1 以下である方、もしくは F2 または F3 の食道静脈瘤に対して内視鏡
治療を施行して F1 以下になった方」とされた方が日本語として読みやすいと考えます。
②説明文書8頁(エ)
「血液疾患の方のうち、血小板が3万/μL 以上の方」は、研究
計画書の記載と同様に「血液疾患の方のうち、血小板が減少しているが、血小板が3万
/μL 以上の方」と記載いただいた方が理解しやすいと考えます。
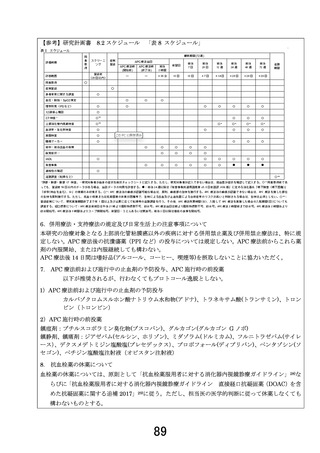
③説明文書9頁(2)研究のスケジュールの箇所の2段落目、「術後1年6ヶ月(72
週)まで経過観察が行われます。」のあとに「経過観察期間中は、12 週、24 週、48 週、
72 週に来院いただき、上部消化管内視鏡検査を受けていただきます。」と加筆いただく
と被験者の方に自分が APC 治療以外に何をされるのかが理解しやすくなると考えます。
④同意書・同意撤回書の署名欄の下線が消えているので修正ください。
【回答】
ご指摘いただきありがとうございます。
該当箇所について、記載を修正致しました。
以上
72
で治療ができる旨加筆されているが、再発を早期に発見するための手立てについて説明
がないため被験者の不安への応えになっていないと考えます。再発した場合に治療がで
きることに加え、再発の早期発見のためにどのような手立てが用意されているのか、被
験者は自身で何ができるのか等を具体的に加筆する必要があると考えます。
【回答】
ご指摘いただきありがとうございます。
APC 療法後の遺残再発病変に対して可能な限り治療機会を確保するため、術後 12
週、24 週、48 週、72 週に上部消化管内視鏡検査を実施する旨について、不利益の
箇所に追記致しました。本臨床試験で対象とする非常に初期段階の癌や遺残再発
病変の初期は自覚症状に乏しく、研究対象者自身ができることはないと考えます。
研究計画書、説明同意書において、有害事象に関連する術後症状については「病状
チェックシート(研究計画書 別添 1)」を用いて記録いただくよう定めています。
4.説明文書をより理解しやすくするために以下の点について対応してください。
①説明文書7頁(ウ)の3行目から「F1 以下の食道静脈瘤を合併している方…」は
「食道静脈瘤が F1 以下である方、もしくは F2 または F3 の食道静脈瘤に対して内視鏡
治療を施行して F1 以下になった方」とされた方が日本語として読みやすいと考えます。
②説明文書8頁(エ)
「血液疾患の方のうち、血小板が3万/μL 以上の方」は、研究
計画書の記載と同様に「血液疾患の方のうち、血小板が減少しているが、血小板が3万
/μL 以上の方」と記載いただいた方が理解しやすいと考えます。
③説明文書9頁(2)研究のスケジュールの箇所の2段落目、「術後1年6ヶ月(72
週)まで経過観察が行われます。」のあとに「経過観察期間中は、12 週、24 週、48 週、
72 週に来院いただき、上部消化管内視鏡検査を受けていただきます。」と加筆いただく
と被験者の方に自分が APC 治療以外に何をされるのかが理解しやすくなると考えます。
④同意書・同意撤回書の署名欄の下線が消えているので修正ください。
【回答】
ご指摘いただきありがとうございます。
該当箇所について、記載を修正致しました。
以上
72