よむ、つかう、まなぶ。
参考資料1-2 TERMS®サリドマイド製剤等安全管理手順[6.2MB] (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40908.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第3回 6/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
様式 10-A
藤本製薬株式会社
TERMS®管理センター あて
MM
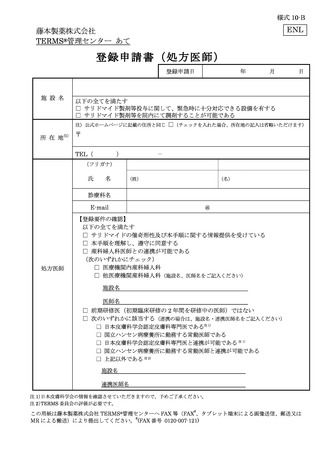
登録申請書(処方医師)
登録申請日
施 設 名
年
月
日
以下の全てを満たす
□ サリドマイド製剤等投与に関して、緊急時に十分対応できる設備を有する
□ サリドマイド製剤等を院内にて調剤することが可能である
注)公式ホームページに記載の住所と同じ □(チェックを入れた場合、所在地の記入は省略いただけます)
所 在 地注)
〒
TEL (
)
-
(フリガナ)
氏
名
(姓)
(名)
診療科名
E-mail
@
【登録要件の確認】
処方医師
以下の全てを満たす
□ サリドマイド、レナリドミドの催奇形性及び本手順に関する情報提供を受けている
□ 本手順を理解し、遵守に同意する
□ 産科婦人科医師との連携が可能である
(次のいずれかにチェック)
□ 医療機関内産科婦人科
□ 他医療機関産科婦人科(施設名、医師名をご記入ください)
施設名
医師名
□ 前期研修医(初期臨床研修の 2 年間を研修中の医師)ではない
□ 次のいずれかに該当する(連携の場合は連携医師名をご記入ください)
□ 日本血液学会認定血液専門医である注 1)
□ 同一医療機関にて日本血液学会認定血液専門医と連携が可能である・注 1)
連携医師名
□ 上記以外である 注 2)
注 1)日本血液学会の情報を確認させていただきますので、予めご了承ください。
注 2)TERMS 委員会の評価が必要です。処方医師登録審議申請書(様式 H46-A)を併せてご提出ください。
#
この用紙は藤本製薬株式会社 TERMS®管理センターへ FAX 等(FAX 、タブレット端末による画像送信、郵送又は
#
MR による搬送)により提出してください。 (FAX 番号 0120-007-121)
藤本製薬株式会社
TERMS®管理センター あて
MM
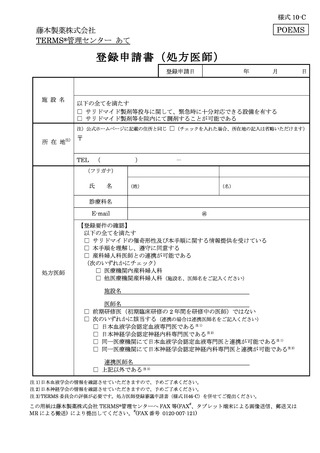
登録申請書(処方医師)
登録申請日
施 設 名
年
月
日
以下の全てを満たす
□ サリドマイド製剤等投与に関して、緊急時に十分対応できる設備を有する
□ サリドマイド製剤等を院内にて調剤することが可能である
注)公式ホームページに記載の住所と同じ □(チェックを入れた場合、所在地の記入は省略いただけます)
所 在 地注)
〒
TEL (
)
-
(フリガナ)
氏
名
(姓)
(名)
診療科名
@
【登録要件の確認】
処方医師
以下の全てを満たす
□ サリドマイド、レナリドミドの催奇形性及び本手順に関する情報提供を受けている
□ 本手順を理解し、遵守に同意する
□ 産科婦人科医師との連携が可能である
(次のいずれかにチェック)
□ 医療機関内産科婦人科
□ 他医療機関産科婦人科(施設名、医師名をご記入ください)
施設名
医師名
□ 前期研修医(初期臨床研修の 2 年間を研修中の医師)ではない
□ 次のいずれかに該当する(連携の場合は連携医師名をご記入ください)
□ 日本血液学会認定血液専門医である注 1)
□ 同一医療機関にて日本血液学会認定血液専門医と連携が可能である・注 1)
連携医師名
□ 上記以外である 注 2)
注 1)日本血液学会の情報を確認させていただきますので、予めご了承ください。
注 2)TERMS 委員会の評価が必要です。処方医師登録審議申請書(様式 H46-A)を併せてご提出ください。
#
この用紙は藤本製薬株式会社 TERMS®管理センターへ FAX 等(FAX 、タブレット端末による画像送信、郵送又は
#
MR による搬送)により提出してください。 (FAX 番号 0120-007-121)