よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
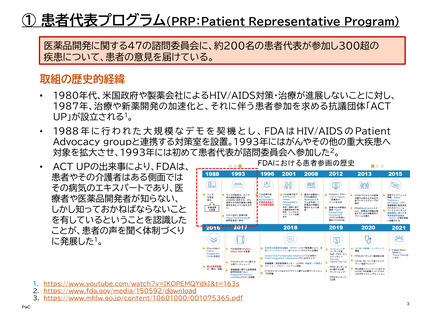
② 患者中心の医薬品開発 (PFDD: Patient-Focused Drug Development)
患者中心の医薬品開発 (PFDD)は、特定の疾患やその治療法について、患者の視点を
体系的に把握することを目的としたFDA主導の公開会議である。また、それをモデルと
して、FDA主導の会議の検討対象となる疾患以外の疾患領域に関する意見を集約する
ために患者団体が主導する会議(Externally-led PFDD)も開催されている。
FDA主導のPFDD会議
外部主導のEL-PFDD会議
会議形態
2つのパネルディスカッションとオープ
ンディスカッション。会議の大部分は、
患 者や介護者から自分の病状につい
ての見解を聞くことに費やされる。
FDAスタッフの意見を取り入れながら
患者団体が企画・主催するもので、
FDA主導のPFDD会議で確立された
プロセスをモデルとしている。
2023年実施回数
1回
13回
0回
11回
2024年実施回数
(10/1時点公開情報)
対象領域
•
•
•
•
•
1.
2.
PwC
患者からの情報提供の必要性が確認された場合
慢性的で、症状があり、機能および日常生活動作に影響を及ぼす疾患領域
臨床試験で正式には把握されていない疾患領域
現在、治療法が存在しないか、治療法が極めて少ない疾患領域、または利用可能な治療法が患
者の気分、機能、生存に直接影響しない疾患領域
特定可能な集団(子供や高齢者など)に深刻な影響を及ぼす疾病領域
https://www.fda.gov/industry/prescription-drug-user-fee-amendments/fda-led-patient-focused-drug-development-pfdd-public-meetings
https://www.fda.gov/media/160223/download?attachment
10
患者中心の医薬品開発 (PFDD)は、特定の疾患やその治療法について、患者の視点を
体系的に把握することを目的としたFDA主導の公開会議である。また、それをモデルと
して、FDA主導の会議の検討対象となる疾患以外の疾患領域に関する意見を集約する
ために患者団体が主導する会議(Externally-led PFDD)も開催されている。
FDA主導のPFDD会議
外部主導のEL-PFDD会議
会議形態
2つのパネルディスカッションとオープ
ンディスカッション。会議の大部分は、
患 者や介護者から自分の病状につい
ての見解を聞くことに費やされる。
FDAスタッフの意見を取り入れながら
患者団体が企画・主催するもので、
FDA主導のPFDD会議で確立された
プロセスをモデルとしている。
2023年実施回数
1回
13回
0回
11回
2024年実施回数
(10/1時点公開情報)
対象領域
•
•
•
•
•
1.
2.
PwC
患者からの情報提供の必要性が確認された場合
慢性的で、症状があり、機能および日常生活動作に影響を及ぼす疾患領域
臨床試験で正式には把握されていない疾患領域
現在、治療法が存在しないか、治療法が極めて少ない疾患領域、または利用可能な治療法が患
者の気分、機能、生存に直接影響しない疾患領域
特定可能な集団(子供や高齢者など)に深刻な影響を及ぼす疾病領域
https://www.fda.gov/industry/prescription-drug-user-fee-amendments/fda-led-patient-focused-drug-development-pfdd-public-meetings
https://www.fda.gov/media/160223/download?attachment
10