よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
① 患者代表プログラム(PRP:Patient Representative Program)
医薬品開発に関する47の諮問委員会に、約200名の患者代表が参加し300超の
疾患について、患者の意見を届けている。
取組の歴史的経緯
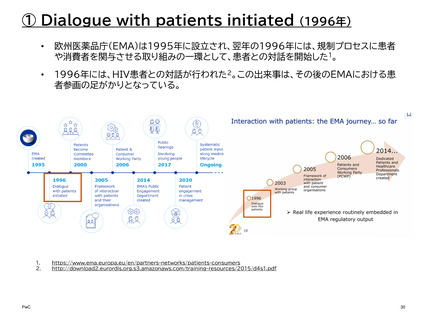
•
1980年代、米国政府や製薬会社によるHIV/AIDS対策・治療が進展しないことに対し、
1987年、治療や新薬開発の加速化と、それに伴う患者参加を求める抗議団体「ACT
UP」が設立される1。
•
1988 年 に 行 わ れ た 大 規 模 な デ モ を 契 機 と し 、 FDA は HIV/AIDS の Patient
Advocacy groupと連携する対策室を設置。1993年にはがんやその他の重大疾患へ
対象を拡大させ、1993年には初めて患者代表が諮問委員会へ参加した2。
•
ACT UPの出来事により、FDAは、
患者やその介護者はある側面では
その病気のエキスパートであり、医
療者や医薬品開発者が知らない、
しかし知っておかねばならないこと
を有しているということを認識した
ことが、患者の声を聞く体制づくり
に発展した1。
1. https://www.youtube.com/watch?v=IKOPEMQYdkI&t=163s
2. https://www.fda.gov/media/150592/download
3. https://www.mhlw.go.jp/content/10601000/001075365.pdf
PwC
3
医薬品開発に関する47の諮問委員会に、約200名の患者代表が参加し300超の
疾患について、患者の意見を届けている。
取組の歴史的経緯
•
1980年代、米国政府や製薬会社によるHIV/AIDS対策・治療が進展しないことに対し、
1987年、治療や新薬開発の加速化と、それに伴う患者参加を求める抗議団体「ACT
UP」が設立される1。
•
1988 年 に 行 わ れ た 大 規 模 な デ モ を 契 機 と し 、 FDA は HIV/AIDS の Patient
Advocacy groupと連携する対策室を設置。1993年にはがんやその他の重大疾患へ
対象を拡大させ、1993年には初めて患者代表が諮問委員会へ参加した2。
•
ACT UPの出来事により、FDAは、
患者やその介護者はある側面では
その病気のエキスパートであり、医
療者や医薬品開発者が知らない、
しかし知っておかねばならないこと
を有しているということを認識した
ことが、患者の声を聞く体制づくり
に発展した1。
1. https://www.youtube.com/watch?v=IKOPEMQYdkI&t=163s
2. https://www.fda.gov/media/150592/download
3. https://www.mhlw.go.jp/content/10601000/001075365.pdf
PwC
3