よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (45 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
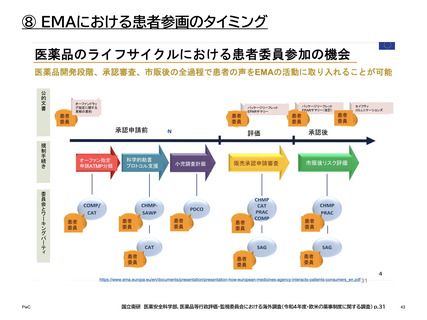
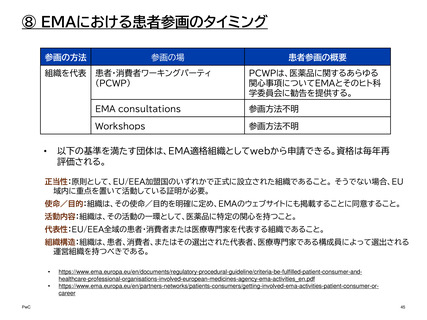
⑧ EMAにおける患者参画のタイミング
参画の方法
組織を代表
•
参画の場
患者参画の概要
患者・消費者ワーキングパーティ
(PCWP)
PCWPは、医薬品に関するあらゆる
関心事項についてEMAとそのヒト科
学委員会に勧告を提供する。
EMA consultations
参画方法不明
Workshops
参画方法不明
以下の基準を満たす団体は、EMA適格組織としてwebから申請できる。資格は毎年再
評価される。
正当性:原則として、EU/EEA加盟国のいずれかで正式に設立された組織であること。 そうでない場合、EU
域内に重点を置いて活動している証明が必要。
使命/目的:組織は、その使命/目的を明確に定め、EMAのウェブサイトにも掲載することに同意すること。
活動内容:組織は、その活動の一環として、医薬品に特定の関心を持つこと。
代表性:EU/EEA全域の患者・消費者または医療専門家を代表する組織であること。
組織構造:組織は、患者、消費者、またはその選出された代表者、医療専門家である構成員によって選出される
運営組織を持つべきである。
•
•
PwC
https://www.ema.europa.eu/en/documents/regulatory-procedural-guideline/criteria-be-fulfilled-patient-consumer-andhealthcare-professional-organisations-involved-european-medicines-agency-ema-activities_en.pdf
https://www.ema.europa.eu/en/partners-networks/patients-consumers/getting-involved-ema-activities-patient-consumer-orcareer
45
参画の方法
組織を代表
•
参画の場
患者参画の概要
患者・消費者ワーキングパーティ
(PCWP)
PCWPは、医薬品に関するあらゆる
関心事項についてEMAとそのヒト科
学委員会に勧告を提供する。
EMA consultations
参画方法不明
Workshops
参画方法不明
以下の基準を満たす団体は、EMA適格組織としてwebから申請できる。資格は毎年再
評価される。
正当性:原則として、EU/EEA加盟国のいずれかで正式に設立された組織であること。 そうでない場合、EU
域内に重点を置いて活動している証明が必要。
使命/目的:組織は、その使命/目的を明確に定め、EMAのウェブサイトにも掲載することに同意すること。
活動内容:組織は、その活動の一環として、医薬品に特定の関心を持つこと。
代表性:EU/EEA全域の患者・消費者または医療専門家を代表する組織であること。
組織構造:組織は、患者、消費者、またはその選出された代表者、医療専門家である構成員によって選出される
運営組織を持つべきである。
•
•
PwC
https://www.ema.europa.eu/en/documents/regulatory-procedural-guideline/criteria-be-fulfilled-patient-consumer-andhealthcare-professional-organisations-involved-european-medicines-agency-ema-activities_en.pdf
https://www.ema.europa.eu/en/partners-networks/patients-consumers/getting-involved-ema-activities-patient-consumer-orcareer
45