よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
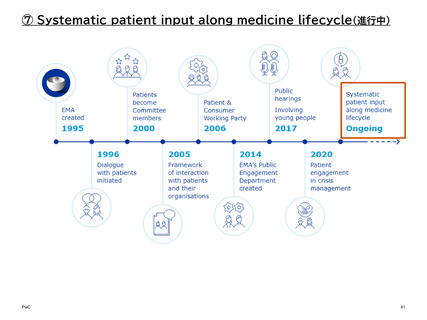
① 患者代表プログラム(PRP:Patient Representative Program)
医薬品開発パイプライン上の参画タイミング
新薬開発プロセス
この諮問委員会が開催されるのは、
NDAが提出されたタイミング。
患者代表は、会議や審査部
門との協議の中で、当局が
意見を必要とするときにい
つでも活動する。そのため、
活動頻度はニーズに応じて
異なり、1年に1回~数回活
動する人もいれば、4年間
の任期中にまったく活動し
ない人もいる。
4
https://www.fda.gov/patients/aboutoffice-patient-affairs/faqs-aboutfda-patient-representative-program
PwC
https://www.fda.gov/drugs/cder-small-business-industry-assistance-sbia/new-drugdevelopment-and-review-process
4
医薬品開発パイプライン上の参画タイミング
新薬開発プロセス
この諮問委員会が開催されるのは、
NDAが提出されたタイミング。
患者代表は、会議や審査部
門との協議の中で、当局が
意見を必要とするときにい
つでも活動する。そのため、
活動頻度はニーズに応じて
異なり、1年に1回~数回活
動する人もいれば、4年間
の任期中にまったく活動し
ない人もいる。
4
https://www.fda.gov/patients/aboutoffice-patient-affairs/faqs-aboutfda-patient-representative-program
PwC
https://www.fda.gov/drugs/cder-small-business-industry-assistance-sbia/new-drugdevelopment-and-review-process
4