よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
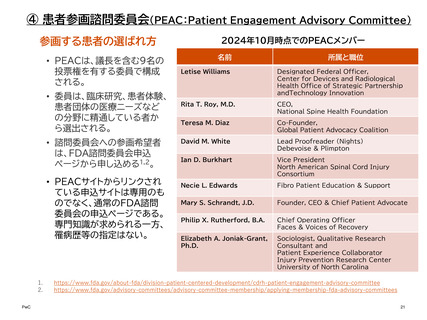
④ 患者参画諮問委員会(PEAC:Patient Engagement Advisory Committee)
•
PEACからのフィードバックを受けてFDAが実施した措置には、以下のものがある。
年次
FDAが実施した措置
2024
• 「医療機器のリコールに関する情報伝達:文献の迅速レビュー」と題する文献レビューを
実施し、公表。医療製品のリコール関連のコミュニケーションにおけるリスクコミュニケー
ションのアプローチ、方法、およびベストプラクティスに関する情報を調査。
• 患者および医療従事者によるAR/VR機器の使用に関するスペイン語のインフォグラ
フィックの作成。
• 医療機器における健康の公平性に関するディスカッションペーパーを公表。
2023
• FDAウェブサイトを更新し、患者および医療従事者によるAR/VR機器の使用に関するイ
ンフォグラフィックを追加。
2022
• FDAウェブサイトを更新し、AR/VRを搭載した医療機器のリストを追加。
• 最終ガイダンス「医療機器の臨床試験の設計と実施における患者の関与」を発行。
2021
• バーチャル公開会議 - 医療機器の製品ライフサイクル全体における患者生成ヘルスデー
タ(PGHD)を開催。
• 人工知能/機械学習(AI/ML)行動計画を発表。AI/MLアルゴリズムにおけるバイアスの
特定と排除に向けたレギュラトリーサイエンスの取り組みを支援する多様性計画を含む。
• 「患者へのサイバーセキュリティ脆弱性の伝達:フレームワークに関する検討事項」ディス
カッションガイドを掲載。
https://www.fda.gov/about-fda/division-patient-centered-development/cdrh-patient-engagement-advisory-committee
PwC
19
•
PEACからのフィードバックを受けてFDAが実施した措置には、以下のものがある。
年次
FDAが実施した措置
2024
• 「医療機器のリコールに関する情報伝達:文献の迅速レビュー」と題する文献レビューを
実施し、公表。医療製品のリコール関連のコミュニケーションにおけるリスクコミュニケー
ションのアプローチ、方法、およびベストプラクティスに関する情報を調査。
• 患者および医療従事者によるAR/VR機器の使用に関するスペイン語のインフォグラ
フィックの作成。
• 医療機器における健康の公平性に関するディスカッションペーパーを公表。
2023
• FDAウェブサイトを更新し、患者および医療従事者によるAR/VR機器の使用に関するイ
ンフォグラフィックを追加。
2022
• FDAウェブサイトを更新し、AR/VRを搭載した医療機器のリストを追加。
• 最終ガイダンス「医療機器の臨床試験の設計と実施における患者の関与」を発行。
2021
• バーチャル公開会議 - 医療機器の製品ライフサイクル全体における患者生成ヘルスデー
タ(PGHD)を開催。
• 人工知能/機械学習(AI/ML)行動計画を発表。AI/MLアルゴリズムにおけるバイアスの
特定と排除に向けたレギュラトリーサイエンスの取り組みを支援する多様性計画を含む。
• 「患者へのサイバーセキュリティ脆弱性の伝達:フレームワークに関する検討事項」ディス
カッションガイドを掲載。
https://www.fda.gov/about-fda/division-patient-centered-development/cdrh-patient-engagement-advisory-committee
PwC
19