よむ、つかう、まなぶ。
【資料3-2】医薬品等行政評価・監視委員会における海外調査(FDA、EMAにおける患者、市民参画の取組)[3.8MB] (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_47693.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第18回 12/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
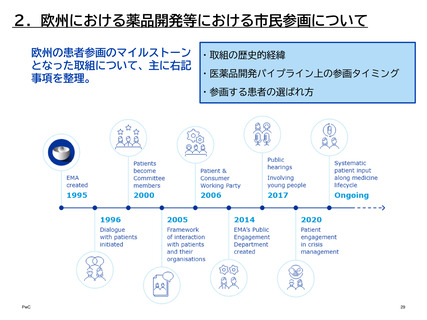
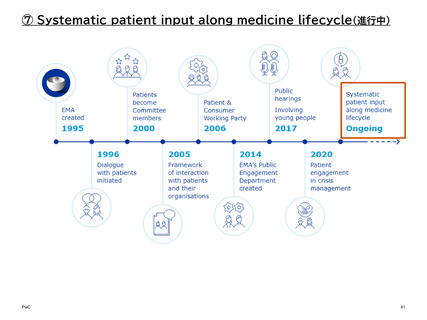
① Dialogue with patients initiated (1996年)
•
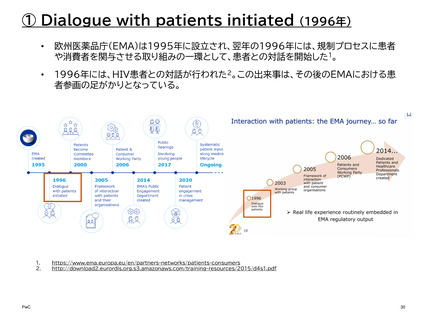
欧州医薬品庁(EMA)は1995年に設立され、翌年の1996年には、規制プロセスに患者
や消費者を関与させる取り組みの一環として、患者との対話を開始した1。
•
1996年には、HIV患者との対話が行われた2。この出来事は、その後のEMAにおける患
者参画の足がかりとなっている。
1.
2.
PwC
https://www.ema.europa.eu/en/partners-networks/patients-consumers
http://download2.eurordis.org.s3.amazonaws.com/training-resources/2015/d4s1.pdf
30
•
欧州医薬品庁(EMA)は1995年に設立され、翌年の1996年には、規制プロセスに患者
や消費者を関与させる取り組みの一環として、患者との対話を開始した1。
•
1996年には、HIV患者との対話が行われた2。この出来事は、その後のEMAにおける患
者参画の足がかりとなっている。
1.
2.
PwC
https://www.ema.europa.eu/en/partners-networks/patients-consumers
http://download2.eurordis.org.s3.amazonaws.com/training-resources/2015/d4s1.pdf
30