よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.4MB] (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
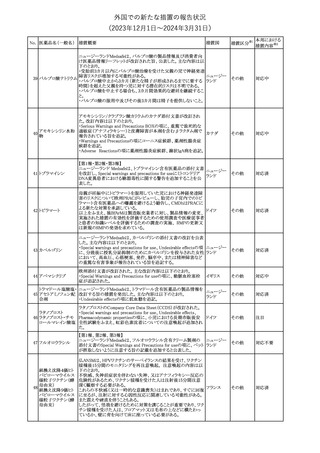
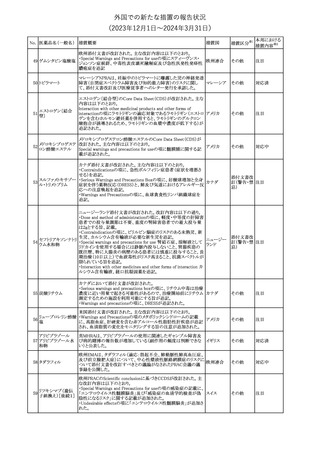
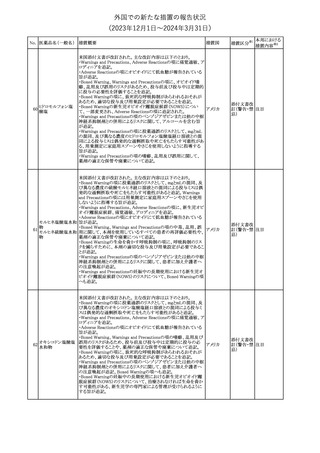
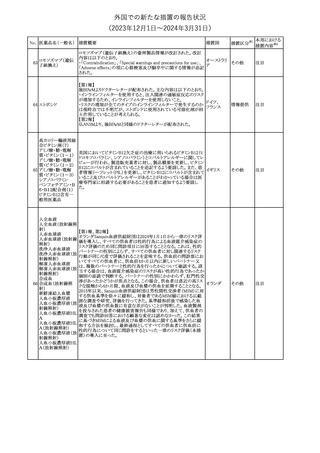
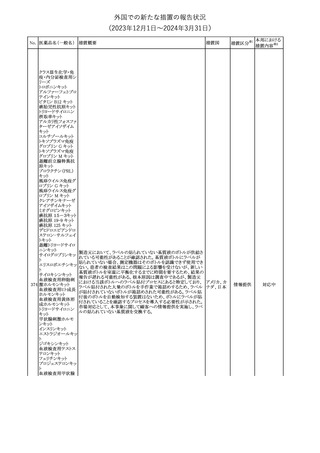
外国での新たな措置の報告状況
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
【第1,2,3報】
仏ANSMは、プロゲスチン単剤治療における髄膜腫リスクを監視する
臨時科学委員会の助言に従い、リスクを最小限にするための推奨
事項を作成した。
<medrogestone>
以下の適応の第一選択薬として使用しないこと。
・更年期障害、エストロゲンと組み合わせた人工周期
・サイクルの不規則性
・月経前症候群(本態性月経困難症)
・非重度の乳房痛(肥満痛)
脳画像によるモニタリングが推奨される。
<メドロキシプロゲステロン酢酸エステル>
他の避妊方法を使用できない場合に使用すること。
脳画像によるモニタリングが推奨される。
<promegestone:2020年に販売終了>
5年以上治療された後、リスクのあるプロゲスチン(cyproterone
acetate、酢酸クロルマジノン、nomegestrol acetate、medrogestone、
メドロキシプロゲステロン酢酸エステル)又は髄膜腫のリスクが確認さ
れていないプロゲスチン(ジエノゲスト、ドロスピレノン、デソゲストレ
メドロキシプロゲステ ル)のいずれかで治療された場合には脳MRIを実施する必要があ
ロン酢酸エステル
る。
78 ドロスピレノン・エチ 患者に髄膜腫を示唆する兆候がある場合には、promegestone投与 フランス
ニルエストラジオー を中止予定であっても脳MRIを実施すること。
ル ベータデクス
<黄体ホルモン作用物質全般の使用及び黄体ホルモン物質から別
の黄体ホルモン作用物質への切替えに関する注意事項>
・髄膜腫の既往があるか、現在髄膜腫が存在する場合、髄膜腫リス
クのあるプロゲスチン(cyproterone acetate、酢酸クロルマジノン、
nomegestrol acetate、medrogestone、メドロキシプロゲステロン酢酸
エステル)を投与してはならない。
・cyproterone acetate、酢酸クロルマジノン、nomegestrol acetate、
medrogestone、メドロキシプロゲステロン酢酸エステル又は
promegestoneによる治療の代替として新しいプロゲスチンを処方す
ることの髄膜腫を発症するリスクは、除外できないが決定されていな
い。
・これらのプロゲスチンを1年以上使用し、治療が高リスクのプロゲス
チン又は髄膜腫リスクが知られていないプロゲスチンに変更された
場合は、切り替え時に脳MRIを実施する必要がある。
・処方にあたっては、最小有効量を可能な限り短期間で投与する。
・投与の継続が有益か否かを定期的に(年1回)評価すること。特に
閉経前後には、髄膜腫のリスクが加齢とともに著明に上昇することに
留意する。
・髄膜腫を示唆する神経学的臨床徴候がみられる場合には脳MRI
を実施する必要がある。
その他
対応中
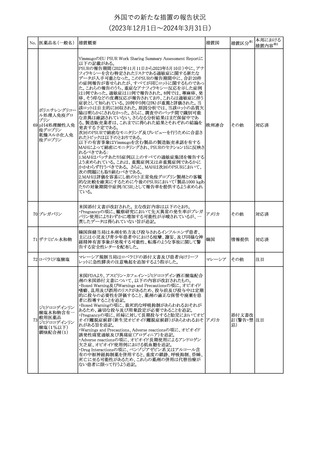
第23回 Summary Monthly Safety Report (SMSR)(報告期間:2023
年11月1日~2023年11月30日)を入手したもの。報告期間中、安全
ニルマトレルビル・リ
79
性懸念リストに変更はなかった。今回の報告期間中に皮膚反応の安 アメリカ
トナビル
全性シグナルが開始され、現在のData Lock Pointにおいても評価
中である。
その他
注目
ヒドロコルチゾンコハ ヒドロコルチゾンコハク酸ナトリウム静注用製剤の米国添付文書が改
80 ク酸ナトリウム含有 訂された。主な内容は以下のとおり。
アメリカ
一般用医薬品
Warnings and Precautionsに腫瘍崩壊症候群に関して追記された。
その他
注目
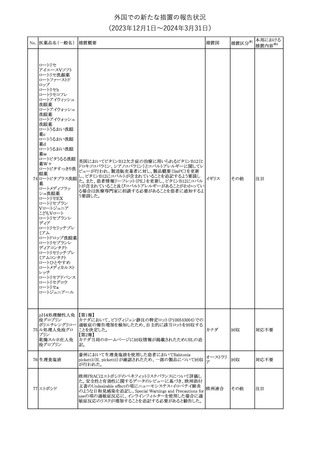
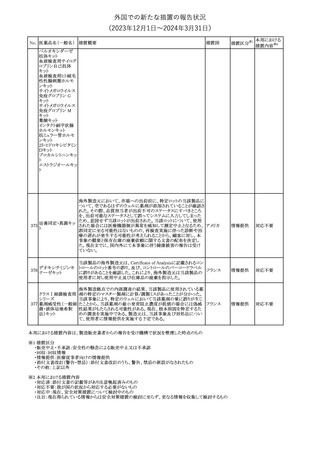
欧州SmPCの以下の点が改訂された。
①Special warning and precautions for useの項に、静脈瘤患者への
使用(この医薬品は、静脈壁のびらんや出血リスクを防ぐために、静
脈瘤の領域では注意して使用する必要がある。)を追記
パイナップル茎搾汁
81
②Drug interactionsの項のCYP2C8基質からrosiglitazone、sorafenib ドイツ
精製物
を削除。
③Undesirable effectsの項の 「創傷感染」を「蜂窩織炎を含む創傷
感染」に変更し、「適用部位発疹」、「適用部位掻痒感」、 「皮下血
腫」を追加。
その他
注目
No. 医薬品名(一般名) 措置概要
措置国
14
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
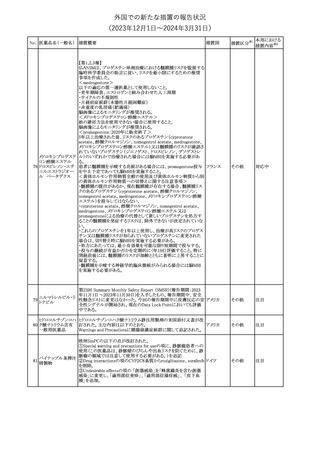
【第1,2,3報】
仏ANSMは、プロゲスチン単剤治療における髄膜腫リスクを監視する
臨時科学委員会の助言に従い、リスクを最小限にするための推奨
事項を作成した。
<medrogestone>
以下の適応の第一選択薬として使用しないこと。
・更年期障害、エストロゲンと組み合わせた人工周期
・サイクルの不規則性
・月経前症候群(本態性月経困難症)
・非重度の乳房痛(肥満痛)
脳画像によるモニタリングが推奨される。
<メドロキシプロゲステロン酢酸エステル>
他の避妊方法を使用できない場合に使用すること。
脳画像によるモニタリングが推奨される。
<promegestone:2020年に販売終了>
5年以上治療された後、リスクのあるプロゲスチン(cyproterone
acetate、酢酸クロルマジノン、nomegestrol acetate、medrogestone、
メドロキシプロゲステロン酢酸エステル)又は髄膜腫のリスクが確認さ
れていないプロゲスチン(ジエノゲスト、ドロスピレノン、デソゲストレ
メドロキシプロゲステ ル)のいずれかで治療された場合には脳MRIを実施する必要があ
ロン酢酸エステル
る。
78 ドロスピレノン・エチ 患者に髄膜腫を示唆する兆候がある場合には、promegestone投与 フランス
ニルエストラジオー を中止予定であっても脳MRIを実施すること。
ル ベータデクス
<黄体ホルモン作用物質全般の使用及び黄体ホルモン物質から別
の黄体ホルモン作用物質への切替えに関する注意事項>
・髄膜腫の既往があるか、現在髄膜腫が存在する場合、髄膜腫リス
クのあるプロゲスチン(cyproterone acetate、酢酸クロルマジノン、
nomegestrol acetate、medrogestone、メドロキシプロゲステロン酢酸
エステル)を投与してはならない。
・cyproterone acetate、酢酸クロルマジノン、nomegestrol acetate、
medrogestone、メドロキシプロゲステロン酢酸エステル又は
promegestoneによる治療の代替として新しいプロゲスチンを処方す
ることの髄膜腫を発症するリスクは、除外できないが決定されていな
い。
・これらのプロゲスチンを1年以上使用し、治療が高リスクのプロゲス
チン又は髄膜腫リスクが知られていないプロゲスチンに変更された
場合は、切り替え時に脳MRIを実施する必要がある。
・処方にあたっては、最小有効量を可能な限り短期間で投与する。
・投与の継続が有益か否かを定期的に(年1回)評価すること。特に
閉経前後には、髄膜腫のリスクが加齢とともに著明に上昇することに
留意する。
・髄膜腫を示唆する神経学的臨床徴候がみられる場合には脳MRI
を実施する必要がある。
その他
対応中
第23回 Summary Monthly Safety Report (SMSR)(報告期間:2023
年11月1日~2023年11月30日)を入手したもの。報告期間中、安全
ニルマトレルビル・リ
79
性懸念リストに変更はなかった。今回の報告期間中に皮膚反応の安 アメリカ
トナビル
全性シグナルが開始され、現在のData Lock Pointにおいても評価
中である。
その他
注目
ヒドロコルチゾンコハ ヒドロコルチゾンコハク酸ナトリウム静注用製剤の米国添付文書が改
80 ク酸ナトリウム含有 訂された。主な内容は以下のとおり。
アメリカ
一般用医薬品
Warnings and Precautionsに腫瘍崩壊症候群に関して追記された。
その他
注目
欧州SmPCの以下の点が改訂された。
①Special warning and precautions for useの項に、静脈瘤患者への
使用(この医薬品は、静脈壁のびらんや出血リスクを防ぐために、静
脈瘤の領域では注意して使用する必要がある。)を追記
パイナップル茎搾汁
81
②Drug interactionsの項のCYP2C8基質からrosiglitazone、sorafenib ドイツ
精製物
を削除。
③Undesirable effectsの項の 「創傷感染」を「蜂窩織炎を含む創傷
感染」に変更し、「適用部位発疹」、「適用部位掻痒感」、 「皮下血
腫」を追加。
その他
注目
No. 医薬品名(一般名) 措置概要
措置国
14