よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.4MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
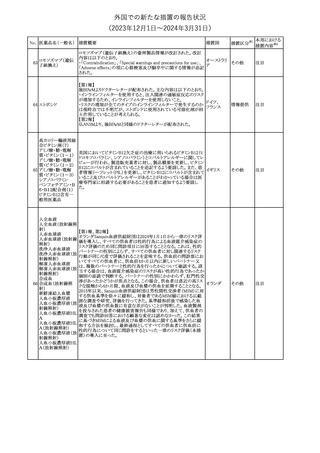
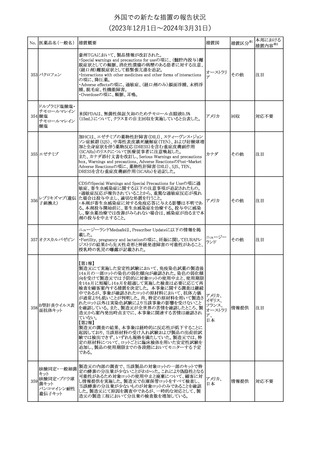
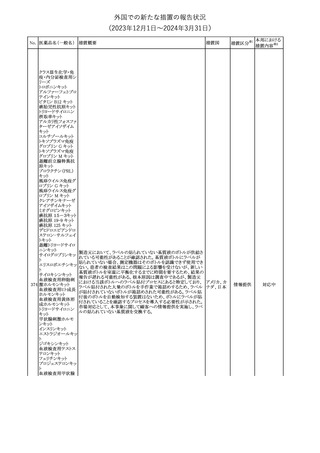
外国での新たな措置の報告状況
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
その他
注目
【第1報】
ロシア保健省連邦国家予算機関SCEEMPよりセファロスポリンの有
害事象として、痙攣及び神経毒性(脳症、けいれん、ミオクローヌス)
発症のリスクについて、添付文書に記載することが求められた。
【第2報】
マレーシアNPRAは、セファロスポリンの使用と発作のリスクとの間に ロシア、
セフジトレン ピボキ
14
潜在的な関連性があることに注意しながら使用することよう注意喚起 マレーシア、 その他
シル
を発表した。
カナダ
【第3報】
ロシア医薬品・医療機器流通規制局は、SCEEMPの求めに応じ、セ
ファロスポリンの有害事象として、痙攣及び神経毒性(脳症、けいれ
ん、ミオクローヌス)発症について添付文書改訂する勧告を通知し
た。
注目
No. 医薬品名(一般名) 措置概要
措置国
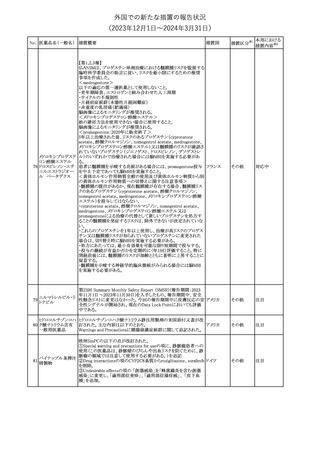
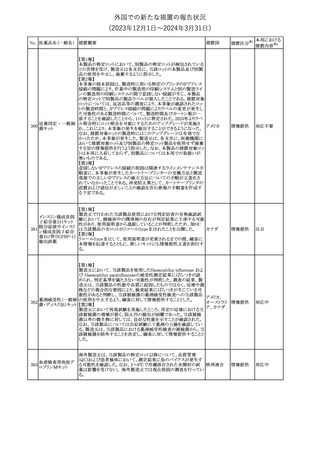
欧州において、PRACよりイブプロフェン含有製剤の添付文書につ
いて以下の内容を改訂するよう勧告され、CMDhが合意したもの。
【局所製剤】
・Contraindicationsの項、経口剤等と同様に妊娠後期を禁忌とする
こと。また、妊娠前期及び妊娠中期では必要な場合のみ使用し、使
用の際には可能な限り投与量及び投与期間を少なくすることを追
イブプロフェン含有 記。
13
欧州連合
一般用医薬品
【全身製剤】
・Special Warnings and Precautions for Use及びUndesirable Effects
の項、コーニス症候群を追記。
【全身製剤、局所製剤共通】
・Special Warnings and Precautions for Use及びUndesirable Effects
の項、重度の皮膚障害(Drug Reaction with Eosinophilia and
Systemic Symptoms(DRESS)を含む)を追記。
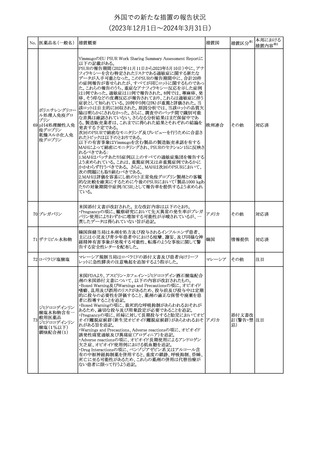
15 レベチラセタム
【第1報】【第2報】【第3報】
米 FDAは、レベチラセタムの製品情報に好酸球増加と全身症状を
アメリカ
伴う薬物反応(DRESS)のリスクに関する警告を追加するよう勧告し
た。
その他
対応済
16 フルコナゾール
欧州PRACは、以下の欧州添付文書のFertility, pregnancy and
lactation の項の改訂を勧告した。
・妊娠の可能性のある女性の項が新たに追加され、以下の内容を記
載。
治療を開始する前に、患者には胎児に対する潜在的なリスクについ
て説明する必要がある。
単回投与後、妊娠前に1週間(5~6半減期に相当)の休薬期間が推
欧州連合
奨される。より長い治療期間の場合、治療期間中及び最終投与後1
週間は避妊が必要に応じて考慮される。
・妊娠の項に、以下の内容を追記。
妊娠初期にフルコナゾールに曝露された数千人の妊婦を含む5件
の観察研究のメタアナリシスでは、フルコナゾールを使用しなかった
場合やアゾールの局所使用と比較した場合、心臓奇形のリスクが
1.8~2倍増加した。
その他
注目
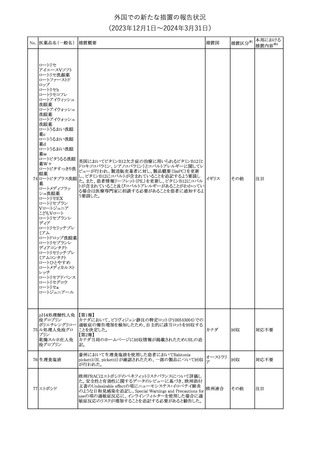
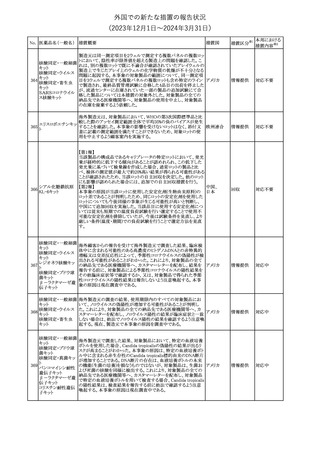
レボチロキシンナトリウムの米国添付文書が改訂された。主な改訂
内容は以下のとおり。
・「Warnings and precautions」の過量投与又は過少投与に関連した
リスクに関する記載の項に、
レボチロキシンナトリ
17
「Use in specific populations」の「Pediatric use」の項に記載のあっ アメリカ
ウム水和物
た、先天性及び後天性甲状腺機能低下症の小児患者では、過小
治療は認知発達や線形成長に悪影響を与える可能性があり、過剰
治療は頭蓋骨癒合症や骨年齢の加速と関連するとの旨が追記され
た。
その他
注目
米国添文のDrug Interactionsの項に、妊娠可能な女性対象の薬物
ベロトラルスタット塩 相互作用試験において、本剤と経口避妊薬であるデソゲストレル・
18
アメリカ
酸塩
エチニルエストラジオール錠の併用により、デソゲストレルの曝露量
が増加した旨追記された。
その他
対応済
回収
対応不要
19 ドネペジル塩酸塩
カナダにおいて、ドネペジル塩酸塩10mg錠の一部のボトルにサイズ
超過の錠剤が含まれている可能性があるため、1ロットが回収され
カナダ
た。
4
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
その他
注目
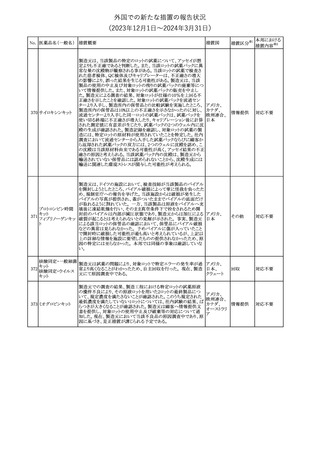
【第1報】
ロシア保健省連邦国家予算機関SCEEMPよりセファロスポリンの有
害事象として、痙攣及び神経毒性(脳症、けいれん、ミオクローヌス)
発症のリスクについて、添付文書に記載することが求められた。
【第2報】
マレーシアNPRAは、セファロスポリンの使用と発作のリスクとの間に ロシア、
セフジトレン ピボキ
14
潜在的な関連性があることに注意しながら使用することよう注意喚起 マレーシア、 その他
シル
を発表した。
カナダ
【第3報】
ロシア医薬品・医療機器流通規制局は、SCEEMPの求めに応じ、セ
ファロスポリンの有害事象として、痙攣及び神経毒性(脳症、けいれ
ん、ミオクローヌス)発症について添付文書改訂する勧告を通知し
た。
注目
No. 医薬品名(一般名) 措置概要
措置国
欧州において、PRACよりイブプロフェン含有製剤の添付文書につ
いて以下の内容を改訂するよう勧告され、CMDhが合意したもの。
【局所製剤】
・Contraindicationsの項、経口剤等と同様に妊娠後期を禁忌とする
こと。また、妊娠前期及び妊娠中期では必要な場合のみ使用し、使
用の際には可能な限り投与量及び投与期間を少なくすることを追
イブプロフェン含有 記。
13
欧州連合
一般用医薬品
【全身製剤】
・Special Warnings and Precautions for Use及びUndesirable Effects
の項、コーニス症候群を追記。
【全身製剤、局所製剤共通】
・Special Warnings and Precautions for Use及びUndesirable Effects
の項、重度の皮膚障害(Drug Reaction with Eosinophilia and
Systemic Symptoms(DRESS)を含む)を追記。
15 レベチラセタム
【第1報】【第2報】【第3報】
米 FDAは、レベチラセタムの製品情報に好酸球増加と全身症状を
アメリカ
伴う薬物反応(DRESS)のリスクに関する警告を追加するよう勧告し
た。
その他
対応済
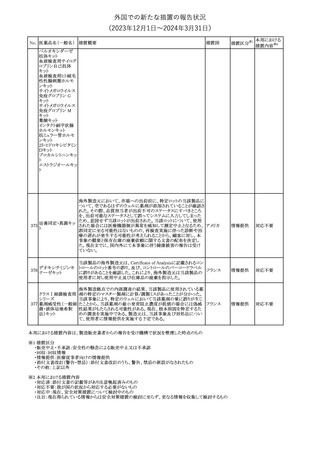
16 フルコナゾール
欧州PRACは、以下の欧州添付文書のFertility, pregnancy and
lactation の項の改訂を勧告した。
・妊娠の可能性のある女性の項が新たに追加され、以下の内容を記
載。
治療を開始する前に、患者には胎児に対する潜在的なリスクについ
て説明する必要がある。
単回投与後、妊娠前に1週間(5~6半減期に相当)の休薬期間が推
欧州連合
奨される。より長い治療期間の場合、治療期間中及び最終投与後1
週間は避妊が必要に応じて考慮される。
・妊娠の項に、以下の内容を追記。
妊娠初期にフルコナゾールに曝露された数千人の妊婦を含む5件
の観察研究のメタアナリシスでは、フルコナゾールを使用しなかった
場合やアゾールの局所使用と比較した場合、心臓奇形のリスクが
1.8~2倍増加した。
その他
注目
レボチロキシンナトリウムの米国添付文書が改訂された。主な改訂
内容は以下のとおり。
・「Warnings and precautions」の過量投与又は過少投与に関連した
リスクに関する記載の項に、
レボチロキシンナトリ
17
「Use in specific populations」の「Pediatric use」の項に記載のあっ アメリカ
ウム水和物
た、先天性及び後天性甲状腺機能低下症の小児患者では、過小
治療は認知発達や線形成長に悪影響を与える可能性があり、過剰
治療は頭蓋骨癒合症や骨年齢の加速と関連するとの旨が追記され
た。
その他
注目
米国添文のDrug Interactionsの項に、妊娠可能な女性対象の薬物
ベロトラルスタット塩 相互作用試験において、本剤と経口避妊薬であるデソゲストレル・
18
アメリカ
酸塩
エチニルエストラジオール錠の併用により、デソゲストレルの曝露量
が増加した旨追記された。
その他
対応済
回収
対応不要
19 ドネペジル塩酸塩
カナダにおいて、ドネペジル塩酸塩10mg錠の一部のボトルにサイズ
超過の錠剤が含まれている可能性があるため、1ロットが回収され
カナダ
た。
4