よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.4MB] (47 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
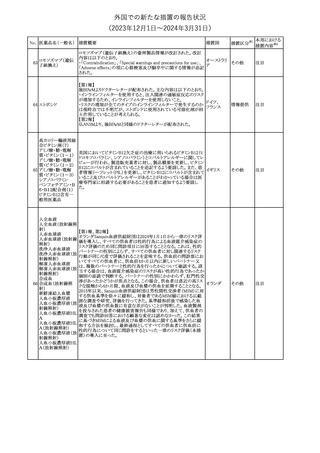
外国での新たな措置の報告状況
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
その他
対応済
スイス
その他
注目
オランダ
その他
注目
【第1報】
欧州PRACは、ガドテリドールのPeriodic safety update reports
(PSURs)を公表し、ガドテリドールと妊娠中投与のリスク及び髄腔内
投与によるリスクとの因果関係には、合理的な可能性があると考え、
製品情報の改訂が公表された。主な改訂内容は以下の通り。
・Warningの項に髄腔内に使用してはならない旨の追記
・Pregnancyの項に妊婦におけるガドリニウム系造影剤の使用に関す
るデータは限られていること、ガドリニウムは胎盤を通過できること、
ガドリニウムへの曝露が胎児への有害影響と関連するかどうかは不
明であることが追記
【第2報】
欧州EMAよりPRAC会合の議事録が公表された。ガドテリドールに関
する主な内容は以下のとおり。
欧州連合
・有効性及び安全性のデータから、ガドテリドール含有医薬品のベ
ネフィットリスクバランスは保たれている。
・製品情報の改訂勧告:
○髄腔内に投与しないことを示す警告を含むこと
○妊婦への使用に関するデータは限られており、ガドリニウムへの
曝露が乳児への影響と関連しているかどうかは不明であることを反
映すること
・次回のPSURにおいて、ガドリニウム投与を受けた妊婦から出生し
た乳児への影響についての情報を評価し、製品情報の更新が必要
かどうかを検討すべきである
・ガドテリドールを投与された母親からの授乳による乳児への影響に
ついての情報を評価し、製品情報の更新が必要かどうかを検討す
べきである
その他
注目
No. 医薬品名(一般名) 措置概要
措置国
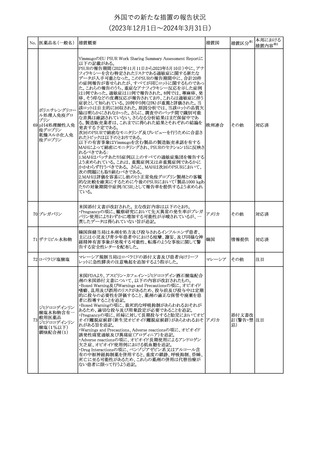
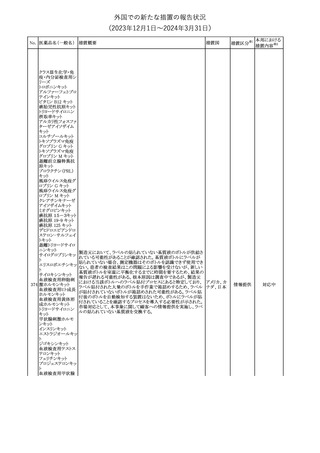
【第1報】
独BfArmは、クロルマジノン酢酸エステル/エチニルエストラジオール
配合避妊薬について、Direct Healthcare Professional
Communication(DHPC)を公表した。主な内容は以下のとおり。
後ろ向きコホート研究RIVET-RCS1において、クロルマジノン酢酸エ
ステル/エチニルエストラジオール含有避妊薬を服用した女性は、レ
クロルマジノン酢酸
ボノルゲストレル/エチニルエストラジオール含有避妊薬を服用した
エステル
女性と比較して、静脈血栓塞栓症のリスクが1.25倍高かった。
デソゲストレル・エチ
【第2報】
ニルエストラジオー
欧州CMDhはPRAC評価報告書に基づき、承認後安全性試験
ル
(PASS)(後ろ向きコホート研究RIVET-RCS1)の結果を踏まえ、クロ ドイツ、
283 レボノルゲストレル・
ルマジノン酢酸エステル又はエチニルエストラジオール配合避妊薬 欧州連合
エチニルエストラジ
の製品情報の変更を勧告した。主な内容は以下のとおり。
オール
Special warnings and precautions for use の項に以下を追記する。
ノルエチステロン・エ
・クロルマジノン酢酸エステル/エチニルエストラジオールを含有する
チニルエストラジ
複合ホルモン避妊薬(CHC)は、レボノルゲストレル/エチニルエスト
オール
ラジオール含有避妊薬と比較して静脈血栓塞栓症のリスクが 1.25
倍増加する可能性がある
・レボノルゲストレルを含むCHCを使用している女性1万人のうち1年
間に静脈血栓塞栓症を発症する女性約6人と推定されるのに対し、
クロルマジノン酢酸エステルを含むCHCを使用する女性では1万人
のうち6~9人と推定される
284
セクキヌマブ(遺伝
子組換え)
CCDSが改訂された。主な改訂内容は以下のとおり。
・.Warnings and PrecautionsのHypersensitivity reactionsの項に血
管浮腫が追記された。
欧州PRACの勧告により、全身性製剤について以下の欧州添付文
書改訂が行われる予定。
・Special warnings and precautions for useのSevere cutaneous
モキシフロキサシン
adverse reactionsに、好酸球増加と全身症状を伴う薬物反応
285
塩酸塩
(DRESS)を追記。
・Undesirable effectsの項にDRESS、固定薬疹、光線過敏性反応を
追記。
286 ガドテリドール
47
(2023年12⽉1⽇〜2024年3⽉31⽇)
措置区分※1
本邦における
措置内容※2
その他
対応済
スイス
その他
注目
オランダ
その他
注目
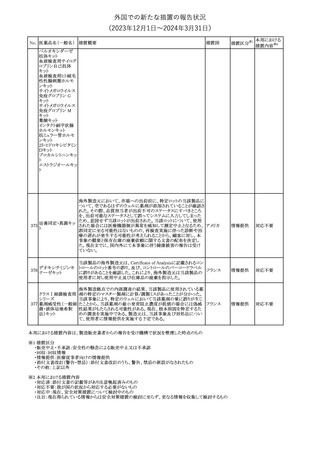
【第1報】
欧州PRACは、ガドテリドールのPeriodic safety update reports
(PSURs)を公表し、ガドテリドールと妊娠中投与のリスク及び髄腔内
投与によるリスクとの因果関係には、合理的な可能性があると考え、
製品情報の改訂が公表された。主な改訂内容は以下の通り。
・Warningの項に髄腔内に使用してはならない旨の追記
・Pregnancyの項に妊婦におけるガドリニウム系造影剤の使用に関す
るデータは限られていること、ガドリニウムは胎盤を通過できること、
ガドリニウムへの曝露が胎児への有害影響と関連するかどうかは不
明であることが追記
【第2報】
欧州EMAよりPRAC会合の議事録が公表された。ガドテリドールに関
する主な内容は以下のとおり。
欧州連合
・有効性及び安全性のデータから、ガドテリドール含有医薬品のベ
ネフィットリスクバランスは保たれている。
・製品情報の改訂勧告:
○髄腔内に投与しないことを示す警告を含むこと
○妊婦への使用に関するデータは限られており、ガドリニウムへの
曝露が乳児への影響と関連しているかどうかは不明であることを反
映すること
・次回のPSURにおいて、ガドリニウム投与を受けた妊婦から出生し
た乳児への影響についての情報を評価し、製品情報の更新が必要
かどうかを検討すべきである
・ガドテリドールを投与された母親からの授乳による乳児への影響に
ついての情報を評価し、製品情報の更新が必要かどうかを検討す
べきである
その他
注目
No. 医薬品名(一般名) 措置概要
措置国
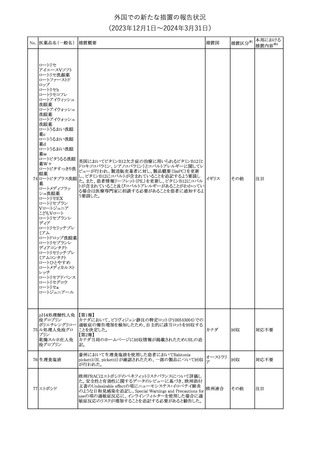
【第1報】
独BfArmは、クロルマジノン酢酸エステル/エチニルエストラジオール
配合避妊薬について、Direct Healthcare Professional
Communication(DHPC)を公表した。主な内容は以下のとおり。
後ろ向きコホート研究RIVET-RCS1において、クロルマジノン酢酸エ
ステル/エチニルエストラジオール含有避妊薬を服用した女性は、レ
クロルマジノン酢酸
ボノルゲストレル/エチニルエストラジオール含有避妊薬を服用した
エステル
女性と比較して、静脈血栓塞栓症のリスクが1.25倍高かった。
デソゲストレル・エチ
【第2報】
ニルエストラジオー
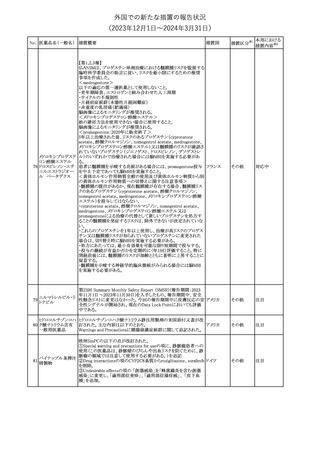
欧州CMDhはPRAC評価報告書に基づき、承認後安全性試験
ル
(PASS)(後ろ向きコホート研究RIVET-RCS1)の結果を踏まえ、クロ ドイツ、
283 レボノルゲストレル・
ルマジノン酢酸エステル又はエチニルエストラジオール配合避妊薬 欧州連合
エチニルエストラジ
の製品情報の変更を勧告した。主な内容は以下のとおり。
オール
Special warnings and precautions for use の項に以下を追記する。
ノルエチステロン・エ
・クロルマジノン酢酸エステル/エチニルエストラジオールを含有する
チニルエストラジ
複合ホルモン避妊薬(CHC)は、レボノルゲストレル/エチニルエスト
オール
ラジオール含有避妊薬と比較して静脈血栓塞栓症のリスクが 1.25
倍増加する可能性がある
・レボノルゲストレルを含むCHCを使用している女性1万人のうち1年
間に静脈血栓塞栓症を発症する女性約6人と推定されるのに対し、
クロルマジノン酢酸エステルを含むCHCを使用する女性では1万人
のうち6~9人と推定される
284
セクキヌマブ(遺伝
子組換え)
CCDSが改訂された。主な改訂内容は以下のとおり。
・.Warnings and PrecautionsのHypersensitivity reactionsの項に血
管浮腫が追記された。
欧州PRACの勧告により、全身性製剤について以下の欧州添付文
書改訂が行われる予定。
・Special warnings and precautions for useのSevere cutaneous
モキシフロキサシン
adverse reactionsに、好酸球増加と全身症状を伴う薬物反応
285
塩酸塩
(DRESS)を追記。
・Undesirable effectsの項にDRESS、固定薬疹、光線過敏性反応を
追記。
286 ガドテリドール
47