よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.4MB] (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
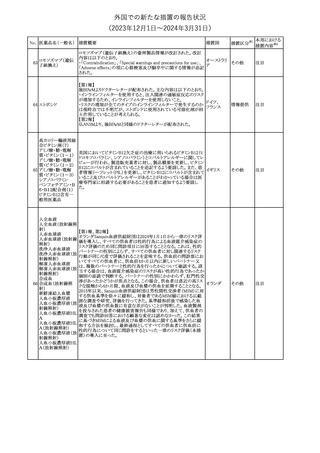
外国での新たな措置の報告状況
(2023年12⽉1⽇〜2024年3⽉31⽇)
No. 医薬品名(一般名) 措置概要
措置国
アスピリン・カフェイン・ジヒドロコデイン酒石酸塩配合剤の米国添付
文書が改訂された。主な改訂内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項にオピオイド誘
発痛覚過敏、アロディニアを追記。
・Adverse Reactionsの項にオピオイドにて低血糖が報告されている
旨が追記。
ジヒドロコデインリン ・Boxed Warning、Pregnancyの項に、妊婦に対して長期投与すると
酸塩(1%以下)
新生児においてオピオイド離脱症候群があらわれるおそれがある旨
101 ジヒドロコデインリン を追記。
アメリカ
酸塩(1%以下)
その他、以下のとおり一部追記、変更がなされている。
鎮咳配合剤(1)
・Boxed Warningの項の中毒、乱用、誤用に関して、本剤を使用して
いるすべての患者の再評価必要性について追記。
・Boxed Warningの項の生命を脅かす呼吸抑制に関して、呼吸抑制
のリスクを減らすために、本剤の適切な投与量及び漸増が必要であ
ることが追記。
・Warnings and Precautionsのベンゾジアゼピン又は他の中枢神経
抑制剤との併用リスクについて、Boxed Warningの項へも追記。
102
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
【第1報】【第2報】
エルサルバ
パロキセチン塩酸塩
エルサルバドル規制当局は、白血球減少、歯ぎしり、顕微鏡的大腸 ドル、
その他
水和物
炎のリスクについて注意喚起するよう要請した。
パナマ
注目
米国添付文書が改訂された。主な改訂内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項に痛覚過敏、ア
ロディニアを追記。
・Adverse Reactionsの項にオピオイドにて低血糖が報告されている
旨が追記。
タペンタドール塩酸 その他、以下のとおり一部追記、変更がなされている。
103
アメリカ
塩
・Boxed Warningの項に、オピオイド嗜癖、乱用及び誤用のリスクが
あるため、投与前及び投与中は定期的に投与の必要性を評価する
こと、薬剤の適正な保管や廃棄を患者に指導することを追記。
・Warnings and Precautionsの項に投薬過誤のリスクに関して、同封
の目盛りシリンジを使用し、用量測定に家庭用スプーンやさじを使
用しないように指導する旨が追記。
その他
注目
米国FDAより、コデインリン酸塩・フェニレフリン塩酸塩・プロメタジン
プロメタジン塩酸塩 塩酸塩配合剤の米国添付文書について、以下の内容が改訂された
104 ヒベンズ酸プロメタジ もの。
アメリカ
ン
・Adverse reactionsの項に、オピオイド使用例における低血糖を追
記。
その他
注目
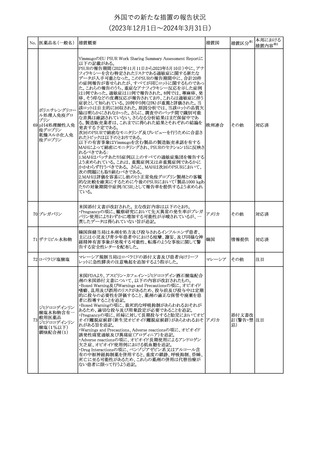
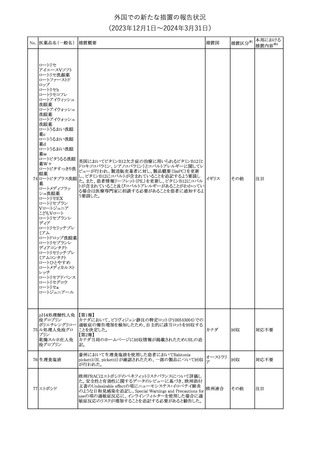
105 アロプリノール
シンガポール規制当局より、医療従事者向けにアロプリノールの処
方に関し情報提供がなされた。主な内容は以下のとおり。
・アロプリノール治療に対する患者の適合性を慎重に評価し、患者
のリスク因子を考慮する。
・可能な場合はリスク因子に対処し、アロプリノールを低用量で開始
し、徐々に増量することにより、SCAR(重度皮膚有害反応)発症のリ
スクを軽減するす。
シンガポー
情報提供
・腎機能障害や高齢など、アロプリノール誘発性 SCAR の既存のリ ル
スク因子を持つ患者に対して、特にリスクが高い患者を特定するた
め、HLA-B*5801遺伝子型解析を検討する。
・患者が適切な意思決定を行えるように、HLA-B*5801検査の利点
と費用について患者と話し合う。
・SCAR の初期の兆候や症状がないか患者を注意深くモニターす
る。
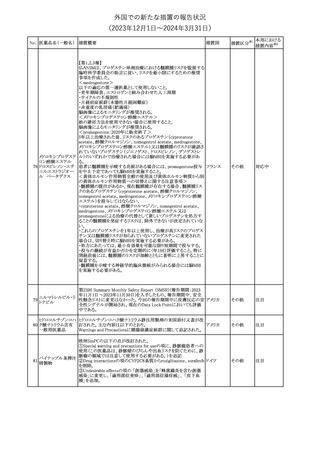
欧州にて、妊娠の可能性がある女性におけるバルプロ酸使用中止
後の治療戦略を調査するため非介入承認後安全性試験(PASS)が
実施され、報告書が公表された。慢性使用後のバルプロ酸中止が
半数の症例で維持された。バルプロ酸中止の成功に関連する要因
106 バルプロ酸ナトリウム
欧州連合
は、若年、病歴が短い、検査による患者管理が良好であること、投与
中止前の用量漸減、及び以前の特定薬剤継続使用歴であった。用
量漸減段階に伴う計画的妊娠がバルプロ酸中止成功の強力なプラ
ス要因であるとした。
20
その他
対応済
対応済
(2023年12⽉1⽇〜2024年3⽉31⽇)
No. 医薬品名(一般名) 措置概要
措置国
アスピリン・カフェイン・ジヒドロコデイン酒石酸塩配合剤の米国添付
文書が改訂された。主な改訂内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項にオピオイド誘
発痛覚過敏、アロディニアを追記。
・Adverse Reactionsの項にオピオイドにて低血糖が報告されている
旨が追記。
ジヒドロコデインリン ・Boxed Warning、Pregnancyの項に、妊婦に対して長期投与すると
酸塩(1%以下)
新生児においてオピオイド離脱症候群があらわれるおそれがある旨
101 ジヒドロコデインリン を追記。
アメリカ
酸塩(1%以下)
その他、以下のとおり一部追記、変更がなされている。
鎮咳配合剤(1)
・Boxed Warningの項の中毒、乱用、誤用に関して、本剤を使用して
いるすべての患者の再評価必要性について追記。
・Boxed Warningの項の生命を脅かす呼吸抑制に関して、呼吸抑制
のリスクを減らすために、本剤の適切な投与量及び漸増が必要であ
ることが追記。
・Warnings and Precautionsのベンゾジアゼピン又は他の中枢神経
抑制剤との併用リスクについて、Boxed Warningの項へも追記。
102
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
【第1報】【第2報】
エルサルバ
パロキセチン塩酸塩
エルサルバドル規制当局は、白血球減少、歯ぎしり、顕微鏡的大腸 ドル、
その他
水和物
炎のリスクについて注意喚起するよう要請した。
パナマ
注目
米国添付文書が改訂された。主な改訂内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項に痛覚過敏、ア
ロディニアを追記。
・Adverse Reactionsの項にオピオイドにて低血糖が報告されている
旨が追記。
タペンタドール塩酸 その他、以下のとおり一部追記、変更がなされている。
103
アメリカ
塩
・Boxed Warningの項に、オピオイド嗜癖、乱用及び誤用のリスクが
あるため、投与前及び投与中は定期的に投与の必要性を評価する
こと、薬剤の適正な保管や廃棄を患者に指導することを追記。
・Warnings and Precautionsの項に投薬過誤のリスクに関して、同封
の目盛りシリンジを使用し、用量測定に家庭用スプーンやさじを使
用しないように指導する旨が追記。
その他
注目
米国FDAより、コデインリン酸塩・フェニレフリン塩酸塩・プロメタジン
プロメタジン塩酸塩 塩酸塩配合剤の米国添付文書について、以下の内容が改訂された
104 ヒベンズ酸プロメタジ もの。
アメリカ
ン
・Adverse reactionsの項に、オピオイド使用例における低血糖を追
記。
その他
注目
105 アロプリノール
シンガポール規制当局より、医療従事者向けにアロプリノールの処
方に関し情報提供がなされた。主な内容は以下のとおり。
・アロプリノール治療に対する患者の適合性を慎重に評価し、患者
のリスク因子を考慮する。
・可能な場合はリスク因子に対処し、アロプリノールを低用量で開始
し、徐々に増量することにより、SCAR(重度皮膚有害反応)発症のリ
スクを軽減するす。
シンガポー
情報提供
・腎機能障害や高齢など、アロプリノール誘発性 SCAR の既存のリ ル
スク因子を持つ患者に対して、特にリスクが高い患者を特定するた
め、HLA-B*5801遺伝子型解析を検討する。
・患者が適切な意思決定を行えるように、HLA-B*5801検査の利点
と費用について患者と話し合う。
・SCAR の初期の兆候や症状がないか患者を注意深くモニターす
る。
欧州にて、妊娠の可能性がある女性におけるバルプロ酸使用中止
後の治療戦略を調査するため非介入承認後安全性試験(PASS)が
実施され、報告書が公表された。慢性使用後のバルプロ酸中止が
半数の症例で維持された。バルプロ酸中止の成功に関連する要因
106 バルプロ酸ナトリウム
欧州連合
は、若年、病歴が短い、検査による患者管理が良好であること、投与
中止前の用量漸減、及び以前の特定薬剤継続使用歴であった。用
量漸減段階に伴う計画的妊娠がバルプロ酸中止成功の強力なプラ
ス要因であるとした。
20
その他
対応済
対応済