よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.4MB] (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
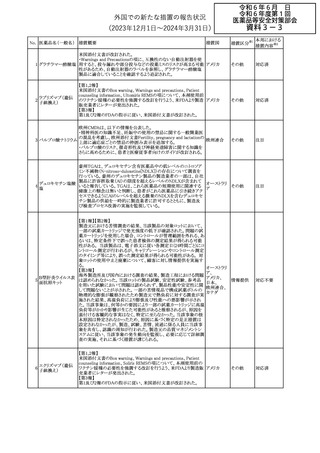
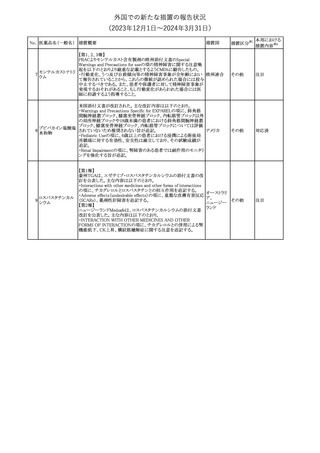
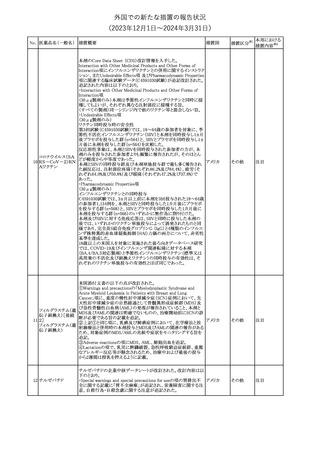
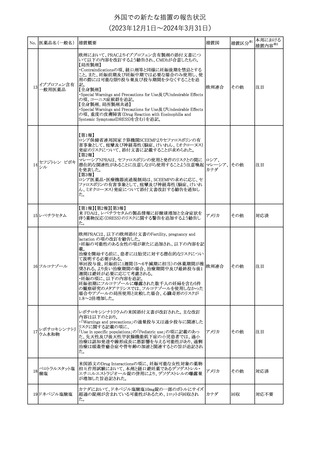
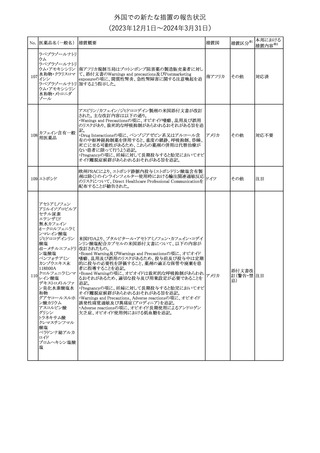
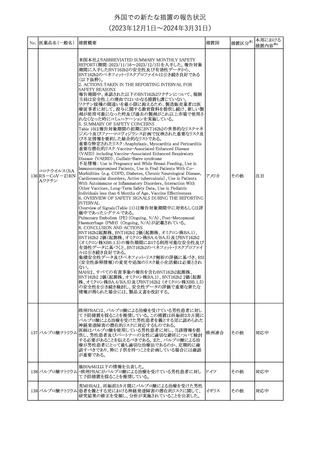
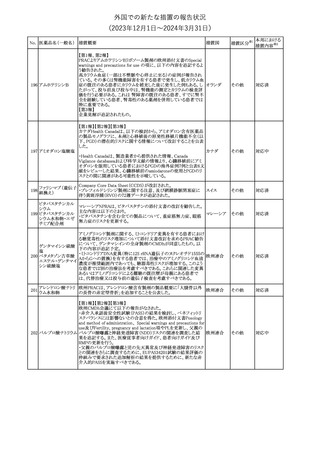
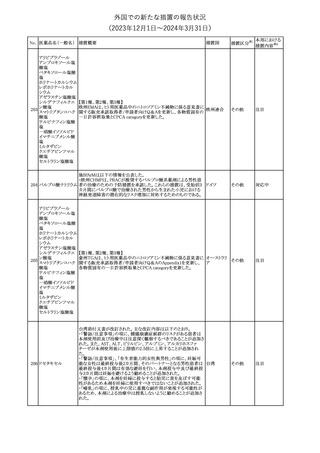
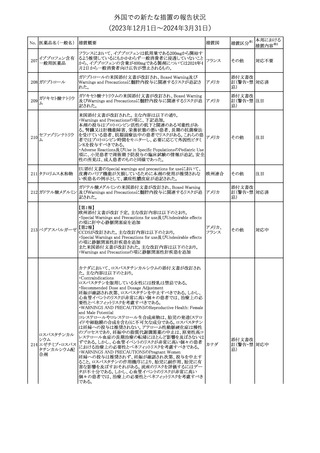
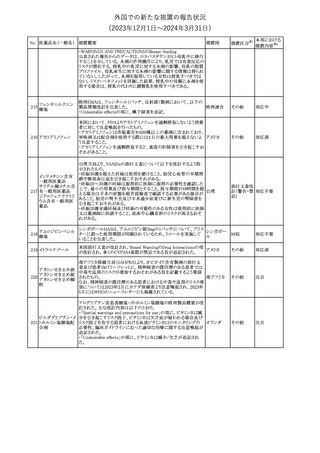
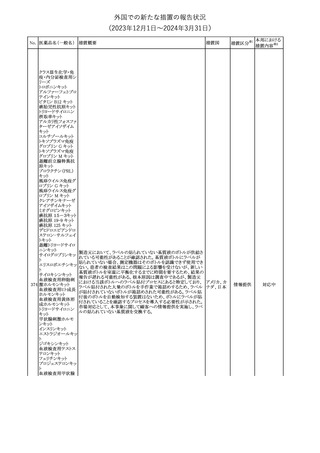
外国での新たな措置の報告状況
(2023年12⽉1⽇〜2024年3⽉31⽇)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
人全血液
人全血液(放射線照
射)
人赤血球液
人赤血球液(放射線
照射)
洗浄人赤血球液
洗浄人赤血球液(放
射線照射)
解凍人赤血球液
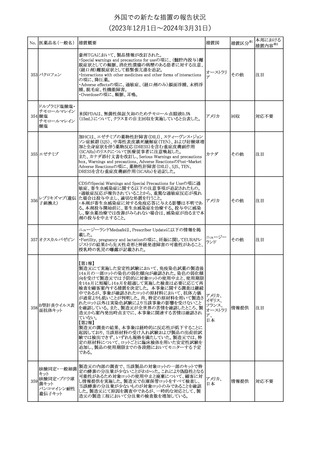
【第1報、第2報】
解凍人赤血球液(放
New Zealand Blood Service(NZBS)は、1980年から1996年期間中に
射線照射)
英国、フランス、アイルランド共和国で 「狂牛病」 が流行していた期
合成血
間に6か月以上在住していた人も2024年2月29日から、血液や血漿
合成血(放射線照
の供血予約を可能とした。
射)
ニュージー
235
NZBSはニュージーランドの供血者集団における変異型クロイツフェ
その他
新鮮凍結人血漿
ランド
ルト・ヤコブ病(vCJD)のリスクを調査し、リスクはごくわずかであり供
人血小板濃厚液
血制限を廃止してもニュージーランドにおける血液及び血液製剤の
人血小板濃厚液(放
安全性を損なうものではないことが示された。NZBSの制限廃止に関
射線照射)
わる勧告は、検討と詳細なリスク評価をもとにMedsafe(ニュージーラ
人血小板濃厚液HL
ンド保健省機関)に承認されているものであるとしている。
A
人血小板濃厚液HL
A(放射線照射)
人血小板濃厚液(放
射線照射)
人血小板濃厚液HL
A(放射線照射)
照射凍結赤血球-
LR「日赤」用時解凍
洗浄
パロノセトロン塩酸
塩
236
グラニセトロン塩酸
塩
本邦における
措置内容※2
注目
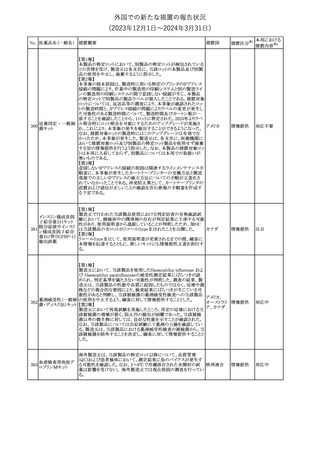
アポモルヒネの豪州製品情報について、アポモルヒネと5-HT3拮抗
剤の併用により重度の低血圧および意識消失のリスクがあることの
添付文書改
オーストラリ
報告に基づき、アポモルヒネの製品情報の禁忌及び他医薬品との
訂(警告・禁 注目
ア
相互作用の項において、制吐剤を含む5-HT3拮抗剤が併用禁忌薬
忌)
として追加された。
【第1報・第2報】
米国添付文書が改訂され、Adverse reactionsの項にClinical Trials
Experience in Pediatric Patientsとして、乳児(出生時に体重750グラ
ム未満の早産児)に対する侵襲性カンジダ感染症予防の臨床試験
フルコナゾール
237
で、本剤の予防投与を受けている乳児の腸管穿孔の発生率は、プ アメリカ
ホスフルコナゾール
ラセボ投与を受けている乳児と比較してより高かった旨、またECMO
使用している小児患者(生後1日~17歳)20名の臨床試験での本剤
の副作用プロファイルは、成人と非ECMO使用小児患者と類似して
いた旨が追記された。
その他
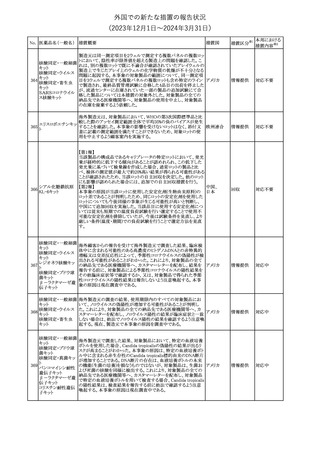
【第1報】
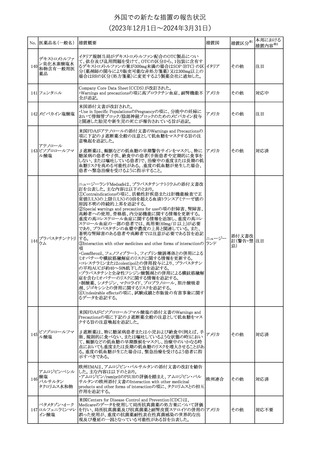
欧州PRACの勧告を踏まえ、韓国添付文書が改訂されることが旨の
情報を得た。改訂内容は以下のとおり。
インフリキシマブ(遺
オーストラリ
・Adverse Reactionsの項に体重増加が追記された。
238 伝子組換え)[後続
ア、
その他
【第2報】
1]
韓国
豪州TGAにおいて、添付文書が改訂された。改訂内容は以下のと
おり。
・Adverse effects (undesirableeffects)の項に体重増加を追記する。
注目
対応済
239
セファゾリンナトリウ
ム
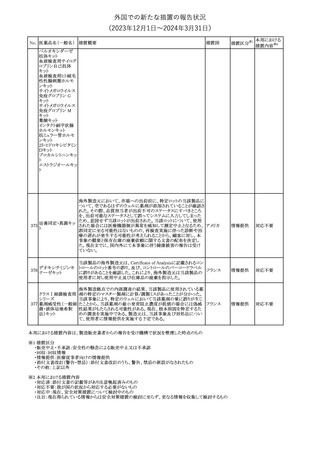
豪州添付文書が改訂された。Special warnings and precautions for
useの項に神経毒性の項が追記され、セファロスポリン治療に関連し オーストラリ
その他
た神経毒性の報告がある旨、神経毒性の症状には、脳症、痙攣、ミ ア
オクローヌスが含まれる旨、追記された。
注目
240
セフロキシム アキ
セチル
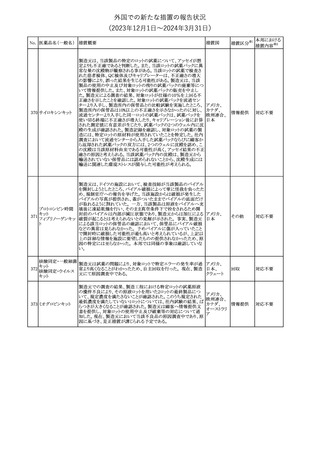
豪州添付文書が改訂された。Special warnings and precautions for
useの項に神経毒性の項が追記され、セファロスポリン治療に関連し オーストラリ
その他
た神経毒性の報告がある旨、神経毒性の症状には、脳症、痙攣、ミ ア
オクローヌスが含まれる旨、追記された。
注目
42
(2023年12⽉1⽇〜2024年3⽉31⽇)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
人全血液
人全血液(放射線照
射)
人赤血球液
人赤血球液(放射線
照射)
洗浄人赤血球液
洗浄人赤血球液(放
射線照射)
解凍人赤血球液
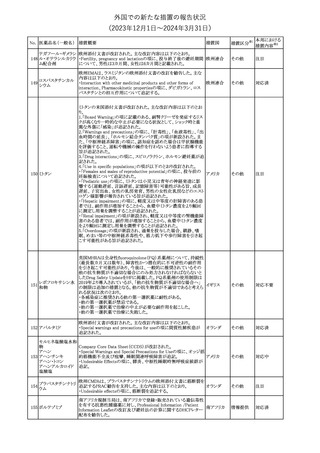
【第1報、第2報】
解凍人赤血球液(放
New Zealand Blood Service(NZBS)は、1980年から1996年期間中に
射線照射)
英国、フランス、アイルランド共和国で 「狂牛病」 が流行していた期
合成血
間に6か月以上在住していた人も2024年2月29日から、血液や血漿
合成血(放射線照
の供血予約を可能とした。
射)
ニュージー
235
NZBSはニュージーランドの供血者集団における変異型クロイツフェ
その他
新鮮凍結人血漿
ランド
ルト・ヤコブ病(vCJD)のリスクを調査し、リスクはごくわずかであり供
人血小板濃厚液
血制限を廃止してもニュージーランドにおける血液及び血液製剤の
人血小板濃厚液(放
安全性を損なうものではないことが示された。NZBSの制限廃止に関
射線照射)
わる勧告は、検討と詳細なリスク評価をもとにMedsafe(ニュージーラ
人血小板濃厚液HL
ンド保健省機関)に承認されているものであるとしている。
A
人血小板濃厚液HL
A(放射線照射)
人血小板濃厚液(放
射線照射)
人血小板濃厚液HL
A(放射線照射)
照射凍結赤血球-
LR「日赤」用時解凍
洗浄
パロノセトロン塩酸
塩
236
グラニセトロン塩酸
塩
本邦における
措置内容※2
注目
アポモルヒネの豪州製品情報について、アポモルヒネと5-HT3拮抗
剤の併用により重度の低血圧および意識消失のリスクがあることの
添付文書改
オーストラリ
報告に基づき、アポモルヒネの製品情報の禁忌及び他医薬品との
訂(警告・禁 注目
ア
相互作用の項において、制吐剤を含む5-HT3拮抗剤が併用禁忌薬
忌)
として追加された。
【第1報・第2報】
米国添付文書が改訂され、Adverse reactionsの項にClinical Trials
Experience in Pediatric Patientsとして、乳児(出生時に体重750グラ
ム未満の早産児)に対する侵襲性カンジダ感染症予防の臨床試験
フルコナゾール
237
で、本剤の予防投与を受けている乳児の腸管穿孔の発生率は、プ アメリカ
ホスフルコナゾール
ラセボ投与を受けている乳児と比較してより高かった旨、またECMO
使用している小児患者(生後1日~17歳)20名の臨床試験での本剤
の副作用プロファイルは、成人と非ECMO使用小児患者と類似して
いた旨が追記された。
その他
【第1報】
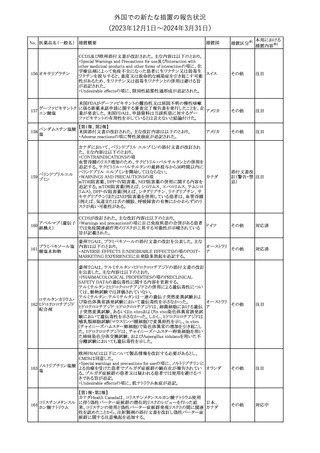
欧州PRACの勧告を踏まえ、韓国添付文書が改訂されることが旨の
情報を得た。改訂内容は以下のとおり。
インフリキシマブ(遺
オーストラリ
・Adverse Reactionsの項に体重増加が追記された。
238 伝子組換え)[後続
ア、
その他
【第2報】
1]
韓国
豪州TGAにおいて、添付文書が改訂された。改訂内容は以下のと
おり。
・Adverse effects (undesirableeffects)の項に体重増加を追記する。
注目
対応済
239
セファゾリンナトリウ
ム
豪州添付文書が改訂された。Special warnings and precautions for
useの項に神経毒性の項が追記され、セファロスポリン治療に関連し オーストラリ
その他
た神経毒性の報告がある旨、神経毒性の症状には、脳症、痙攣、ミ ア
オクローヌスが含まれる旨、追記された。
注目
240
セフロキシム アキ
セチル
豪州添付文書が改訂された。Special warnings and precautions for
useの項に神経毒性の項が追記され、セファロスポリン治療に関連し オーストラリ
その他
た神経毒性の報告がある旨、神経毒性の症状には、脳症、痙攣、ミ ア
オクローヌスが含まれる旨、追記された。
注目
42