よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
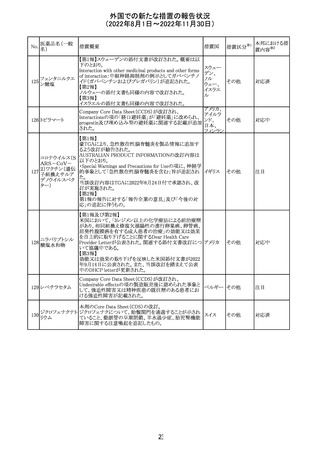
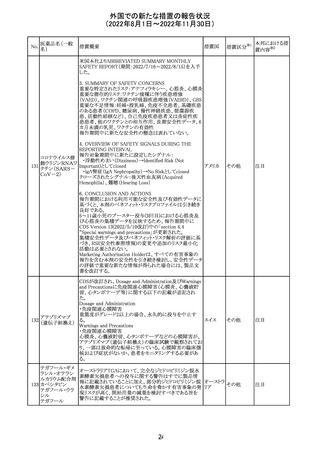
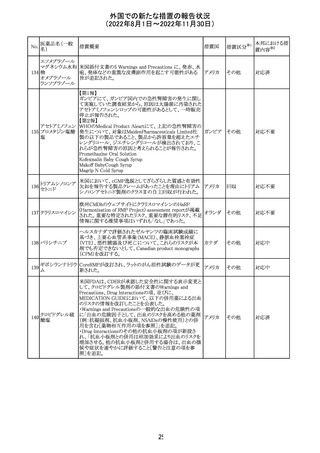
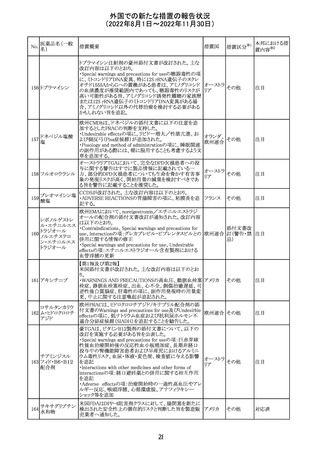
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
治験責任医師宛てに情報が発出された。HER2過剰発現の
進行又は転移性非小細胞肺癌患者を対象に、本剤、デュ
ルバルマブ(遺伝子組換え)及びプラチナ製剤を併用投与
トラスツズマブ
する臨床試験において、組入れ基準が以下のとおり変更に
51 デルクステカン
なった。
イギリス
(遺伝子組換え) ・スクリーニング時にクレアチニンクリアランスが60mL/min以
上(Cockcroft-Gault式による推定)であること
・本治験治療の開始までにプラチナ含有レジメンによる前
治療から6カ月以上が経過していること
措置区分※1
本邦における措
置内容※2
情報提供
対応不要
キザルチニブ塩
52
酸塩
治験薬概要書及び同意説明文書が改訂された。主な改訂
内容は以下のとおり。
アメリカ
・Other Safety Observations及びWarnings and Precautions
に、腫瘍崩壊症候群の発現の可能性が追記された。
その他
注目
53 プレガバリン
アイルランドHRPAはプレガバリンについて以下の情報提供
を行った。
・欧州において、治療の範囲内の用量においても、依存が
生じる可能性があり、薬物乱用の既往のある場合は注意喚
起が必要であると判断されていること。
・医療従事者は個々の患者の誤用、乱用、依存のリスクに
ついて注意深く評価を行う必要があること。
・中止による離脱症状は薬物依存が生じていることを示唆
アイルラ
する可能性があること。プレガバリンを中止する際には、使
ンド
用目的に関わらず、最低1週間以上をかけて徐々に行うこと
が推奨されること。
・オピオイドや他の中枢神経系抑制薬の使用がない場合
や、呼吸抑制のリスク因子の有無によらず、重度の呼吸抑
制の発現と関連していること。呼吸抑制のリスクが高い患者
(呼吸機能障害患者、呼吸器疾患または神経疾患患者、
腎障害患者、中枢神経抑制剤を併用している患者、高齢
者等)では用量の調整が必要かもしれないこと。
その他
対応中
54 フィナステリド
米国添付文書のAdverse Reactionsに以下が追記された。
・Clinical Trials Experienceの項に、性機能アンケートの結
果として、性的興味、勃起、性的問題の認識に関してプラ
セボが優越していたこと、性生活全般の満足度に関して統 アメリカ
計学的に優位な差はなかったことが追記された。
・Postmarketing Experienceの項に自殺念慮及び自殺行為
が追記された。
その他
注目
55 ボリコナゾール
【第1報】
欧州添付文書において、Special warnings and precautions
for useの項の皮膚扁平上皮癌が報告されている旨、
Undesirable effectsの項の皮膚扁平上皮癌に、その例とし
て括弧書きで上皮内有棘細胞癌及びボーエン病が追加さ
れた。
アメリカ、
その他
欧州連合
【第2報】
米国添付文書において、Warnings and Precautionsの項の
皮膚扁平上皮癌が報告されている旨、Adverse reactionsの
項の皮膚扁平上皮癌に、その例として括弧書きで、上皮内
有棘細胞癌及びボーエン病が追加された。
注目
11
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
治験責任医師宛てに情報が発出された。HER2過剰発現の
進行又は転移性非小細胞肺癌患者を対象に、本剤、デュ
ルバルマブ(遺伝子組換え)及びプラチナ製剤を併用投与
トラスツズマブ
する臨床試験において、組入れ基準が以下のとおり変更に
51 デルクステカン
なった。
イギリス
(遺伝子組換え) ・スクリーニング時にクレアチニンクリアランスが60mL/min以
上(Cockcroft-Gault式による推定)であること
・本治験治療の開始までにプラチナ含有レジメンによる前
治療から6カ月以上が経過していること
措置区分※1
本邦における措
置内容※2
情報提供
対応不要
キザルチニブ塩
52
酸塩
治験薬概要書及び同意説明文書が改訂された。主な改訂
内容は以下のとおり。
アメリカ
・Other Safety Observations及びWarnings and Precautions
に、腫瘍崩壊症候群の発現の可能性が追記された。
その他
注目
53 プレガバリン
アイルランドHRPAはプレガバリンについて以下の情報提供
を行った。
・欧州において、治療の範囲内の用量においても、依存が
生じる可能性があり、薬物乱用の既往のある場合は注意喚
起が必要であると判断されていること。
・医療従事者は個々の患者の誤用、乱用、依存のリスクに
ついて注意深く評価を行う必要があること。
・中止による離脱症状は薬物依存が生じていることを示唆
アイルラ
する可能性があること。プレガバリンを中止する際には、使
ンド
用目的に関わらず、最低1週間以上をかけて徐々に行うこと
が推奨されること。
・オピオイドや他の中枢神経系抑制薬の使用がない場合
や、呼吸抑制のリスク因子の有無によらず、重度の呼吸抑
制の発現と関連していること。呼吸抑制のリスクが高い患者
(呼吸機能障害患者、呼吸器疾患または神経疾患患者、
腎障害患者、中枢神経抑制剤を併用している患者、高齢
者等)では用量の調整が必要かもしれないこと。
その他
対応中
54 フィナステリド
米国添付文書のAdverse Reactionsに以下が追記された。
・Clinical Trials Experienceの項に、性機能アンケートの結
果として、性的興味、勃起、性的問題の認識に関してプラ
セボが優越していたこと、性生活全般の満足度に関して統 アメリカ
計学的に優位な差はなかったことが追記された。
・Postmarketing Experienceの項に自殺念慮及び自殺行為
が追記された。
その他
注目
55 ボリコナゾール
【第1報】
欧州添付文書において、Special warnings and precautions
for useの項の皮膚扁平上皮癌が報告されている旨、
Undesirable effectsの項の皮膚扁平上皮癌に、その例とし
て括弧書きで上皮内有棘細胞癌及びボーエン病が追加さ
れた。
アメリカ、
その他
欧州連合
【第2報】
米国添付文書において、Warnings and Precautionsの項の
皮膚扁平上皮癌が報告されている旨、Adverse reactionsの
項の皮膚扁平上皮癌に、その例として括弧書きで、上皮内
有棘細胞癌及びボーエン病が追加された。
注目
11