よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
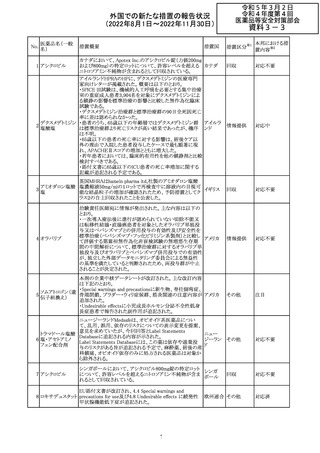
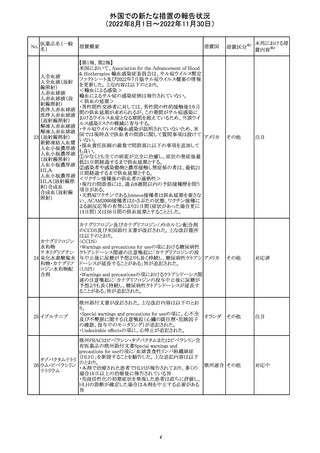
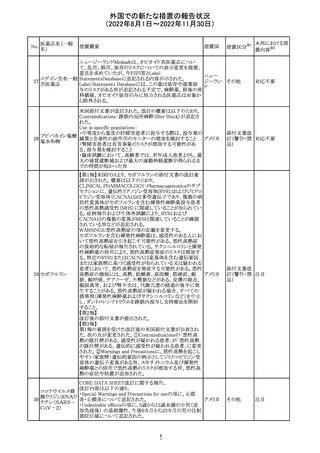
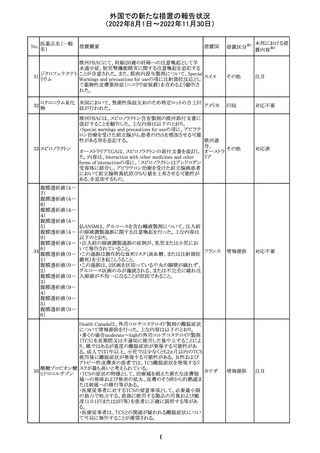
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置区分※1
本邦における措
置内容※2
情報提供
対応済
その他
注目
その他
対応中
ニュージーランドmedsafeはPrescriber updateに、好酸球増
ニュー
加と全身症状を伴う薬物反応(DRESS)に関して発現頻度
ジーラン その他
が高いとされる薬剤や有害事象低減のための漸増して投
ド
与することの重要性について記載した。
対応済
措置概要
措置国
米国FDAは、本剤の処方者が薬物相互作用について評価
するためのガイダンスとなる”PAXLOVID Patient Eligibility
Screening Checklist Tool for Prescribers”の更新版を公表
している。
当該ガイダンスには、患者の既往歴、合併症、併用薬の
ニルマトレルビ
112
チェックリストに加え、現時点でファクトシートやチェックリスト アメリカ
ル・リトナビル
に記載されていない薬剤を服用している患者の薬物相互
作用の可能性を評価する必要があるとして、追加のリソース
として、米国添付文書の検索サイト、薬物相互作用をチェッ
クできるサイト、NIH COVID-19治療ガイドラインのリンク先
などが記載されている。
カナダ保健省のHPに、イブルチニブの重篤かつ致死的な
不整脈又は心不全のリスクに対する消費者及び医療関係
者への注意喚起が記載された。
消費者に対しては、不整脈の症状(例:動悸、ふらつき、め
まい、息切れ、胸部不快感、失神)又は心不全の症状(例:
息切れ、横になっているときの呼吸困難、足、足首又は脚
の腫脹、脱力/疲労)が認められた場合は、医療従事者に
連絡することが注意喚起された。
医療関係者に対しては、以下の点が注意喚起された。
113 イブルチニブ
カナダ
・イブルチニブの投与を開始する前に患者の心機能を臨床
的に評価し、心臓の既往歴を考慮すること。
・投与中は患者の心機能低下の臨床徴候を注意深く観察
し、適切に管理すること。不整脈症状(例:動悸、頭部ふら
ふら感)が発現した患者又は呼吸困難が新たに発現した患
者については、さらなる評価(例:心電図、心エコー)を検討
する。
・不整脈又は心不全が新たに発現又は悪化した患者につ
いては、新たな用量調節ガイドラインに従う。
CORE SAFETY INFORMATIONが改訂された。概要は以
下のとおり。
SPECIAL WARNINGS AND SPECIAL PRECAUTIONS
デクスメデトミジン FOR USE:24時間を超えるデクスメデトミジンの使用は、通
114
アメリカ
塩酸塩
常治療に比べて、63.7歳以下の重症成人ICU患者の死亡
率の上昇と関連がある旨が追記された。
CLINICAL STUDIES:集中治療評価におけるSPICE III試
験の試験結果が追記された。
ラモトリギン
115
アロプリノール
アダパレン
米国添付文書が改訂され、contraindications とwarnings
116 アダパレン・過酸 and precautionsに、有効成分及び賦形剤に対する、アナ アメリカ
化ベンゾイル
フィラキシーを含む過敏症に関連した注意が追記された。
添付文書改
訂(警告・禁 注目
忌)
米国添付文書が改訂された。主な改訂箇所は下記のとお
り。
・Warnings and Precautionsの項に甲状腺機能低下症の小
児患者において、治療不足による認知発達及び線形成長
への悪影響を及ぼす可能性がある旨、並びに治療過剰が
頭蓋骨癒合及び骨年齢の加速と関連している旨が記載さ
れた。
レボチロキシンナ ・Adverse reactionsの項に小児における有害事象として偽
117
アメリカ
トリウム水和物
小脳炎、大腿骨頭すべり症が追記された。また、治療過剰
により頭骨未閉鎖の乳児患者では頭蓋骨癒合症が、成長
期の小児では骨端の早期閉鎖が起こる旨が追記された。
・Pediatric Useの項に小児の適応(原発性(甲状腺)、二次
性(下垂体)、三次性(視床下部)先天性または後天性甲状
腺機能低下症における補充療法、及び甲状腺ホルモン依
存性の高分化型甲状腺癌の治療における手術及び放射
性ヨウ素治療の補助療法)が記載された。
その他
21
注目
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置区分※1
本邦における措
置内容※2
情報提供
対応済
その他
注目
その他
対応中
ニュージーランドmedsafeはPrescriber updateに、好酸球増
ニュー
加と全身症状を伴う薬物反応(DRESS)に関して発現頻度
ジーラン その他
が高いとされる薬剤や有害事象低減のための漸増して投
ド
与することの重要性について記載した。
対応済
措置概要
措置国
米国FDAは、本剤の処方者が薬物相互作用について評価
するためのガイダンスとなる”PAXLOVID Patient Eligibility
Screening Checklist Tool for Prescribers”の更新版を公表
している。
当該ガイダンスには、患者の既往歴、合併症、併用薬の
ニルマトレルビ
112
チェックリストに加え、現時点でファクトシートやチェックリスト アメリカ
ル・リトナビル
に記載されていない薬剤を服用している患者の薬物相互
作用の可能性を評価する必要があるとして、追加のリソース
として、米国添付文書の検索サイト、薬物相互作用をチェッ
クできるサイト、NIH COVID-19治療ガイドラインのリンク先
などが記載されている。
カナダ保健省のHPに、イブルチニブの重篤かつ致死的な
不整脈又は心不全のリスクに対する消費者及び医療関係
者への注意喚起が記載された。
消費者に対しては、不整脈の症状(例:動悸、ふらつき、め
まい、息切れ、胸部不快感、失神)又は心不全の症状(例:
息切れ、横になっているときの呼吸困難、足、足首又は脚
の腫脹、脱力/疲労)が認められた場合は、医療従事者に
連絡することが注意喚起された。
医療関係者に対しては、以下の点が注意喚起された。
113 イブルチニブ
カナダ
・イブルチニブの投与を開始する前に患者の心機能を臨床
的に評価し、心臓の既往歴を考慮すること。
・投与中は患者の心機能低下の臨床徴候を注意深く観察
し、適切に管理すること。不整脈症状(例:動悸、頭部ふら
ふら感)が発現した患者又は呼吸困難が新たに発現した患
者については、さらなる評価(例:心電図、心エコー)を検討
する。
・不整脈又は心不全が新たに発現又は悪化した患者につ
いては、新たな用量調節ガイドラインに従う。
CORE SAFETY INFORMATIONが改訂された。概要は以
下のとおり。
SPECIAL WARNINGS AND SPECIAL PRECAUTIONS
デクスメデトミジン FOR USE:24時間を超えるデクスメデトミジンの使用は、通
114
アメリカ
塩酸塩
常治療に比べて、63.7歳以下の重症成人ICU患者の死亡
率の上昇と関連がある旨が追記された。
CLINICAL STUDIES:集中治療評価におけるSPICE III試
験の試験結果が追記された。
ラモトリギン
115
アロプリノール
アダパレン
米国添付文書が改訂され、contraindications とwarnings
116 アダパレン・過酸 and precautionsに、有効成分及び賦形剤に対する、アナ アメリカ
化ベンゾイル
フィラキシーを含む過敏症に関連した注意が追記された。
添付文書改
訂(警告・禁 注目
忌)
米国添付文書が改訂された。主な改訂箇所は下記のとお
り。
・Warnings and Precautionsの項に甲状腺機能低下症の小
児患者において、治療不足による認知発達及び線形成長
への悪影響を及ぼす可能性がある旨、並びに治療過剰が
頭蓋骨癒合及び骨年齢の加速と関連している旨が記載さ
れた。
レボチロキシンナ ・Adverse reactionsの項に小児における有害事象として偽
117
アメリカ
トリウム水和物
小脳炎、大腿骨頭すべり症が追記された。また、治療過剰
により頭骨未閉鎖の乳児患者では頭蓋骨癒合症が、成長
期の小児では骨端の早期閉鎖が起こる旨が追記された。
・Pediatric Useの項に小児の適応(原発性(甲状腺)、二次
性(下垂体)、三次性(視床下部)先天性または後天性甲状
腺機能低下症における補充療法、及び甲状腺ホルモン依
存性の高分化型甲状腺癌の治療における手術及び放射
性ヨウ素治療の補助療法)が記載された。
その他
21
注目