よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
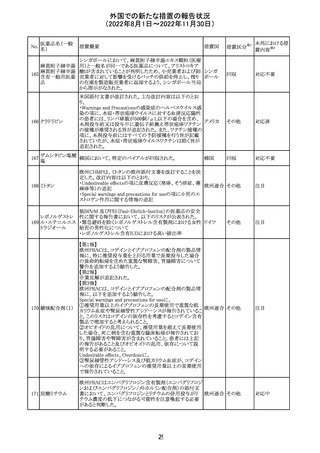
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
【第1報】
mRNA-1273二価ワクチンのシグナル検出結果をもとに、医
療専門家に本剤の過少投与リスクを通知し、医療専門家向
けに教育ツールを開発することなどを決定した。
2022年9月以降、mRNA-1273二価ワクチンの投与に関し
て、製品表示の混乱により誤って過少投与となるケースが
多数報告され、品質苦情、規制当局、自発報告、医療専門
家からの問い合わせなど、様々な情報源から報告を受けて
いる。グローバル安全性データベースの分析により、「製品
表示の混乱」と「過少投与」を基本語(PT)とする報告が一価
ワクチンよりも二価ワクチンで多いことが明らかになった。ほ
とんどの報告は、識別可能な患者はおらず、実際の投与量
に関して処方者が混乱したものの有害事象は発生しなかっ
たケースや、処方者が0.5mLの代わりに0.25mLを投与し、
被接種者の投与量不足につながったケースであった。考え
られる根本的な原因を調査した結果、過少投与につながる
製品表示の混乱を潜在的なリスク(重要ではない)と考えて
いる。「Dear Healthcare Professional Communications」の
配布、医療専門家向け教育ツールの開発、ウェブサイトで
の教育情報の提供など、リスク最小化策を追加で提案して
いる。
【第2報】
本邦におけるmRNA-1273二価ワクチン(起源株/オミクロン
株 BA.4-5)の承認を受け、新規成分mRNA-1273.222に関
する追加報告を行ったもの。
【第3報】
mRNA-1273二価ワクチン(起源株/オミクロン株)において
コロナウイルス修
「製品表示の混乱」及び「過少投与」がシグナル検出された
飾ウリジンRNAワ
アメリカ、
213
問題について、dosing communication letter(以下、レターと
その他
クチン(SARS-
スペイン
表記)の配布を決定し、欧州EMAより承認を得た旨の報告。
CoV-2)
承認されたレターの概要は以下。
<二価ブースターワクチンの正しい接種用量について>
<対BA.1単回接種用バイアルのラベルに関する注意喚起>
mRNA-1273二価ワクチンにおいて、0.5mLではなく0.25mL
を接種するという過少投与が発生した主な原因について、
先に承認されたmRNA-1273一価ワクチンの接種量が
0.25mLであったために接種量の混乱を招いた可能性があ
ると考えている。
・EMAにより承認されたmRNA-1273二価ワクチン(起源株/
オミクロン株BA.1)は、12歳以上の接種者に対して0.5mLが
正しい接種用量である。(バイアルからシリンジへの充填時
の目盛りを0.5mLとして図示)
<二価ワクチン 起源株/オミクロン株BA.1– 単回接種用バ
イアル>
・一部の承認国で使用されているmRNA-1273二価ワクチン
(起源株/オミクロン株 BA.1) の単回接種用バイアルのラ
ベルに不適切な表示問題があることを確認した。二価ワク
チンである本剤のラベルには「エラソメラン」のみが記載され
ていた。
・0.5mL単回接種と記載された本剤バイアルは、「エラソメラ
ン」と「イムエラソメラン」からなる二価のワクチンである。
・本剤の用途はブースター接種のみである。
<疑わしい副反応の報告>
医療関係者は、副反応が疑われた場合には規定の報告シ
ステムを通じて報告をおこなうこと。名前、住所、ファックス
番号、ウェブサイトアドレスなどを含む詳細も報告すること。
バッチ/ロット番号がある場合はそれらも報告すること。
214 テイコプラニン
英国において、200mg静注製剤の2バッチについて、細菌
性エンドトキシンの存在が確認されたとして、自主回収され イギリス
ている。
36
回収
本邦における措
置内容※2
注目
対応不要
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
【第1報】
mRNA-1273二価ワクチンのシグナル検出結果をもとに、医
療専門家に本剤の過少投与リスクを通知し、医療専門家向
けに教育ツールを開発することなどを決定した。
2022年9月以降、mRNA-1273二価ワクチンの投与に関し
て、製品表示の混乱により誤って過少投与となるケースが
多数報告され、品質苦情、規制当局、自発報告、医療専門
家からの問い合わせなど、様々な情報源から報告を受けて
いる。グローバル安全性データベースの分析により、「製品
表示の混乱」と「過少投与」を基本語(PT)とする報告が一価
ワクチンよりも二価ワクチンで多いことが明らかになった。ほ
とんどの報告は、識別可能な患者はおらず、実際の投与量
に関して処方者が混乱したものの有害事象は発生しなかっ
たケースや、処方者が0.5mLの代わりに0.25mLを投与し、
被接種者の投与量不足につながったケースであった。考え
られる根本的な原因を調査した結果、過少投与につながる
製品表示の混乱を潜在的なリスク(重要ではない)と考えて
いる。「Dear Healthcare Professional Communications」の
配布、医療専門家向け教育ツールの開発、ウェブサイトで
の教育情報の提供など、リスク最小化策を追加で提案して
いる。
【第2報】
本邦におけるmRNA-1273二価ワクチン(起源株/オミクロン
株 BA.4-5)の承認を受け、新規成分mRNA-1273.222に関
する追加報告を行ったもの。
【第3報】
mRNA-1273二価ワクチン(起源株/オミクロン株)において
コロナウイルス修
「製品表示の混乱」及び「過少投与」がシグナル検出された
飾ウリジンRNAワ
アメリカ、
213
問題について、dosing communication letter(以下、レターと
その他
クチン(SARS-
スペイン
表記)の配布を決定し、欧州EMAより承認を得た旨の報告。
CoV-2)
承認されたレターの概要は以下。
<二価ブースターワクチンの正しい接種用量について>
<対BA.1単回接種用バイアルのラベルに関する注意喚起>
mRNA-1273二価ワクチンにおいて、0.5mLではなく0.25mL
を接種するという過少投与が発生した主な原因について、
先に承認されたmRNA-1273一価ワクチンの接種量が
0.25mLであったために接種量の混乱を招いた可能性があ
ると考えている。
・EMAにより承認されたmRNA-1273二価ワクチン(起源株/
オミクロン株BA.1)は、12歳以上の接種者に対して0.5mLが
正しい接種用量である。(バイアルからシリンジへの充填時
の目盛りを0.5mLとして図示)
<二価ワクチン 起源株/オミクロン株BA.1– 単回接種用バ
イアル>
・一部の承認国で使用されているmRNA-1273二価ワクチン
(起源株/オミクロン株 BA.1) の単回接種用バイアルのラ
ベルに不適切な表示問題があることを確認した。二価ワク
チンである本剤のラベルには「エラソメラン」のみが記載され
ていた。
・0.5mL単回接種と記載された本剤バイアルは、「エラソメラ
ン」と「イムエラソメラン」からなる二価のワクチンである。
・本剤の用途はブースター接種のみである。
<疑わしい副反応の報告>
医療関係者は、副反応が疑われた場合には規定の報告シ
ステムを通じて報告をおこなうこと。名前、住所、ファックス
番号、ウェブサイトアドレスなどを含む詳細も報告すること。
バッチ/ロット番号がある場合はそれらも報告すること。
214 テイコプラニン
英国において、200mg静注製剤の2バッチについて、細菌
性エンドトキシンの存在が確認されたとして、自主回収され イギリス
ている。
36
回収
本邦における措
置内容※2
注目
対応不要