よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (49 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
措置区分※1
本邦における措
置内容※2
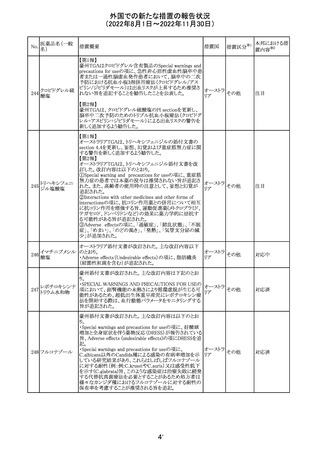
スイスにおいて、コデイン含有製品の製品情報に副作用と
コデインリン酸塩 して「胆管出口括約筋の緊張亢進」の記載があること、禁忌
294 水和物(1%以
として「内臓手術後の使用」が記載されているため、Codein スイス
下)
Knoll の製品情報にも同様の内容を追記するよう推奨され
たもの。
その他
注目
アムロジピンベシ
ル酸塩
カンデサルタン
295
シレキセチル・ア
ムロジピンベシル
酸塩配合剤
カナダHealth Canadaは、アムロジピンベシル酸/テルミサル
タン配合剤の製品情報を改訂し、降圧剤の服用によるめま
カナダ
い、失神、立ちくらみ等が現れることがあるため服用後は運
転や機械操作をさせないよう注意喚起した。
その他
対応済
296 メサラジン
EU添付文書のwarnings and precaution for use に、次亜塩
素酸ナトリウム系漂白剤との接触による赤褐色の尿の変色
欧州連合 その他
及び好酸球増多および全身症状を伴う薬物反応(DRESS)
のリスクに関する記載が追記された。
対応中
No.
医薬品名(一般
名)
措置概要
措置国
中国NMPAより、中国添付文書の改訂に関する公告が発表
された。主な改訂内容は下記のとおり。
・【不良反応】(副作用)の項に市販後の報告として末梢性
浮腫、関節痛、背痛、大腿骨骨幹部の非定型骨折、めま
い、不眠症、胸痛、胸部不快感、呼吸困難、急性喘息の増
悪、 動悸、過敏反応、食欲減退、血尿、頻尿、腎障害、脱
アレンドロン酸ナ
297
毛、ブドウ膜炎、強膜炎または上強膜炎、外耳道の真珠腫 中国
トリウム水和物
(限局性骨壊死)が追記された。
・【注意事項】の項に、顎骨壊死のリスク及び非定形大腿骨
骨幹部骨折のリスクが追記された。
・【薬物相互作用】の項に、10mg/dayを超えるアレンドロン
酸とアスピリンとの併用により上部消化管障害の発生率が
増加した旨が記載された。
その他
注目
その他
対応不要
アラブ首長国連邦のBurjeel Medical City Hospitalでデファ
イテリオ(defibrotide)の偽造品の可能性のある製品が見つ
かったことから、製造販売元のJazz Pharmaceuticals社は、
UAE規制当局を通じてEMAをはじめとする規制当局に注
意報告を行ったもの。
デファイテリオはUAEでは承認されておらず、販社である
Biologix FZ Co.(以下Biologix社)を通じて登録された患者
にのみ供給されている(Named Patient Program)製品とされ
ていたが、Biologix社は該当のBatch No.の製品を供給して
いなかった。Burjeel Medical City Hospitalは、他の経路を
通じて製品の供給を受けたことが確認された。
298
デフィブロチドナ
アラブ
トリウム
製造元において以下が確認されている。
・Batch Number: 19G19A は、デファイテリオに割り振られ
た番号ではない。
・Serial Number:344780048603とBatch Number:19G19Aと
の組み合わせの記録はない。
・Batch Numbwer:19G19AはEUの拠点には存在しない。
・有効期限06/2023年は間違っている。製品の有効期間が
36ヶ月であるため、2019年後半に製造されたロットは、遅く
とも2022年12月に有効期限が切れる。
・Burjeel Medical City Hospitalから提供された写真から、改
ざん防止装置は、本物の製品に使用されているものと異な
る。
49
(2022年8月1日~2022年11月30日)
措置区分※1
本邦における措
置内容※2
スイスにおいて、コデイン含有製品の製品情報に副作用と
コデインリン酸塩 して「胆管出口括約筋の緊張亢進」の記載があること、禁忌
294 水和物(1%以
として「内臓手術後の使用」が記載されているため、Codein スイス
下)
Knoll の製品情報にも同様の内容を追記するよう推奨され
たもの。
その他
注目
アムロジピンベシ
ル酸塩
カンデサルタン
295
シレキセチル・ア
ムロジピンベシル
酸塩配合剤
カナダHealth Canadaは、アムロジピンベシル酸/テルミサル
タン配合剤の製品情報を改訂し、降圧剤の服用によるめま
カナダ
い、失神、立ちくらみ等が現れることがあるため服用後は運
転や機械操作をさせないよう注意喚起した。
その他
対応済
296 メサラジン
EU添付文書のwarnings and precaution for use に、次亜塩
素酸ナトリウム系漂白剤との接触による赤褐色の尿の変色
欧州連合 その他
及び好酸球増多および全身症状を伴う薬物反応(DRESS)
のリスクに関する記載が追記された。
対応中
No.
医薬品名(一般
名)
措置概要
措置国
中国NMPAより、中国添付文書の改訂に関する公告が発表
された。主な改訂内容は下記のとおり。
・【不良反応】(副作用)の項に市販後の報告として末梢性
浮腫、関節痛、背痛、大腿骨骨幹部の非定型骨折、めま
い、不眠症、胸痛、胸部不快感、呼吸困難、急性喘息の増
悪、 動悸、過敏反応、食欲減退、血尿、頻尿、腎障害、脱
アレンドロン酸ナ
297
毛、ブドウ膜炎、強膜炎または上強膜炎、外耳道の真珠腫 中国
トリウム水和物
(限局性骨壊死)が追記された。
・【注意事項】の項に、顎骨壊死のリスク及び非定形大腿骨
骨幹部骨折のリスクが追記された。
・【薬物相互作用】の項に、10mg/dayを超えるアレンドロン
酸とアスピリンとの併用により上部消化管障害の発生率が
増加した旨が記載された。
その他
注目
その他
対応不要
アラブ首長国連邦のBurjeel Medical City Hospitalでデファ
イテリオ(defibrotide)の偽造品の可能性のある製品が見つ
かったことから、製造販売元のJazz Pharmaceuticals社は、
UAE規制当局を通じてEMAをはじめとする規制当局に注
意報告を行ったもの。
デファイテリオはUAEでは承認されておらず、販社である
Biologix FZ Co.(以下Biologix社)を通じて登録された患者
にのみ供給されている(Named Patient Program)製品とされ
ていたが、Biologix社は該当のBatch No.の製品を供給して
いなかった。Burjeel Medical City Hospitalは、他の経路を
通じて製品の供給を受けたことが確認された。
298
デフィブロチドナ
アラブ
トリウム
製造元において以下が確認されている。
・Batch Number: 19G19A は、デファイテリオに割り振られ
た番号ではない。
・Serial Number:344780048603とBatch Number:19G19Aと
の組み合わせの記録はない。
・Batch Numbwer:19G19AはEUの拠点には存在しない。
・有効期限06/2023年は間違っている。製品の有効期間が
36ヶ月であるため、2019年後半に製造されたロットは、遅く
とも2022年12月に有効期限が切れる。
・Burjeel Medical City Hospitalから提供された写真から、改
ざん防止装置は、本物の製品に使用されているものと異な
る。
49