よむ、つかう、まなぶ。
資料No.1-1~1-5_第十八改正日本薬局方第二追補(案) (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00008.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和5年度第1回 1/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第十八改正日本薬局方第二追補
1
医薬品各条
改正事項
アリピプラゾール
43
0.2の類縁物質A及び約0.8の類縁物質Bのピーク面積は自動
44
積分法で求めた面積にそれぞれ感度係数0.7を乗じた値とす
45
る.
46
溶解液:水/アセトニトリル/メタノール/酢酸(100)混
47
2
医薬品各条の部
L-アラニンの条の次に次の一条を加える.
3
アリピプラゾール
4
Aripiprazole
48
6
C23H27Cl2N3O2:448.39
7
7-{4-[4-(2,3-Dichlorophenyl)piperazin-1-yl]butoxy}-3,4-
8
dihydroquinolin-2(1H)-one
9
[129722-12-9]
11
12
13
14
15
試験条件
49
検出器,カラム,カラム温度,移動相及び流量は定量法
50
52
10
液(60:30:10:1)
の試験条件を準用する.
51
5
面積測定範囲:溶媒のピークの後から注入後25分まで
システム適合性
53
システムの性能は定量法のシステム適合性を準用する.
54
検出の確認:試料溶液1 mLに溶解液を加えて20 mLと
55
する.この液2 mLに溶解液を加えて20 mLとし,シ
56
ステム適合性試験用溶液とする.システム適合性試験
57
用溶液2 mLを正確に量り,溶解液を加えて正確に20
58
mLとする.この液20 μLから得たアリピプラゾール
59
のピーク面積が,システム適合性試験用溶液のアリピ
60
プラゾールのピーク面積の7 ~ 13%になることを確
61
認する.
62
本品を乾燥したものは定量するとき,アリピプラゾール
(C23H27Cl2N3O2) 98.0 ~ 102.0%を含む.
性状 本品は白色の結晶又は結晶性の粉末である.
本品はジクロロメタンに溶けやすく,水,アセトニトリル,
メタノール又はエタノール(99.5)にほとんど溶けない.
本品は結晶多形が認められる.
16
確認試験
17
(1)
18
吸光度測定法〈2.24〉 により吸収スペクトルを測定し,本品
19
のスペクトルと本品の参照スペクトル又はアリピプラゾール
20
標準品について同様に操作して得られたスペクトルを比較す
21
るとき,両者のスペクトルは同一波長のところに同様の強度
本品のメタノール溶液(1→50000)につき,紫外可視
22
の吸収を認める.
23
(2)
24
化カリウム錠剤法により試験を行い,本品のスペクトルと本
25
26
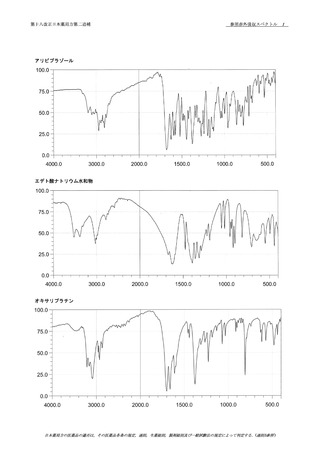
本品につき,赤外吸収スペクトル測定法〈2.25〉 の臭
1 .
システムの再現性:標準溶液20 μLにつき,上記の条件
63
で試験を6回繰り返すとき,アリピプラゾールのピー
64
ク面積の相対標準偏差は2.0%以下である.
65
乾燥減量〈2.41〉 0.1%以下(1 g,105℃,3時間).
66
強熱残分〈2.44〉 0.1%以下(1 g).
67
定量法
本操作は遮光した容器を用いて行う.本品及びアリピ
68
プラゾール標準品を乾燥し,その約50 mgずつを精密に量り,
69
それぞれ溶解液に溶かし,正確に50 mLとする.これらの液
70
5 mLずつを正確に量り,それぞれ溶解液を加えて正確に50
71
mLとし,試料溶液及び標準溶液とする.試料溶液及び標準
72
溶液20 μLずつを正確にとり,次の条件で液体クロマトグラ
73
フィー 〈2.01〉 により試験を行い,それぞれの液のアリピプ
74
ラゾールのピーク面積AT及びASを測定する.
75
アリピプラゾール(C23H27Cl2N3O2)の量(mg)=MS × AT/AS
76
MS:アリピプラゾール標準品の秤取量(mg)
品の参照スペクトル又はアリピプラゾール標準品のスペクト
77
溶解液:水/アセトニトリル/メタノール/酢酸(100)混
ルを比較するとき,両者のスペクトルは同一波数のところに
78
27
同様の強度の吸収を認める.もし,これらのスペクトルに差
79
28
を認めるときは,本品及びアリピプラゾール標準品をそれぞ
80
検出器:紫外吸光光度計(測定波長:254 nm)
29
れジクロロメタンに溶かした後,ジクロロメタンを蒸発し,
81
カラム:内径4.6 mm,長さ10 cmのステンレス管に3
残留物につき,同様の試験を行う.
82
μmの液体クロマトグラフィー用オクタデシルシリル
30
31
本操作は遮光した容器を用いて行う.定
83
化シリカゲルを充塡する.
量法で得た試料溶液を試料溶液とする.試料溶液1 mLを正
84
カラム温度:25℃付近の一定温度
33
確に量り,溶解液を加えて正確に100 mLとする.この液5
85
移動相A:薄めたトリフルオロ酢酸(1→2000)/液体ク
34
mLを正確に量り,溶解液を加えて正確に50 mLとし,標準
86
35
溶液とする.試料溶液及び標準溶液20 μLずつを正確にとり,
87
36
次の条件で液体クロマトグラフィー〈2.01〉 により試験を行
88
37
う.それぞれの液の各々のピーク面積を自動積分法により測
89
38
定するとき,試料溶液のアリピプラゾール以外のピーク面積
90
39
は,標準溶液のアリピプラゾールのピーク面積より大きくな
40
く,試料溶液のアリピプラゾール以外のピークの合計面積は,
41
標準溶液のアリピプラゾールのピーク面積の3倍より大きく
42
ない.ただし,アリピプラゾールに対する相対保持時間約
32
純度試験
類縁物質
液(60:30:10:1)
試験条件
ロマトグラフィー用アセトニトリル混液(9:1)
移動相B:液体クロマトグラフィー用アセトニトリル/
薄めたトリフルオロ酢酸(1→2000)混液(9:1)
移動相の送液:移動相A及び移動相Bの混合比を次のよ
うに変えて濃度勾配制御する.
注入後の時間
(分)
0~ 2
2 ~ 10
10 ~ 20
移動相A
(vol%)
80
80 → 65
65 → 10
移動相B
(vol%)
20
20 → 35
35 → 90
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する.(通則5参照 )
1
医薬品各条
改正事項
アリピプラゾール
43
0.2の類縁物質A及び約0.8の類縁物質Bのピーク面積は自動
44
積分法で求めた面積にそれぞれ感度係数0.7を乗じた値とす
45
る.
46
溶解液:水/アセトニトリル/メタノール/酢酸(100)混
47
2
医薬品各条の部
L-アラニンの条の次に次の一条を加える.
3
アリピプラゾール
4
Aripiprazole
48
6
C23H27Cl2N3O2:448.39
7
7-{4-[4-(2,3-Dichlorophenyl)piperazin-1-yl]butoxy}-3,4-
8
dihydroquinolin-2(1H)-one
9
[129722-12-9]
11
12
13
14
15
試験条件
49
検出器,カラム,カラム温度,移動相及び流量は定量法
50
52
10
液(60:30:10:1)
の試験条件を準用する.
51
5
面積測定範囲:溶媒のピークの後から注入後25分まで
システム適合性
53
システムの性能は定量法のシステム適合性を準用する.
54
検出の確認:試料溶液1 mLに溶解液を加えて20 mLと
55
する.この液2 mLに溶解液を加えて20 mLとし,シ
56
ステム適合性試験用溶液とする.システム適合性試験
57
用溶液2 mLを正確に量り,溶解液を加えて正確に20
58
mLとする.この液20 μLから得たアリピプラゾール
59
のピーク面積が,システム適合性試験用溶液のアリピ
60
プラゾールのピーク面積の7 ~ 13%になることを確
61
認する.
62
本品を乾燥したものは定量するとき,アリピプラゾール
(C23H27Cl2N3O2) 98.0 ~ 102.0%を含む.
性状 本品は白色の結晶又は結晶性の粉末である.
本品はジクロロメタンに溶けやすく,水,アセトニトリル,
メタノール又はエタノール(99.5)にほとんど溶けない.
本品は結晶多形が認められる.
16
確認試験
17
(1)
18
吸光度測定法〈2.24〉 により吸収スペクトルを測定し,本品
19
のスペクトルと本品の参照スペクトル又はアリピプラゾール
20
標準品について同様に操作して得られたスペクトルを比較す
21
るとき,両者のスペクトルは同一波長のところに同様の強度
本品のメタノール溶液(1→50000)につき,紫外可視
22
の吸収を認める.
23
(2)
24
化カリウム錠剤法により試験を行い,本品のスペクトルと本
25
26
本品につき,赤外吸収スペクトル測定法〈2.25〉 の臭
1 .
システムの再現性:標準溶液20 μLにつき,上記の条件
63
で試験を6回繰り返すとき,アリピプラゾールのピー
64
ク面積の相対標準偏差は2.0%以下である.
65
乾燥減量〈2.41〉 0.1%以下(1 g,105℃,3時間).
66
強熱残分〈2.44〉 0.1%以下(1 g).
67
定量法
本操作は遮光した容器を用いて行う.本品及びアリピ
68
プラゾール標準品を乾燥し,その約50 mgずつを精密に量り,
69
それぞれ溶解液に溶かし,正確に50 mLとする.これらの液
70
5 mLずつを正確に量り,それぞれ溶解液を加えて正確に50
71
mLとし,試料溶液及び標準溶液とする.試料溶液及び標準
72
溶液20 μLずつを正確にとり,次の条件で液体クロマトグラ
73
フィー 〈2.01〉 により試験を行い,それぞれの液のアリピプ
74
ラゾールのピーク面積AT及びASを測定する.
75
アリピプラゾール(C23H27Cl2N3O2)の量(mg)=MS × AT/AS
76
MS:アリピプラゾール標準品の秤取量(mg)
品の参照スペクトル又はアリピプラゾール標準品のスペクト
77
溶解液:水/アセトニトリル/メタノール/酢酸(100)混
ルを比較するとき,両者のスペクトルは同一波数のところに
78
27
同様の強度の吸収を認める.もし,これらのスペクトルに差
79
28
を認めるときは,本品及びアリピプラゾール標準品をそれぞ
80
検出器:紫外吸光光度計(測定波長:254 nm)
29
れジクロロメタンに溶かした後,ジクロロメタンを蒸発し,
81
カラム:内径4.6 mm,長さ10 cmのステンレス管に3
残留物につき,同様の試験を行う.
82
μmの液体クロマトグラフィー用オクタデシルシリル
30
31
本操作は遮光した容器を用いて行う.定
83
化シリカゲルを充塡する.
量法で得た試料溶液を試料溶液とする.試料溶液1 mLを正
84
カラム温度:25℃付近の一定温度
33
確に量り,溶解液を加えて正確に100 mLとする.この液5
85
移動相A:薄めたトリフルオロ酢酸(1→2000)/液体ク
34
mLを正確に量り,溶解液を加えて正確に50 mLとし,標準
86
35
溶液とする.試料溶液及び標準溶液20 μLずつを正確にとり,
87
36
次の条件で液体クロマトグラフィー〈2.01〉 により試験を行
88
37
う.それぞれの液の各々のピーク面積を自動積分法により測
89
38
定するとき,試料溶液のアリピプラゾール以外のピーク面積
90
39
は,標準溶液のアリピプラゾールのピーク面積より大きくな
40
く,試料溶液のアリピプラゾール以外のピークの合計面積は,
41
標準溶液のアリピプラゾールのピーク面積の3倍より大きく
42
ない.ただし,アリピプラゾールに対する相対保持時間約
32
純度試験
類縁物質
液(60:30:10:1)
試験条件
ロマトグラフィー用アセトニトリル混液(9:1)
移動相B:液体クロマトグラフィー用アセトニトリル/
薄めたトリフルオロ酢酸(1→2000)混液(9:1)
移動相の送液:移動相A及び移動相Bの混合比を次のよ
うに変えて濃度勾配制御する.
注入後の時間
(分)
0~ 2
2 ~ 10
10 ~ 20
移動相A
(vol%)
80
80 → 65
65 → 10
移動相B
(vol%)
20
20 → 35
35 → 90
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する.(通則5参照 )