よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
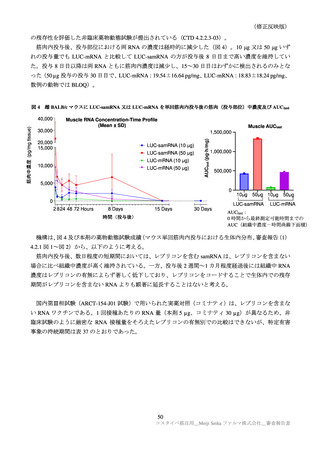
4.R.1 本剤の非臨床薬物動態について
申請者は、本剤の自己増幅とその制御及び非臨床薬物動態について、以下のように説明した。
mRNA-2105 のレプリコンは VEEV に由来する。VEEV では構造タンパク質をコードする配列を、
mRNA-2105 では S タンパク質をコードする配列に置換している。そのため、本剤投与で感染性ウイル
ス粒子は産生されず、また逆転写酵素を欠くため、宿主細胞 DNA に mRNA-2105 の配列が挿入されるこ
とはない。本剤は mRNA-2105 を LNP 製剤化したものであり、筋肉内投与後、主に投与部位の筋細胞及
び抗原提示細胞(樹状細胞など)にエンドサイトーシスにより取り込まれると予想される(Vaccines
(Basel) 2019; 7(4): 122、Vaccines (Basel) 2021; 9(2):147 等)
。LNP から細胞質内に放出された mRNA-2105
は、VEEV レプリカーゼの複製機構により増幅し 19)、細胞内リボソームによって S タンパク質抗原が翻
訳される結果、期待される効果が得られると考える。細胞内で増幅した mRNA 及び翻訳タンパク質につ
いては、細胞内ヌクレアーゼ及び細胞内プロテアーゼによって分解・除去されると考えられる(Vaccines
(Basel) 2021;9(2):97)
。
通常、投与された mRNA は、生体内の核酸と同様に速やかに代謝されるが、LNP に封入することで
mRNA が代謝されることなく細胞内に取り込まれる。そのため、LNP に封入した mRNA の体内動態は、
封入される mRNA ではなく、主に LNP の組成や粒子の大きさに依存する(Mol Ther Nucleic Acids 2019;
15: 1-11、Nanomedicine (Lond) 2016; 11: 673-92)
。本剤及び ARCT-021 の成分は類似しており、LNP の組
成及び LNP:mRNA 比は同じであるため、ARCT-021 の成分の組織分布及び消失の結果(4.1 及び 4.2)
は、本剤に外挿可能であると考える。
代謝については、両ワクチンで新規のイオン化脂質である ATX-126 について実施し、結果は 4.3 のと
おりであった。
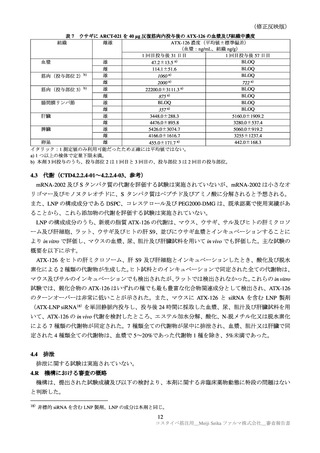
本剤の胎盤移行性については、ARCT-021 のウサギ受胎能、胚・胎児及び発生後の発生毒性試験
(CTD4.2.3.5.3-01)から考察した。mRNA-2002 は、10 µg 投与群の 20 検体中 1 検体の胎児の血漿(8.19
pg/mL)を除き、いずれの投与群においても胎盤及び胎児の組織で検出されなかった。また、ATX-126 は、
胎盤では 10 及び 20 µg 投与群で検出されたが(10 µg 投与群:275.0±33.9 ng/g、20 µg 投与群:387.6±
117.8 ng/g)、いずれの投与群においても胎児の血漿及び組織で検出されなかった。以上の結果から、
ARCT-021 は母動物から胎児へほとんど移行しないと考えられ、本剤も同様と考えられる。
機構は、以下のとおり考える。
主に ARCT-021 の試験成績から、本剤の分布・消失に係る薬物動態を説明することは許容可能であり、
申請者の説明及び提出された非臨床動態試験成績(4.1~4.3)から、本剤の薬物動態特性について一定の
把握は可能と判断する。従来の非自己増幅型 mRNA と比べると、自己増幅型 mRNA は生体内で長く維
持される可能性もあるが、mRNA について蓄積などの特段の懸念を示す結果は得られておらず、投与後
は時間経過に伴い生体内から消失していくことが示されている。S タンパク質は、マウス生体内分布試
験で主に投与部位の筋肉、リンパ節及び血漿で検出されており mRNA と分布域に相違はない。また、時
間経過とともに減少する傾向が示されていることから、最終的には残存しないと推察できる。なお、脂
質の ATX-126 については、半減期が長く、長期にわたって残存する可能性が高いものの、ウサギ反復投
19)細胞質に放出された mRNA-2105 からレプリカ―ゼ(RNA 依存性 RNA ポリメラーゼ含む)が発現し、そのレプリカ―
ゼにより mRNA-2105 に相補的なマイナス鎖 RNA が生じる。マイナス鎖 RNA からレプリカ―ゼにより mRNA-2105
が再び合成される際に、S タンパク質の mRNA も同時に合成される(J Gen Virol 2015;96(9):2483-2500、Gene Ther
2021;28(3-4):117-129)
。
13
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
4.R.1 本剤の非臨床薬物動態について
申請者は、本剤の自己増幅とその制御及び非臨床薬物動態について、以下のように説明した。
mRNA-2105 のレプリコンは VEEV に由来する。VEEV では構造タンパク質をコードする配列を、
mRNA-2105 では S タンパク質をコードする配列に置換している。そのため、本剤投与で感染性ウイル
ス粒子は産生されず、また逆転写酵素を欠くため、宿主細胞 DNA に mRNA-2105 の配列が挿入されるこ
とはない。本剤は mRNA-2105 を LNP 製剤化したものであり、筋肉内投与後、主に投与部位の筋細胞及
び抗原提示細胞(樹状細胞など)にエンドサイトーシスにより取り込まれると予想される(Vaccines
(Basel) 2019; 7(4): 122、Vaccines (Basel) 2021; 9(2):147 等)
。LNP から細胞質内に放出された mRNA-2105
は、VEEV レプリカーゼの複製機構により増幅し 19)、細胞内リボソームによって S タンパク質抗原が翻
訳される結果、期待される効果が得られると考える。細胞内で増幅した mRNA 及び翻訳タンパク質につ
いては、細胞内ヌクレアーゼ及び細胞内プロテアーゼによって分解・除去されると考えられる(Vaccines
(Basel) 2021;9(2):97)
。
通常、投与された mRNA は、生体内の核酸と同様に速やかに代謝されるが、LNP に封入することで
mRNA が代謝されることなく細胞内に取り込まれる。そのため、LNP に封入した mRNA の体内動態は、
封入される mRNA ではなく、主に LNP の組成や粒子の大きさに依存する(Mol Ther Nucleic Acids 2019;
15: 1-11、Nanomedicine (Lond) 2016; 11: 673-92)
。本剤及び ARCT-021 の成分は類似しており、LNP の組
成及び LNP:mRNA 比は同じであるため、ARCT-021 の成分の組織分布及び消失の結果(4.1 及び 4.2)
は、本剤に外挿可能であると考える。
代謝については、両ワクチンで新規のイオン化脂質である ATX-126 について実施し、結果は 4.3 のと
おりであった。
本剤の胎盤移行性については、ARCT-021 のウサギ受胎能、胚・胎児及び発生後の発生毒性試験
(CTD4.2.3.5.3-01)から考察した。mRNA-2002 は、10 µg 投与群の 20 検体中 1 検体の胎児の血漿(8.19
pg/mL)を除き、いずれの投与群においても胎盤及び胎児の組織で検出されなかった。また、ATX-126 は、
胎盤では 10 及び 20 µg 投与群で検出されたが(10 µg 投与群:275.0±33.9 ng/g、20 µg 投与群:387.6±
117.8 ng/g)、いずれの投与群においても胎児の血漿及び組織で検出されなかった。以上の結果から、
ARCT-021 は母動物から胎児へほとんど移行しないと考えられ、本剤も同様と考えられる。
機構は、以下のとおり考える。
主に ARCT-021 の試験成績から、本剤の分布・消失に係る薬物動態を説明することは許容可能であり、
申請者の説明及び提出された非臨床動態試験成績(4.1~4.3)から、本剤の薬物動態特性について一定の
把握は可能と判断する。従来の非自己増幅型 mRNA と比べると、自己増幅型 mRNA は生体内で長く維
持される可能性もあるが、mRNA について蓄積などの特段の懸念を示す結果は得られておらず、投与後
は時間経過に伴い生体内から消失していくことが示されている。S タンパク質は、マウス生体内分布試
験で主に投与部位の筋肉、リンパ節及び血漿で検出されており mRNA と分布域に相違はない。また、時
間経過とともに減少する傾向が示されていることから、最終的には残存しないと推察できる。なお、脂
質の ATX-126 については、半減期が長く、長期にわたって残存する可能性が高いものの、ウサギ反復投
19)細胞質に放出された mRNA-2105 からレプリカ―ゼ(RNA 依存性 RNA ポリメラーゼ含む)が発現し、そのレプリカ―
ゼにより mRNA-2105 に相補的なマイナス鎖 RNA が生じる。マイナス鎖 RNA からレプリカ―ゼにより mRNA-2105
が再び合成される際に、S タンパク質の mRNA も同時に合成される(J Gen Virol 2015;96(9):2483-2500、Gene Ther
2021;28(3-4):117-129)
。
13
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書