よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
プラセボ群 1/1953 例(0.1%)
、重篤な有害事象の本剤群 5/2103 例(0.2%)
、プラセボ群 3/1953 例(0.2%)
は治験薬との因果関係が否定されなかった。
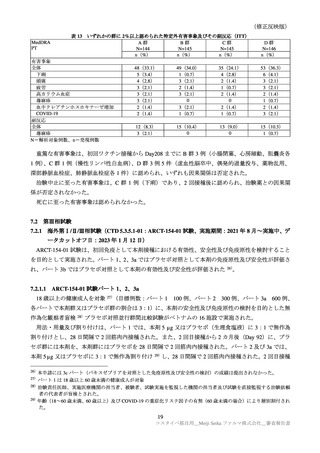
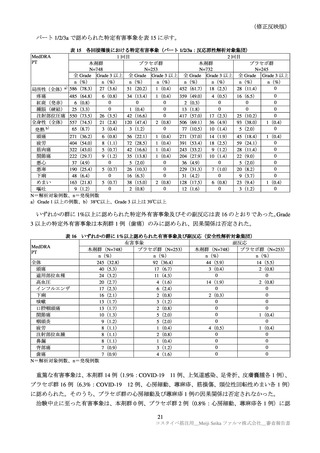
2)ARCT-154-J01 試験
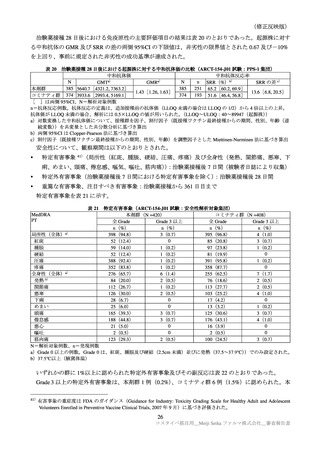
基礎疾患を有する被験者は、安全性解析対象集団の 111/828 例(13.4%)(本剤群 63/420 例(15.0%)
、
コミナティ群 48/408 例(11.8%)
)が該当した。疾患の内訳は、呼吸器疾患(本剤群 14 例、コミナティ
群 8 例)
、心疾患(本剤群 23 例、コミナティ群 21 例)、腎疾患(本剤群 2 例)、肝疾患(本剤群 19 例、
コミナティ群 6 例)
、糖尿病(本剤群 9 例、コミナティ群 12 例)、血液疾患(鉄欠乏性貧血は除く)(本
剤群 2 例、コミナティ群 1 例)
、悪性腫瘍(本剤群 2 例、コミナティ群 4 例)
、神経又は神経筋疾患(本
剤群 1 例)
、睡眠時無呼吸症候群(本剤群 1 例、コミナティ群 3 例)
、重度の精神疾患又は知的障害(本
剤群 1 例、コミナティ群 3 例)及び BMI 30 以上を満たす肥満(本剤群 1 例、コミナティ群 1 例)であ
った。
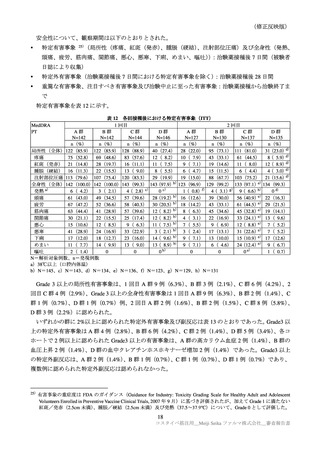
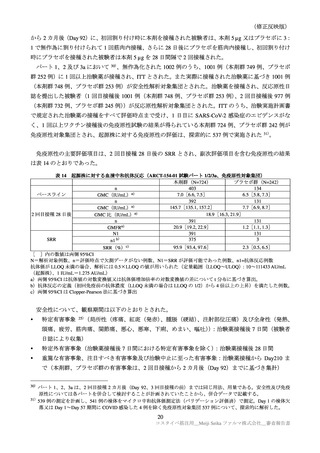
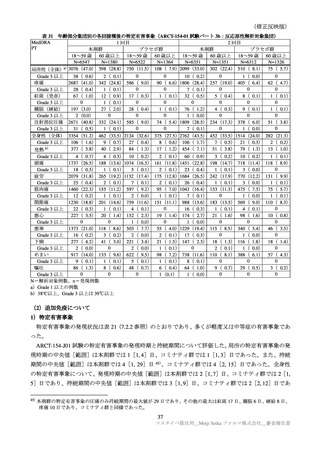
表 34
特定有害事象(ARCT-154-J01 試験:安全性解析対象集団のうち、基礎疾患を有する被験者)
本剤群(N =63)
コミナティ群(N =48)
全 Grade
Grade 3 以上
全 Grade
Grade 3 以上
n(%)
n(%)
n(%)
n(%)
0
59(93.7)
48(100.0)
1(2.1)
局所性(全体)a)
MedDRA
PT
紅斑
腫脹
硬結
圧痛
疼痛
全身性(全体)a)
7(11.1)
3(4.8)
2(3.2)
57(90.5)
52(82.5)
40(63.5)
0
0
0
0
0
1(1.6)
12(25.0)
13(27.1)
13(27.1)
48(100.0)
44(91.7)
32(66.7)
1(2.1)
1(2.1)
0
0
0
2(4.2)
7(11.1)
1(1.6)
9(18.8)
1(2.1)
発熱 b)
0
0
関節痛
22(34.9)
12(25.0)
0
0
悪寒
15(23.8)
12(25.0)
0
0
下痢
6(9.5)
2(4.2)
0
0
めまい
2(3.2)
1(2.1)
0
0
頭痛
21(33.3)
10(20.8)
0
0
倦怠感
27(42.9)
18(37.5)
0
0
悪心
6(9.5)
2(4.2)
0
0
0
嘔吐
2(3.2)
0
筋肉痛
23(36.5)
10(20.8)
1(2.1)
N=解析対象例数、n=発現例数
a)Grade 0 以上の例数。Grade 0 は、紅斑、腫脹及び硬結(2.5cm 未満)並びに発熱(37.5~37.9℃)
)でのみ設定された。
b)37.5℃以上(腋窩体温)
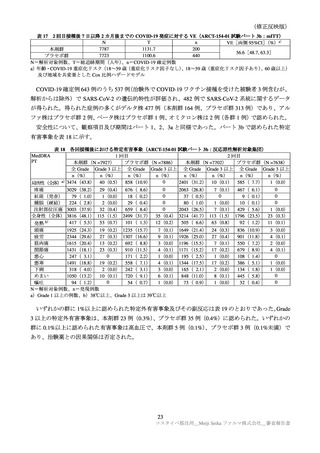
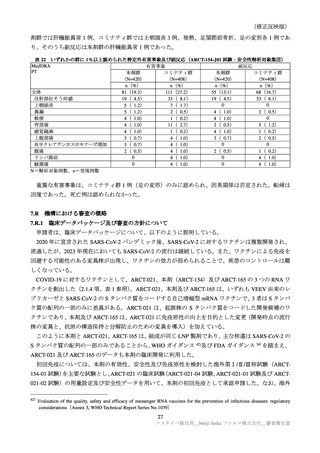
基礎疾患を有する被験者における特定外有害事象は、本剤群 11/63 例(17.5%)、コミナティ群 13/48 例
(27.1%)
、特定外副反応は本剤群 9/63 例(14.3%)
、コミナティ群 8/48 例(16.7%)であった。重篤な有
害事象及び死亡に至った有害事象は認められなかった。
ARCT-154-01 試験及び ARCT-154-J01 試験で基礎疾患の有無別の特定有害事象及び全ての有害事象の
発現割合は、個別の事象の発現割合を踏まえても基礎疾患の有無による安全性の明確な差異は認められ
なかった。これらの成績からは、基礎疾患のある者に対する本剤の接種で、有害事象の発現割合や重症
度が増加する懸念はないと考える。
しかしながら、
基礎疾患のある者への接種実績は限られていること、
「新型コロナウイルス感染症に係る臨時の予防接種実施要領」
(厚生労働省、令和 4 年 8 月 1 日版)で接
種要注意者にも該当することから、類薬と同様の注意喚起が必要と考える。
41
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
プラセボ群 1/1953 例(0.1%)
、重篤な有害事象の本剤群 5/2103 例(0.2%)
、プラセボ群 3/1953 例(0.2%)
は治験薬との因果関係が否定されなかった。
2)ARCT-154-J01 試験
基礎疾患を有する被験者は、安全性解析対象集団の 111/828 例(13.4%)(本剤群 63/420 例(15.0%)
、
コミナティ群 48/408 例(11.8%)
)が該当した。疾患の内訳は、呼吸器疾患(本剤群 14 例、コミナティ
群 8 例)
、心疾患(本剤群 23 例、コミナティ群 21 例)、腎疾患(本剤群 2 例)、肝疾患(本剤群 19 例、
コミナティ群 6 例)
、糖尿病(本剤群 9 例、コミナティ群 12 例)、血液疾患(鉄欠乏性貧血は除く)(本
剤群 2 例、コミナティ群 1 例)
、悪性腫瘍(本剤群 2 例、コミナティ群 4 例)
、神経又は神経筋疾患(本
剤群 1 例)
、睡眠時無呼吸症候群(本剤群 1 例、コミナティ群 3 例)
、重度の精神疾患又は知的障害(本
剤群 1 例、コミナティ群 3 例)及び BMI 30 以上を満たす肥満(本剤群 1 例、コミナティ群 1 例)であ
った。
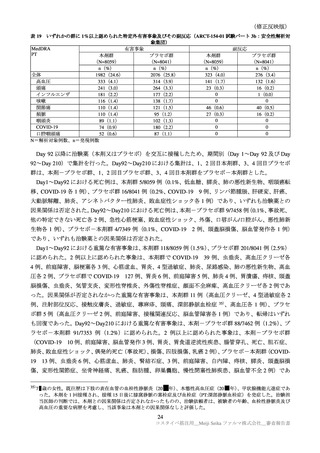
表 34
特定有害事象(ARCT-154-J01 試験:安全性解析対象集団のうち、基礎疾患を有する被験者)
本剤群(N =63)
コミナティ群(N =48)
全 Grade
Grade 3 以上
全 Grade
Grade 3 以上
n(%)
n(%)
n(%)
n(%)
0
59(93.7)
48(100.0)
1(2.1)
局所性(全体)a)
MedDRA
PT
紅斑
腫脹
硬結
圧痛
疼痛
全身性(全体)a)
7(11.1)
3(4.8)
2(3.2)
57(90.5)
52(82.5)
40(63.5)
0
0
0
0
0
1(1.6)
12(25.0)
13(27.1)
13(27.1)
48(100.0)
44(91.7)
32(66.7)
1(2.1)
1(2.1)
0
0
0
2(4.2)
7(11.1)
1(1.6)
9(18.8)
1(2.1)
発熱 b)
0
0
関節痛
22(34.9)
12(25.0)
0
0
悪寒
15(23.8)
12(25.0)
0
0
下痢
6(9.5)
2(4.2)
0
0
めまい
2(3.2)
1(2.1)
0
0
頭痛
21(33.3)
10(20.8)
0
0
倦怠感
27(42.9)
18(37.5)
0
0
悪心
6(9.5)
2(4.2)
0
0
0
嘔吐
2(3.2)
0
筋肉痛
23(36.5)
10(20.8)
1(2.1)
N=解析対象例数、n=発現例数
a)Grade 0 以上の例数。Grade 0 は、紅斑、腫脹及び硬結(2.5cm 未満)並びに発熱(37.5~37.9℃)
)でのみ設定された。
b)37.5℃以上(腋窩体温)
基礎疾患を有する被験者における特定外有害事象は、本剤群 11/63 例(17.5%)、コミナティ群 13/48 例
(27.1%)
、特定外副反応は本剤群 9/63 例(14.3%)
、コミナティ群 8/48 例(16.7%)であった。重篤な有
害事象及び死亡に至った有害事象は認められなかった。
ARCT-154-01 試験及び ARCT-154-J01 試験で基礎疾患の有無別の特定有害事象及び全ての有害事象の
発現割合は、個別の事象の発現割合を踏まえても基礎疾患の有無による安全性の明確な差異は認められ
なかった。これらの成績からは、基礎疾患のある者に対する本剤の接種で、有害事象の発現割合や重症
度が増加する懸念はないと考える。
しかしながら、
基礎疾患のある者への接種実績は限られていること、
「新型コロナウイルス感染症に係る臨時の予防接種実施要領」
(厚生労働省、令和 4 年 8 月 1 日版)で接
種要注意者にも該当することから、類薬と同様の注意喚起が必要と考える。
41
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書