よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
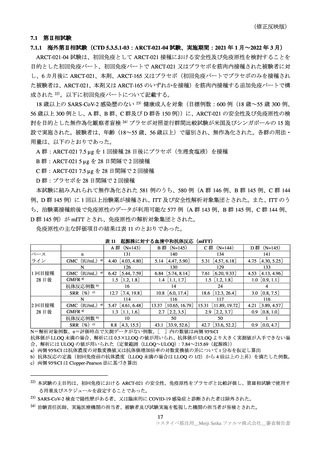
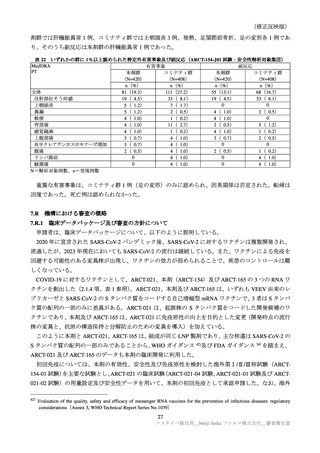
った。因果関係が否定されなかった重篤な有害事象は認められなかった。
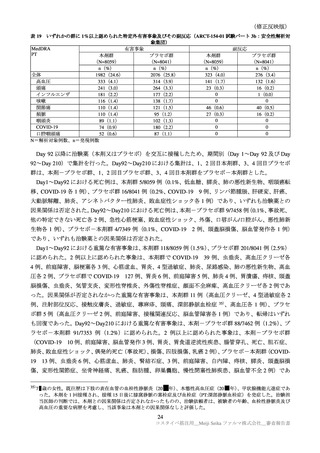
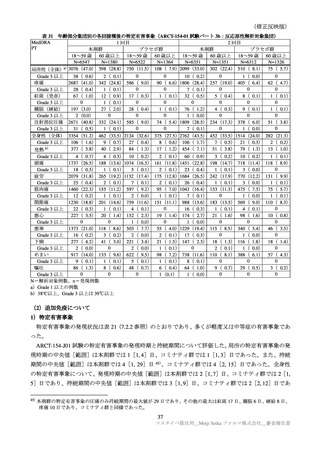
Day1~Day92 における治験中止に至った有害事象は、本剤群 14/8059 例(0.2%)
、プラセボ群 25/8041
例(0.3%)に認められた。2 例以上に認められた事象は、本剤群(頻脈、肺の悪性新生物各 2 例)、プラ
セボ群(COVID-19 9 例、上気道感染、高血圧各 2 例)であった。因果関係が否定されなかった治験中
止に至った事象は本剤群 2 例(4 型過敏症、蕁麻疹各 1 例)のみであった。Day92~Day210 における治
験中止に至った有害事象は、本剤群 16/7462 例(0.2%)、プラセボ群 10/7353 例(0.1%)に認められた。
2 例以上に認められた事象は、本剤-プラセボ群(高血圧 4 例、死亡、偶発的死亡各 2 例)
、プラセボ-
本剤群(高血圧 3 例、COVID-19、頻脈各 2 例)であった。因果関係が否定されなかった治験中止に至っ
た事象は本剤-プラセボ群 3 例(高血圧 2 例、頻脈 1 例)、プラセボ-本剤群(頻脈、アナフィラキシー
反応各 1 例)であり、転帰はプラセボ-本剤群の頻脈(未回復)を除き、回復であった。
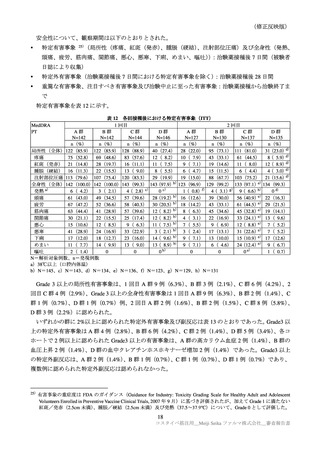
7.2.2 国内第Ⅲ相試験(CTD 5.3.5.1-04:ARCT-154-J01 試験、実施期間:2022 年 11 月~実施中、デー
タカットオフ日:2023 年 3 月 27 日)
SARS-CoV-2 ワクチン(コミナティ又はスパイクバックス、いずれも一価(起源株))を初回免疫とし
て 2 回接種し、追加免疫としてコミナティ(一価(起源株)、以下特記ない場合は同じ)を 3 カ月以上前
に接種した 18 歳以上の健康成人 36)(目標例数:780 例 37)(本剤群 390 例、コミナティ群 390 例)に、
本剤の安全性及び免疫原性の検討を目的とした無作為化観察者盲検 38)実薬対照並行群間比較試験が国
内 11 施設で実施された。
用法・用量は、本剤 5 µg 又はコミナティ 0.3 mL 39)を 1 回筋肉内接種とされた。
無作為化された 828 例 40)(本剤群 420 例、コミナティ群 408 例)全例に 1 回以上治験薬が接種され、
安全性解析対象集団とされた。このうち、SARS-CoV-2(起源株)に対する中和抗体価データがない被験
者を除いた本剤群 417 例、コミナティ群 408 例が FAS とされた。FAS のうち、治験薬接種前の SARSCoV-2 のヌクレオカプシドに対する抗体が陽性の被験者及び治験実施計画書からの重要な逸脱があった
被験者を除いた本剤群 385 例、コミナティ群 374 例が PPS-1、治験実施計画書からの重要な逸脱があっ
た被験者を除いた本剤群 413 例、コミナティ群 400 例が PPS-2 とされた。
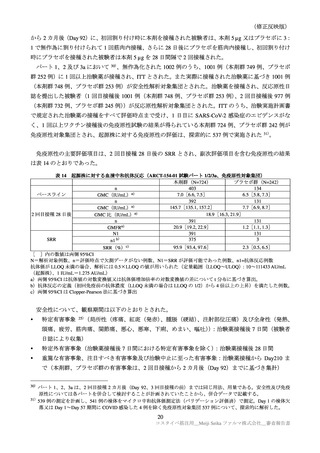
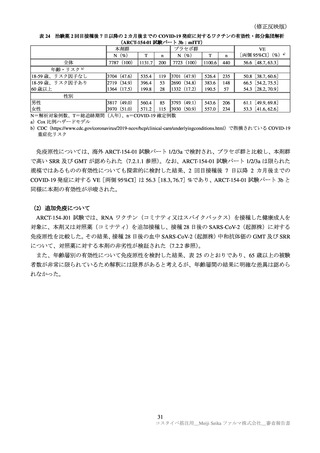
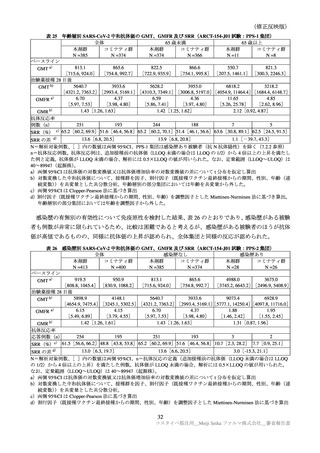
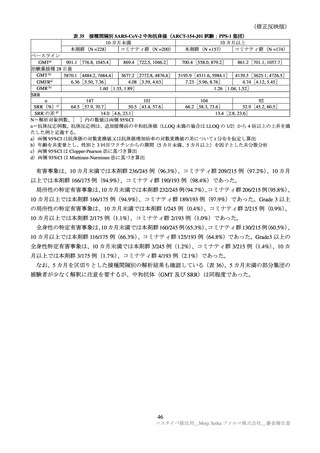
免疫原性の主要評価項目は、PPS-1 集団における治験薬接種 28 日後における起源株に対する中和抗体
の GMT 及び SRR(追加免疫前の中和抗体価(LLOQ 未満の場合は LLOQ の 1/2)から 4 倍以上上昇した
被験者の割合)とされ、各項目について本剤群のコミナティ群に対する非劣性が評価された。本剤群の
コミナティ群に対する、GMT 比(本剤群/コミナティ群)の非劣性マージンは 0.67、SRR の差の非劣性
マージンは-10%と設定された。
36)COVID-19 感染に関連した以下の患者は除外された。①スクリーニングの 1 日前から急性疾患や 37.5℃以上の発熱があ
った者、②スクリーニング時の SARS-CoV-2 抗原検査で陽性の者、③過去 4 カ月以内に SARS-CoV-2 に感染したこと
が明らかな者又は後遺症を伴う COVID-19 罹患歴のある者。
37)免疫原性について GMR を 1.0、中和抗体価の標準偏差を 0.400、各接種群の SRR をいずれも 85%と仮定。コミナティ
に対する本剤の GMT 及び SRR の非劣性(GMT の非劣性マージン=0.67、SRR の非劣性マージン=-10%、有意水準
=片側 2.5%)を 90%以上の確率で検証するためには、解析対象例数は 270 例/群が必要になる。割付症例の 10%程度
が脱落し、20%程度の被験者が接種前感染例として主要解析対象集団から除外されると仮定し、本試験における割付
症例を 780 例(390 例/群)と設定した。
38)治験責任医師、実施医療機関の担当者、被験者、試験実施を監視した機関の担当者及び治験依頼者が盲検とされた。
39)コミナティ 0.3 mL は、トジナメランの RNA 量として 30 µg。
40)既接種ワクチン最終接種からの期間(5 カ月未満/以上)
、性別、年齢(65 歳未満/以上)
、実施医療機関を層別因子
とした無作為化が実施された。
25
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
った。因果関係が否定されなかった重篤な有害事象は認められなかった。
Day1~Day92 における治験中止に至った有害事象は、本剤群 14/8059 例(0.2%)
、プラセボ群 25/8041
例(0.3%)に認められた。2 例以上に認められた事象は、本剤群(頻脈、肺の悪性新生物各 2 例)、プラ
セボ群(COVID-19 9 例、上気道感染、高血圧各 2 例)であった。因果関係が否定されなかった治験中
止に至った事象は本剤群 2 例(4 型過敏症、蕁麻疹各 1 例)のみであった。Day92~Day210 における治
験中止に至った有害事象は、本剤群 16/7462 例(0.2%)、プラセボ群 10/7353 例(0.1%)に認められた。
2 例以上に認められた事象は、本剤-プラセボ群(高血圧 4 例、死亡、偶発的死亡各 2 例)
、プラセボ-
本剤群(高血圧 3 例、COVID-19、頻脈各 2 例)であった。因果関係が否定されなかった治験中止に至っ
た事象は本剤-プラセボ群 3 例(高血圧 2 例、頻脈 1 例)、プラセボ-本剤群(頻脈、アナフィラキシー
反応各 1 例)であり、転帰はプラセボ-本剤群の頻脈(未回復)を除き、回復であった。
7.2.2 国内第Ⅲ相試験(CTD 5.3.5.1-04:ARCT-154-J01 試験、実施期間:2022 年 11 月~実施中、デー
タカットオフ日:2023 年 3 月 27 日)
SARS-CoV-2 ワクチン(コミナティ又はスパイクバックス、いずれも一価(起源株))を初回免疫とし
て 2 回接種し、追加免疫としてコミナティ(一価(起源株)、以下特記ない場合は同じ)を 3 カ月以上前
に接種した 18 歳以上の健康成人 36)(目標例数:780 例 37)(本剤群 390 例、コミナティ群 390 例)に、
本剤の安全性及び免疫原性の検討を目的とした無作為化観察者盲検 38)実薬対照並行群間比較試験が国
内 11 施設で実施された。
用法・用量は、本剤 5 µg 又はコミナティ 0.3 mL 39)を 1 回筋肉内接種とされた。
無作為化された 828 例 40)(本剤群 420 例、コミナティ群 408 例)全例に 1 回以上治験薬が接種され、
安全性解析対象集団とされた。このうち、SARS-CoV-2(起源株)に対する中和抗体価データがない被験
者を除いた本剤群 417 例、コミナティ群 408 例が FAS とされた。FAS のうち、治験薬接種前の SARSCoV-2 のヌクレオカプシドに対する抗体が陽性の被験者及び治験実施計画書からの重要な逸脱があった
被験者を除いた本剤群 385 例、コミナティ群 374 例が PPS-1、治験実施計画書からの重要な逸脱があっ
た被験者を除いた本剤群 413 例、コミナティ群 400 例が PPS-2 とされた。
免疫原性の主要評価項目は、PPS-1 集団における治験薬接種 28 日後における起源株に対する中和抗体
の GMT 及び SRR(追加免疫前の中和抗体価(LLOQ 未満の場合は LLOQ の 1/2)から 4 倍以上上昇した
被験者の割合)とされ、各項目について本剤群のコミナティ群に対する非劣性が評価された。本剤群の
コミナティ群に対する、GMT 比(本剤群/コミナティ群)の非劣性マージンは 0.67、SRR の差の非劣性
マージンは-10%と設定された。
36)COVID-19 感染に関連した以下の患者は除外された。①スクリーニングの 1 日前から急性疾患や 37.5℃以上の発熱があ
った者、②スクリーニング時の SARS-CoV-2 抗原検査で陽性の者、③過去 4 カ月以内に SARS-CoV-2 に感染したこと
が明らかな者又は後遺症を伴う COVID-19 罹患歴のある者。
37)免疫原性について GMR を 1.0、中和抗体価の標準偏差を 0.400、各接種群の SRR をいずれも 85%と仮定。コミナティ
に対する本剤の GMT 及び SRR の非劣性(GMT の非劣性マージン=0.67、SRR の非劣性マージン=-10%、有意水準
=片側 2.5%)を 90%以上の確率で検証するためには、解析対象例数は 270 例/群が必要になる。割付症例の 10%程度
が脱落し、20%程度の被験者が接種前感染例として主要解析対象集団から除外されると仮定し、本試験における割付
症例を 780 例(390 例/群)と設定した。
38)治験責任医師、実施医療機関の担当者、被験者、試験実施を監視した機関の担当者及び治験依頼者が盲検とされた。
39)コミナティ 0.3 mL は、トジナメランの RNA 量として 30 µg。
40)既接種ワクチン最終接種からの期間(5 カ月未満/以上)
、性別、年齢(65 歳未満/以上)
、実施医療機関を層別因子
とした無作為化が実施された。
25
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書