よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (54 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
審査報告(2)
令和 5 年 11 月 8 日
申請品目
[販 売 名] コスタイベ筋注用
[一 般 名] コロナウイルス(SARS-CoV-2)RNA ワクチン
[申 請 者] Meiji Seika ファルマ株式会社
[申請年月日] 令和 5 年 4 月 28 日
[略語等一覧]
別記のとおり。
1.
審査内容
専門協議及びその後の機構における審査の概略は、以下のとおりである。なお、本専門協議の専門委
員は、本品目についての専門委員からの申し出等に基づき、「医薬品医療機器総合機構における専門協
議等の実施に関する達」(平成 20 年 12 月 25 日付け
20 達第 8 号)の規定により、指名した。
専門協議では、審査報告(1)に記載した論点(「7.R.2 有効性について」、「7.R.4 臨床的位置付け
及び効能・効果について」及び「7.R.5 用法・用量について」)に関する機構の判断は専門委員から支
持された。
機構は、下記の点について追加で検討し、必要な対応を行った。
1.1 安全性について
審査報告(1)の「7.R.3 安全性について」に記載した機構の判断は専門委員から支持された。また、
専門委員から以下の意見が出された。
本剤は、レプリコンを含む RNA を有効成分とする医薬品として初めて実用化される品目である。
そのため、作用機序や、生体内で残存する可能性はないのか、被接種者及び医療従事者に丁寧に情
報提供することが望ましい。
レプリコンを含むことで、長期的な安全性への影響や、有効性の持続等、既承認薬に比べ臨床的な
特徴が出ているのか否か、説明が必要と考える。
機構は、情報提供資材等に本剤の作用機序や、レプリコンについての基礎的な説明も含めるよう申請
者に求め、申請者は了解した。
また、機構は、レプリコンの作用機序及び生体内での残存等について、提出された資料から以下を確
認した。
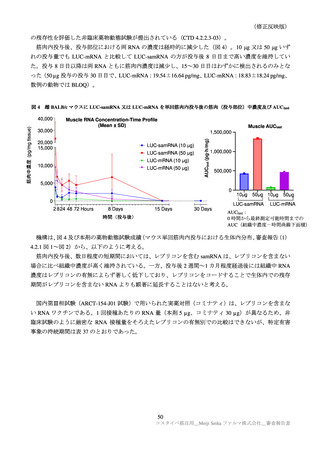
薬物動態の参考資料として、マウスに、レプリカーゼとルシフェラーゼをコードする mRNA(LUCsamRNA)及びルシフェラーゼのみをコードする mRNA(LUC-mRNA)を LNP 51)に封入して投与した際
51)使用された LNP は ARCT-021 及び ARCT-154 ワクチンで使用されたものと同様の LNP である。
49
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
審査報告(2)
令和 5 年 11 月 8 日
申請品目
[販 売 名] コスタイベ筋注用
[一 般 名] コロナウイルス(SARS-CoV-2)RNA ワクチン
[申 請 者] Meiji Seika ファルマ株式会社
[申請年月日] 令和 5 年 4 月 28 日
[略語等一覧]
別記のとおり。
1.
審査内容
専門協議及びその後の機構における審査の概略は、以下のとおりである。なお、本専門協議の専門委
員は、本品目についての専門委員からの申し出等に基づき、「医薬品医療機器総合機構における専門協
議等の実施に関する達」(平成 20 年 12 月 25 日付け
20 達第 8 号)の規定により、指名した。
専門協議では、審査報告(1)に記載した論点(「7.R.2 有効性について」、「7.R.4 臨床的位置付け
及び効能・効果について」及び「7.R.5 用法・用量について」)に関する機構の判断は専門委員から支
持された。
機構は、下記の点について追加で検討し、必要な対応を行った。
1.1 安全性について
審査報告(1)の「7.R.3 安全性について」に記載した機構の判断は専門委員から支持された。また、
専門委員から以下の意見が出された。
本剤は、レプリコンを含む RNA を有効成分とする医薬品として初めて実用化される品目である。
そのため、作用機序や、生体内で残存する可能性はないのか、被接種者及び医療従事者に丁寧に情
報提供することが望ましい。
レプリコンを含むことで、長期的な安全性への影響や、有効性の持続等、既承認薬に比べ臨床的な
特徴が出ているのか否か、説明が必要と考える。
機構は、情報提供資材等に本剤の作用機序や、レプリコンについての基礎的な説明も含めるよう申請
者に求め、申請者は了解した。
また、機構は、レプリコンの作用機序及び生体内での残存等について、提出された資料から以下を確
認した。
薬物動態の参考資料として、マウスに、レプリカーゼとルシフェラーゼをコードする mRNA(LUCsamRNA)及びルシフェラーゼのみをコードする mRNA(LUC-mRNA)を LNP 51)に封入して投与した際
51)使用された LNP は ARCT-021 及び ARCT-154 ワクチンで使用されたものと同様の LNP である。
49
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書