よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
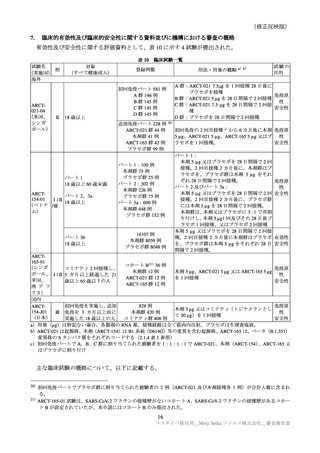
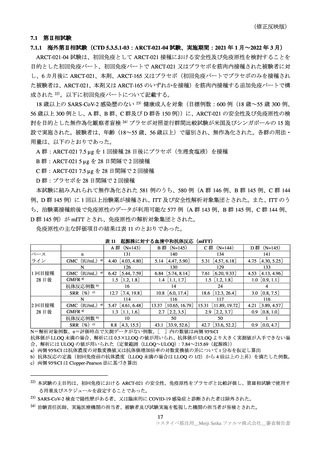
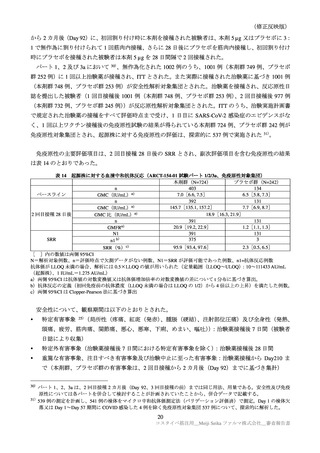
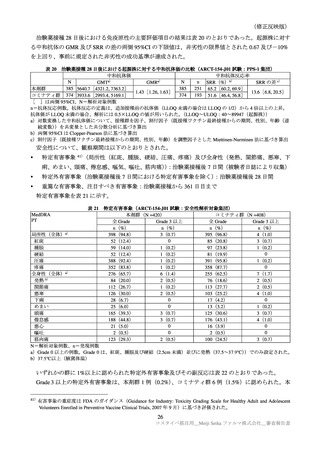
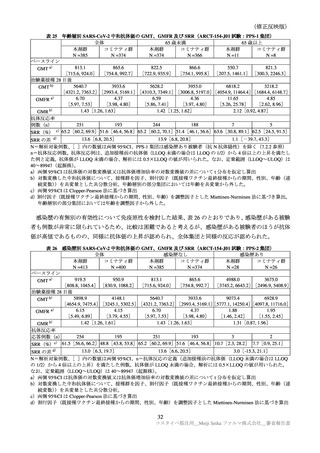
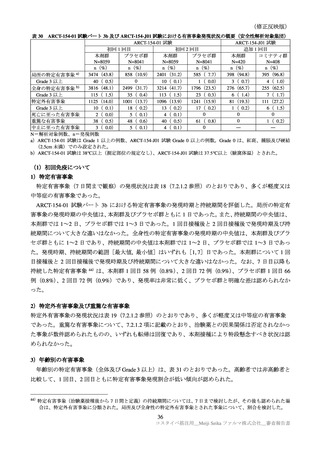
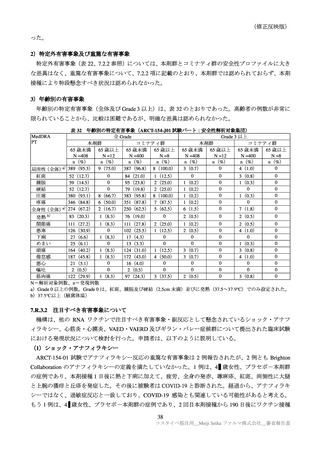
パート 1/2/3a で認められた特定有害事象を表 15 に示す。
表 15
各回接種後における特定有害事象(パート 1/2/3a:反応原性解析対象集団)
1 回目
2 回目
本剤群
プラセボ群
本剤群
プラセボ群
N=748
N=253
N=732
N=245
全 Grade Grade 3 以上 全 Grade Grade 3 以上 全 Grade Grade 3 以上 全 Grade Grade 3 以上
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
a)586(78.3) 27(3.6)
0
51(20.2)
1(0.4)
452(61.7)
18(2.5)
28(11.4)
局所性(全体)
MedDRA
PT
疼痛
485(64.8) 6(0.8) 34(13.4)
0
0
紅斑(発赤)
6(0.8)
0
腫脹(硬結) 25(3.3)
1(0.4)
注射部位圧痛 550(73.5) 26(3.5) 42(16.6)
全身性(全体) 557(74.5) 21(2.8) 120(47.4)
65(8.7)
3(0.4)
3(1.2)
発熱 b)
1(0.4)
0
0
0
2(0.8)
0
359(49.0) 4(0.5)
0
2(0.3)
0
13(1.8)
417(57.0) 17(2.3)
506(69.1) 36(4.9)
77(10.5) 10(1.4)
16(6.5)
0
0
25(10.2)
93(38.0)
5(2.0)
0
0
0
0
1(0.4)
0
頭痛
271(36.2) 6(0.8) 56(22.1) 1(0.4)
疲労
404(54.0) 8(1.1) 72(28.5) 1(0.4)
筋肉痛
322(43.0) 5(0.7) 42(16.6) 1(0.4)
関節痛
222(29.7) 9(1.2) 35(13.8) 1(0.4)
0
0
悪心
37(4.9)
5(2.0)
0
悪寒
190(25.4) 5(0.7) 26(10.3)
0
0
下痢
48(6.4)
16(6.3)
めまい
163(21.8) 5(0.7) 38(15.0) 2(0.8)
0
0
嘔吐
9(1.2)
2(0.8)
N=解析対象例数、n=発現例数
a)Grade 1 以上の例数、b)38℃以上、Grade 3 以上は 39℃以上
271(37.0) 14(1.9)
391(53.4) 18(2.5)
243(33.2) 9(1.2)
204(27.9) 10(1.4)
0
36(4.9)
229(31.3) 7(1.0)
0
31(4.2)
128(17.5) 6(0.8)
0
12(1.6)
45(18.4)
59(24.1)
28(11.4)
22(9.0)
5(2.0)
20(8.2)
9(3.7)
23(9.4)
3(1.2)
1(0.4)
0
0
0
0
0
0
1(0.4)
0
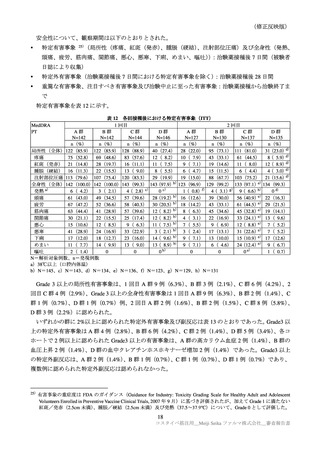
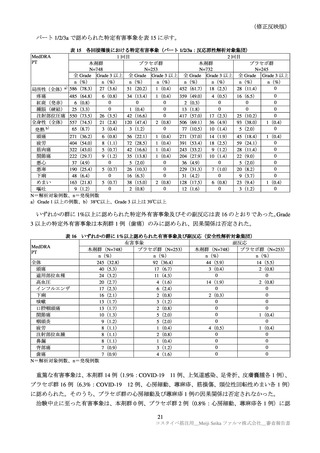
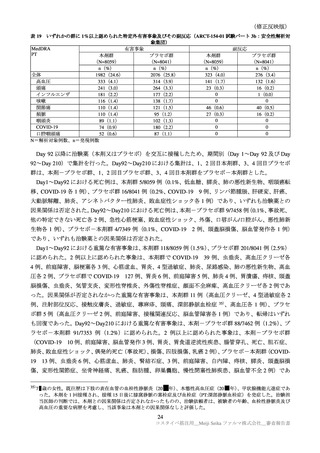
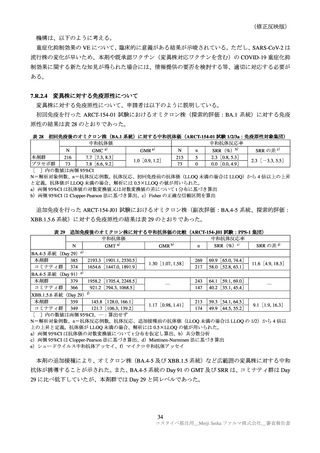
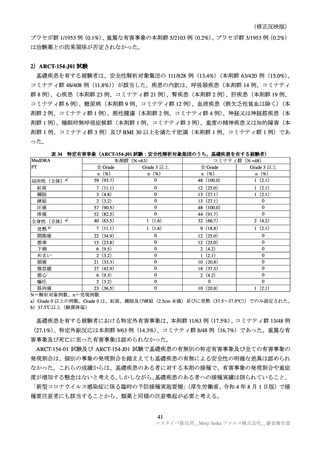
いずれかの群に 1%以上に認められた特定外有害事象及びその副反応は表 16 のとおりであった。
Grade
3 以上の特定外有害事象は本剤群 1 例(歯痛)のみに認められ、因果関係は否定された。
表 16
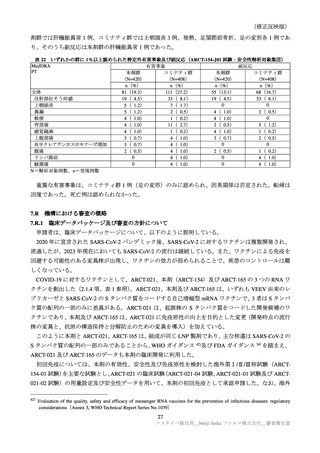
いずれかの群に 1%以上認められた有害事象及び副反応(安全性解析対象集団)
副反応
有害事象
MedDRA
本剤群(N=748)
プラセボ群(N=253)
本剤群(N=748)
プラセボ群(N=253)
PT
n(%)
n(%)
n(%)
n(%)
全体
245(32.8)
92(36.4)
44(5.9)
14(5.5)
頭痛
40(5.3)
17(6.7)
3(0.4)
2(0.8)
0
0
適用部位血種
24(3.2)
11(4.3)
高血圧
20(2.7)
4(1.6)
14(1.9)
2(0.8)
0
0
インフルエンザ
17(2.3)
6(2.4)
0
下痢
16(2.1)
2(0.8)
2(0.3)
0
0
咳嗽
13(1.7)
3(1.2)
0
0
口腔咽頭痛
13(1.7)
2(0.8)
0
関節痛
10(1.3)
5(2.0)
1(0.4)
0
0
咽頭炎
9(1.2)
5(2.0)
疲労
8(1.1)
1(0.4)
4(0.5)
1(0.4)
0
0
注射部位血腫
8(1.1)
2(0.8)
0
0
鼻漏
8(1.1)
1(0.4)
0
0
背部痛
7(0.9)
3(1.2)
0
0
歯痛
7(0.9)
4(1.6)
N=解析対象例数、n=発現例数
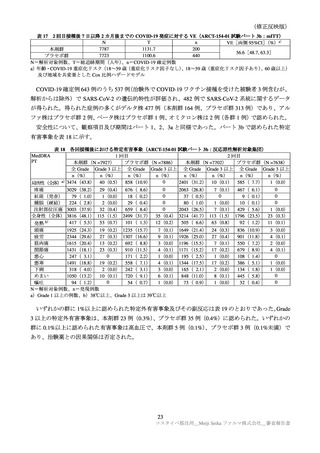
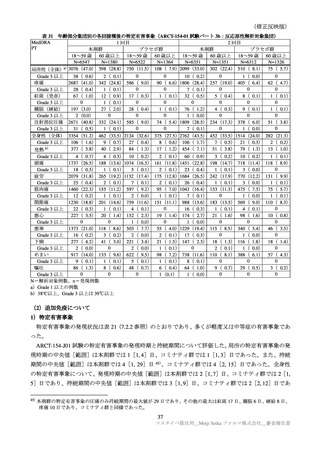
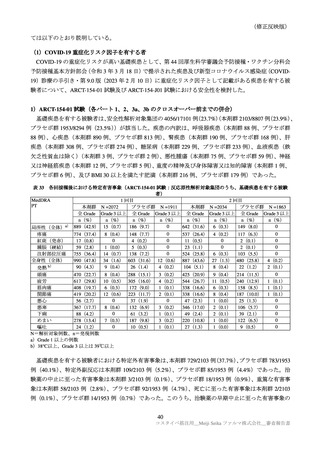
重篤な有害事象は、本剤群 14 例(1.9%:COVID-19
11 例、上気道感染、足骨折、皮膚嚢腫各 1 例)
、
プラセボ群 16 例(6.3%:COVID-19 12 例、心房細動、蕁麻疹、筋損傷、頭位性回転性めまい各 1 例)
に認められた。そのうち、プラセボ群の心房細動及び蕁麻疹 1 例の因果関係は否定されなかった。
治験中止に至った有害事象は、本剤群 0 例、プラセボ群 2 例(0.8%:心房細動、蕁麻疹各 1 例)に認
21
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
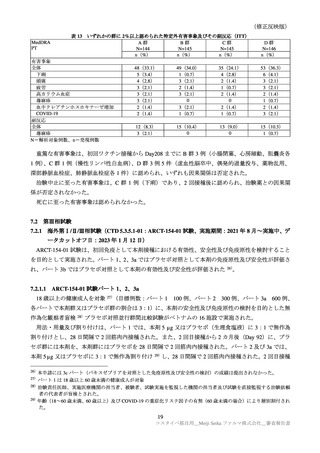
パート 1/2/3a で認められた特定有害事象を表 15 に示す。
表 15
各回接種後における特定有害事象(パート 1/2/3a:反応原性解析対象集団)
1 回目
2 回目
本剤群
プラセボ群
本剤群
プラセボ群
N=748
N=253
N=732
N=245
全 Grade Grade 3 以上 全 Grade Grade 3 以上 全 Grade Grade 3 以上 全 Grade Grade 3 以上
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
a)586(78.3) 27(3.6)
0
51(20.2)
1(0.4)
452(61.7)
18(2.5)
28(11.4)
局所性(全体)
MedDRA
PT
疼痛
485(64.8) 6(0.8) 34(13.4)
0
0
紅斑(発赤)
6(0.8)
0
腫脹(硬結) 25(3.3)
1(0.4)
注射部位圧痛 550(73.5) 26(3.5) 42(16.6)
全身性(全体) 557(74.5) 21(2.8) 120(47.4)
65(8.7)
3(0.4)
3(1.2)
発熱 b)
1(0.4)
0
0
0
2(0.8)
0
359(49.0) 4(0.5)
0
2(0.3)
0
13(1.8)
417(57.0) 17(2.3)
506(69.1) 36(4.9)
77(10.5) 10(1.4)
16(6.5)
0
0
25(10.2)
93(38.0)
5(2.0)
0
0
0
0
1(0.4)
0
頭痛
271(36.2) 6(0.8) 56(22.1) 1(0.4)
疲労
404(54.0) 8(1.1) 72(28.5) 1(0.4)
筋肉痛
322(43.0) 5(0.7) 42(16.6) 1(0.4)
関節痛
222(29.7) 9(1.2) 35(13.8) 1(0.4)
0
0
悪心
37(4.9)
5(2.0)
0
悪寒
190(25.4) 5(0.7) 26(10.3)
0
0
下痢
48(6.4)
16(6.3)
めまい
163(21.8) 5(0.7) 38(15.0) 2(0.8)
0
0
嘔吐
9(1.2)
2(0.8)
N=解析対象例数、n=発現例数
a)Grade 1 以上の例数、b)38℃以上、Grade 3 以上は 39℃以上
271(37.0) 14(1.9)
391(53.4) 18(2.5)
243(33.2) 9(1.2)
204(27.9) 10(1.4)
0
36(4.9)
229(31.3) 7(1.0)
0
31(4.2)
128(17.5) 6(0.8)
0
12(1.6)
45(18.4)
59(24.1)
28(11.4)
22(9.0)
5(2.0)
20(8.2)
9(3.7)
23(9.4)
3(1.2)
1(0.4)
0
0
0
0
0
0
1(0.4)
0
いずれかの群に 1%以上に認められた特定外有害事象及びその副反応は表 16 のとおりであった。
Grade
3 以上の特定外有害事象は本剤群 1 例(歯痛)のみに認められ、因果関係は否定された。
表 16
いずれかの群に 1%以上認められた有害事象及び副反応(安全性解析対象集団)
副反応
有害事象
MedDRA
本剤群(N=748)
プラセボ群(N=253)
本剤群(N=748)
プラセボ群(N=253)
PT
n(%)
n(%)
n(%)
n(%)
全体
245(32.8)
92(36.4)
44(5.9)
14(5.5)
頭痛
40(5.3)
17(6.7)
3(0.4)
2(0.8)
0
0
適用部位血種
24(3.2)
11(4.3)
高血圧
20(2.7)
4(1.6)
14(1.9)
2(0.8)
0
0
インフルエンザ
17(2.3)
6(2.4)
0
下痢
16(2.1)
2(0.8)
2(0.3)
0
0
咳嗽
13(1.7)
3(1.2)
0
0
口腔咽頭痛
13(1.7)
2(0.8)
0
関節痛
10(1.3)
5(2.0)
1(0.4)
0
0
咽頭炎
9(1.2)
5(2.0)
疲労
8(1.1)
1(0.4)
4(0.5)
1(0.4)
0
0
注射部位血腫
8(1.1)
2(0.8)
0
0
鼻漏
8(1.1)
1(0.4)
0
0
背部痛
7(0.9)
3(1.2)
0
0
歯痛
7(0.9)
4(1.6)
N=解析対象例数、n=発現例数
重篤な有害事象は、本剤群 14 例(1.9%:COVID-19
11 例、上気道感染、足骨折、皮膚嚢腫各 1 例)
、
プラセボ群 16 例(6.3%:COVID-19 12 例、心房細動、蕁麻疹、筋損傷、頭位性回転性めまい各 1 例)
に認められた。そのうち、プラセボ群の心房細動及び蕁麻疹 1 例の因果関係は否定されなかった。
治験中止に至った有害事象は、本剤群 0 例、プラセボ群 2 例(0.8%:心房細動、蕁麻疹各 1 例)に認
21
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書