よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
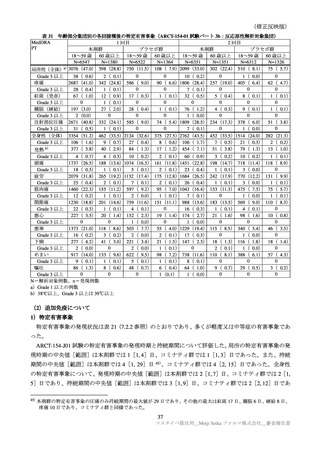
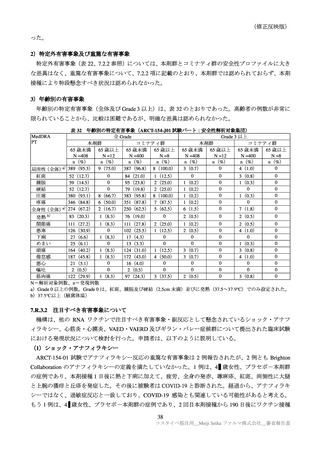
表 19
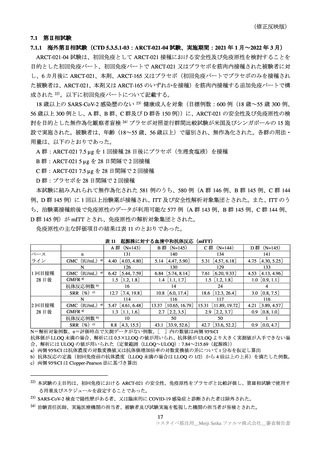
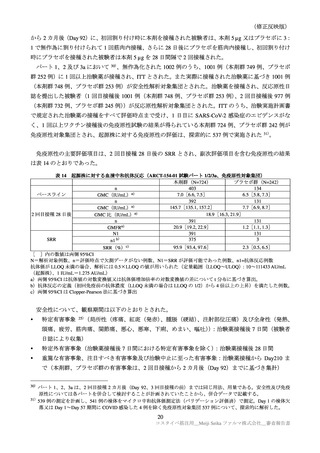
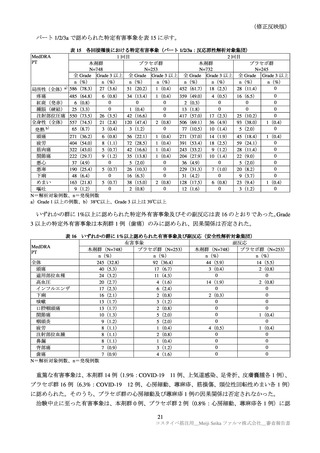
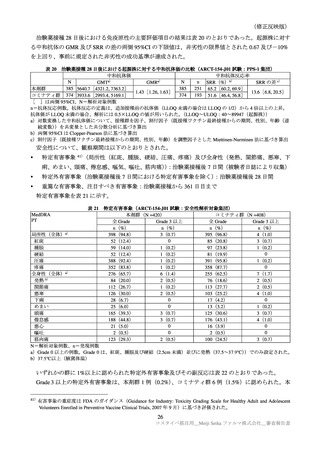
いずれかの群に 1%以上認められた特定外有害事象及びその副反応(ARCT-154-01 試験パート 3b:安全性解析対
象集団)
MedDRA
有害事象
副反応
PT
本剤群
プラセボ群
本剤群
プラセボ群
(N=8059)
(N=8041)
(N=8059)
(N=8041)
n(%)
n(%)
n(%)
n(%)
全体
1982(24.6)
2076(25.8)
323(4.0)
276(3.4)
高血圧
333(4.1)
314(3.9)
141(1.7)
132(1.6)
頭痛
241(3.0)
264(3.3)
23(0.3)
16(0.2)
0
インフルエンザ
181(2.2)
177(2.2)
1(0.0)
0
0
咳嗽
116(1.4)
138(1.7)
関節痛
110(1.4)
121(1.5)
46(0.6)
40(0.5)
頻脈
110(1.4)
95(1.2)
27(0.3)
16(0.2)
0
0
咽頭炎
89(1.1)
102(1.3)
COVID-19
0
0
74(0.9)
180(2.2)
0
0
口腔咽頭痛
52(0.6)
87(1.1)
N=解析対象例数、n=発現例数
Day 92 以降に治験薬(本剤又はプラセボ)を交互に接種したため、期間別(Day 1~Day 92 及び Day
92~Day 210)で集計を行った。Day92~Day210 における集計は、1、2 回目本剤群、3、4 回目プラセボ
群は、本剤-プラセボ群、1、2 回目プラセボ群、3、4 回目本剤群をプラセボ-本剤群とした。
Day1~Day92 における死亡例は、本剤群 5/8059 例(0.1%、低血糖、膵炎、肺の悪性新生物、咽頭癌転
移、COVID-19 各 1 例)
、プラセボ群 16/8041 例(0.2%、COVID-19 9 例、リンパ節腫脹、肝硬変、肝癌、
大動脈解離、肺炎、アシネトバクター性肺炎、敗血症性ショック各 1 例)であり、いずれも治験薬との
因果関係は否定された。Day92~Day210 における死亡例は、本剤-プラセボ群 9/7458 例(0.1%、事故死、
他の特定できない死亡各 2 例、急性心筋梗塞、敗血症性ショック、外傷、口唇がん/口腔がん、悪性肺新
生物各 1 例)
、プラセボ-本剤群 4/7349 例(0.1%、COVID-19 2 例、頭蓋脳損傷、脳血管発作各 1 例)
であり、いずれも治験薬との因果関係は否定された。
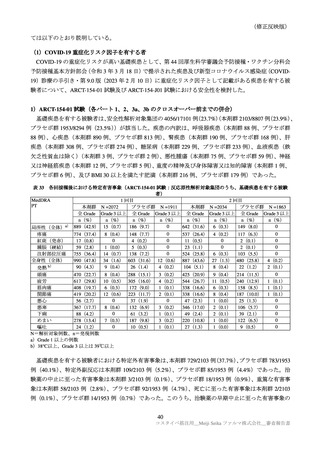
Day1~Day92 における重篤な有害事象は、本剤群 118/8059 例(1.5%)
、プラセボ群 201/8041 例(2.5%)
に認められた。2 例以上に認められた事象は、本剤群で COVID-19 39 例、虫垂炎、高血圧クリーゼ各
4 例、前庭障害、脳梗塞各 3 例、心筋虚血、胃炎、4 型過敏症、肺炎、尿路感染、肺の悪性新生物、高血
圧各 2 例、プラセボ群で COVID-19 127 例、胃炎 6 例、前庭障害 5 例、肺炎 4 例、胃潰瘍、痔核、頭蓋
脳損傷、虫垂炎、気管支炎、変形性脊椎炎、外傷性脊椎症、顔面不全麻痺、高血圧クリーゼ各 2 例であ
った。因果関係が否定されなかった重篤な有害事象は、本剤群 11 例(高血圧クリーゼ、4 型過敏症各 2
例、注射部位反応、接触皮膚炎、過敏症、蕁麻疹、頭痛、深部静脈血栓症 35)、高血圧各 1 例)
、プラセ
ボ群 5 例(高血圧クリーゼ 2 例、前庭障害、接種関連反応、脳血管障害各 1 例)であり、転帰はいずれ
も回復であった。Day92~Day210 における重篤な有害事象は、本剤-プラセボ群 88/7462 例(1.2%)
、プ
ラセボ-本剤群 91/7353 例(1.2%)に認められた。2 例以上に認められた事象は、本剤-プラセボ群
(COVID-19 10 例、前庭障害、脳血管発作 3 例、胃炎、胃食道逆流性疾患、腸管穿孔、死亡、胆石症、
肺炎、敗血症性ショック、偶発的死亡(事故死)
、損傷、四肢損傷、乳癌 2 例)
、プラセボ-本剤群(COVID19
13 例、虫垂炎 6 例、心筋虚血、肺炎、腎結石症、3 例、前庭障害、白内障、痔核、膵炎、頭蓋脳損
傷、変形性関節症、坐骨神経痛、乳癌、脂肪腫、卵巣嚢胞、慢性閉塞性肺疾患、脳血管不全 2 例)であ
35)7
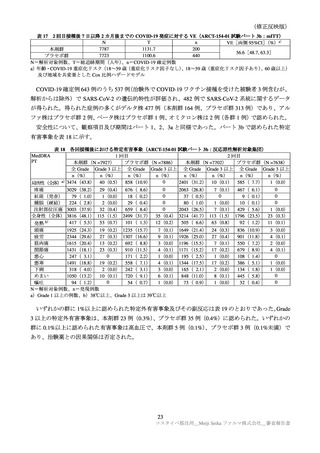
歳の女性。既往歴は下肢の表在血管の血栓性静脈炎(20 年)
、本態性高血圧症(20 年)
、甲状腺機能亢進症であ
った。本剤を 1 回接種され、接種 15 日後に膝窩静脈の塞栓症及び血栓症(PT:深部静脈血栓症)を発症した。治験担
当医師の判断では、本剤との因果関係は否定されなかったものの、治験依頼者は、被験者の年齢、血栓性静脈炎及び
高血圧の重要な病歴を考慮し、当該事象は本剤との因果関係なしと評価した。
24
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
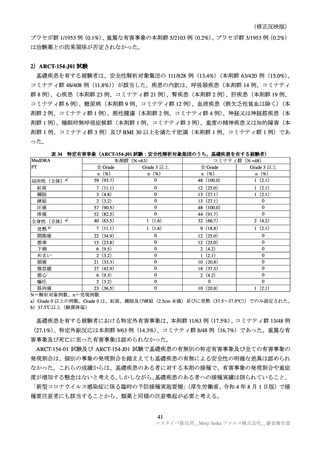
表 19
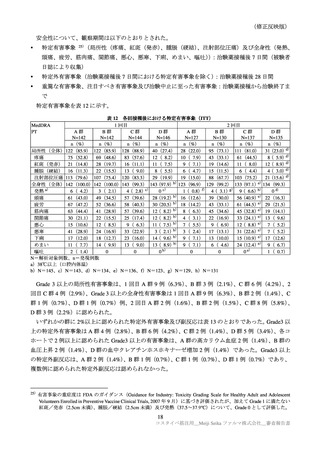
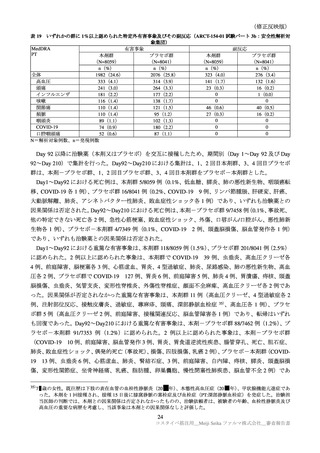
いずれかの群に 1%以上認められた特定外有害事象及びその副反応(ARCT-154-01 試験パート 3b:安全性解析対
象集団)
MedDRA
有害事象
副反応
PT
本剤群
プラセボ群
本剤群
プラセボ群
(N=8059)
(N=8041)
(N=8059)
(N=8041)
n(%)
n(%)
n(%)
n(%)
全体
1982(24.6)
2076(25.8)
323(4.0)
276(3.4)
高血圧
333(4.1)
314(3.9)
141(1.7)
132(1.6)
頭痛
241(3.0)
264(3.3)
23(0.3)
16(0.2)
0
インフルエンザ
181(2.2)
177(2.2)
1(0.0)
0
0
咳嗽
116(1.4)
138(1.7)
関節痛
110(1.4)
121(1.5)
46(0.6)
40(0.5)
頻脈
110(1.4)
95(1.2)
27(0.3)
16(0.2)
0
0
咽頭炎
89(1.1)
102(1.3)
COVID-19
0
0
74(0.9)
180(2.2)
0
0
口腔咽頭痛
52(0.6)
87(1.1)
N=解析対象例数、n=発現例数
Day 92 以降に治験薬(本剤又はプラセボ)を交互に接種したため、期間別(Day 1~Day 92 及び Day
92~Day 210)で集計を行った。Day92~Day210 における集計は、1、2 回目本剤群、3、4 回目プラセボ
群は、本剤-プラセボ群、1、2 回目プラセボ群、3、4 回目本剤群をプラセボ-本剤群とした。
Day1~Day92 における死亡例は、本剤群 5/8059 例(0.1%、低血糖、膵炎、肺の悪性新生物、咽頭癌転
移、COVID-19 各 1 例)
、プラセボ群 16/8041 例(0.2%、COVID-19 9 例、リンパ節腫脹、肝硬変、肝癌、
大動脈解離、肺炎、アシネトバクター性肺炎、敗血症性ショック各 1 例)であり、いずれも治験薬との
因果関係は否定された。Day92~Day210 における死亡例は、本剤-プラセボ群 9/7458 例(0.1%、事故死、
他の特定できない死亡各 2 例、急性心筋梗塞、敗血症性ショック、外傷、口唇がん/口腔がん、悪性肺新
生物各 1 例)
、プラセボ-本剤群 4/7349 例(0.1%、COVID-19 2 例、頭蓋脳損傷、脳血管発作各 1 例)
であり、いずれも治験薬との因果関係は否定された。
Day1~Day92 における重篤な有害事象は、本剤群 118/8059 例(1.5%)
、プラセボ群 201/8041 例(2.5%)
に認められた。2 例以上に認められた事象は、本剤群で COVID-19 39 例、虫垂炎、高血圧クリーゼ各
4 例、前庭障害、脳梗塞各 3 例、心筋虚血、胃炎、4 型過敏症、肺炎、尿路感染、肺の悪性新生物、高血
圧各 2 例、プラセボ群で COVID-19 127 例、胃炎 6 例、前庭障害 5 例、肺炎 4 例、胃潰瘍、痔核、頭蓋
脳損傷、虫垂炎、気管支炎、変形性脊椎炎、外傷性脊椎症、顔面不全麻痺、高血圧クリーゼ各 2 例であ
った。因果関係が否定されなかった重篤な有害事象は、本剤群 11 例(高血圧クリーゼ、4 型過敏症各 2
例、注射部位反応、接触皮膚炎、過敏症、蕁麻疹、頭痛、深部静脈血栓症 35)、高血圧各 1 例)
、プラセ
ボ群 5 例(高血圧クリーゼ 2 例、前庭障害、接種関連反応、脳血管障害各 1 例)であり、転帰はいずれ
も回復であった。Day92~Day210 における重篤な有害事象は、本剤-プラセボ群 88/7462 例(1.2%)
、プ
ラセボ-本剤群 91/7353 例(1.2%)に認められた。2 例以上に認められた事象は、本剤-プラセボ群
(COVID-19 10 例、前庭障害、脳血管発作 3 例、胃炎、胃食道逆流性疾患、腸管穿孔、死亡、胆石症、
肺炎、敗血症性ショック、偶発的死亡(事故死)
、損傷、四肢損傷、乳癌 2 例)
、プラセボ-本剤群(COVID19
13 例、虫垂炎 6 例、心筋虚血、肺炎、腎結石症、3 例、前庭障害、白内障、痔核、膵炎、頭蓋脳損
傷、変形性関節症、坐骨神経痛、乳癌、脂肪腫、卵巣嚢胞、慢性閉塞性肺疾患、脳血管不全 2 例)であ
35)7
歳の女性。既往歴は下肢の表在血管の血栓性静脈炎(20 年)
、本態性高血圧症(20 年)
、甲状腺機能亢進症であ
った。本剤を 1 回接種され、接種 15 日後に膝窩静脈の塞栓症及び血栓症(PT:深部静脈血栓症)を発症した。治験担
当医師の判断では、本剤との因果関係は否定されなかったものの、治験依頼者は、被験者の年齢、血栓性静脈炎及び
高血圧の重要な病歴を考慮し、当該事象は本剤との因果関係なしと評価した。
24
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書