よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (50 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
7.R.5.2 接種対象について
申請者は、本剤の接種対象に関して、以下のように説明している。
(1)接種対象年齢について
本剤の初回免疫及び追加免疫の対象年齢について、ARCT-154-01 試験及び ARCT-154-J01 試験の対象
年齢を踏まえ 18 歳以上とし、用法・用量に関連する注意に設定した。
(2)本剤接種前のワクチン接種歴について
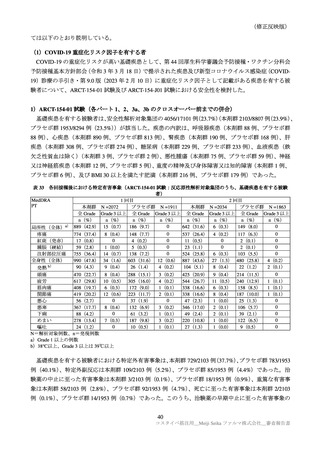
ARCT-154-J01 試験では、初回免疫(2 回接種)及び追加免疫 1 回接種を完了した被験者における、2
回目の追加免疫(以下、4 回目接種)について、ARCT-165-01 試験では、初回免疫(2 回接種)を完了し
た被験者における追加免疫 1 回目(以下、3 回目接種)について、有効性(免疫原性)及び安全性を検
討した。
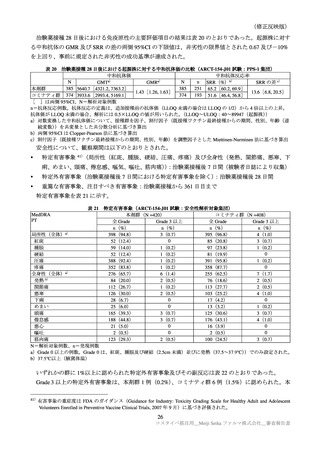
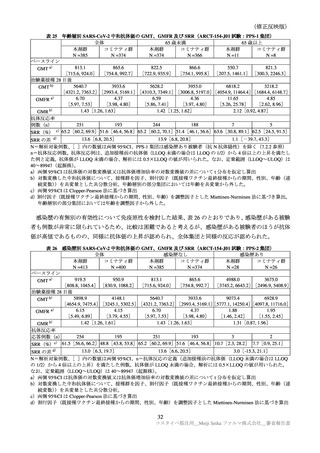
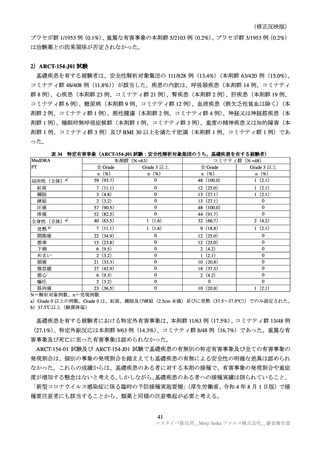
ARCT-154-J01 試験及び ARCT-165-01 試験において、
治験薬接種 28 日後における起源株に対する GMR
及び SRR は同様であった。また、安全性についても、各試験の接種 1 カ月後までの安全性データから、
両試験で本剤の安全性プロファイルに大きな違いはなかった。これらの臨床試験において、試験前の
SARS-CoV-2 ワクチン接種回数の違いによらず、免疫原性及び安全性は同様であったこと、類薬である
既承認 RNA ワクチンの知見を踏まえると(JAMA 2023; 6:e232598、MMWR 2022;71:971-76.)
、本剤接種
前の SARS-CoV-2 ワクチン接種回数に特段の制限を設けることなく、本剤を追加接種することは可能と
考える。また、接種したワクチンの種類について、RNA ワクチン(コミナティ又はスパイクバックス)
以外の SARS-CoV-2 ワクチンを接種した者に対する本剤の接種に関するデータはない。英国の大規模研
究において、コミナティやスパイクバックスでは、接種歴についてワクチンの種類を問わず、SARS-CoV2 に対する中和抗体反応及び細胞性免疫反応を誘導したとの報告がある(Lancet 2021; 398: 2258–76.)
。こ
れらの既承認 RNA ワクチンにおけるデータより、本剤においても同様に接種済みワクチンの種類によ
らず、本剤の追加接種による有効性及び安全性が期待できると考えるものの、RNA ワクチン以外の
SARS-CoV-2 ワクチン接種歴がある者に対する本剤の接種に関するデータを有していないことから、そ
の旨を添付文書で注意喚起する。
機構は、以下のように考える。
申請者の説明はいずれも了承可能である。現時点における本邦での SARS-CoV-2 ワクチンの接種状況
に照らすと接種回数は年齢や職種等によっても異なっており一律ではないこと等から、SARS-CoV-2 ワ
クチンの初回免疫完了例であれば、それ以降の接種回数を制限することなく本剤の追加接種を使用可能
とすることには一定の意義があると判断した。
7.R.5.3 追加免疫時の接種間隔について
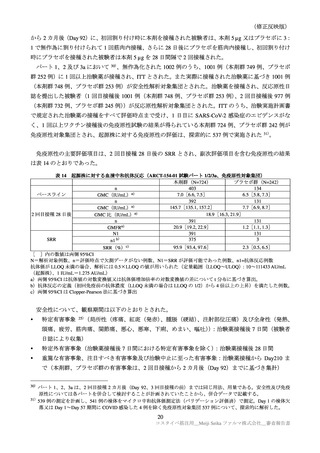
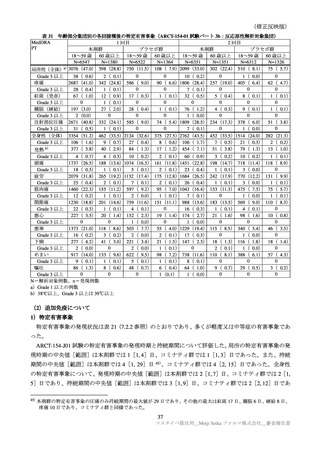
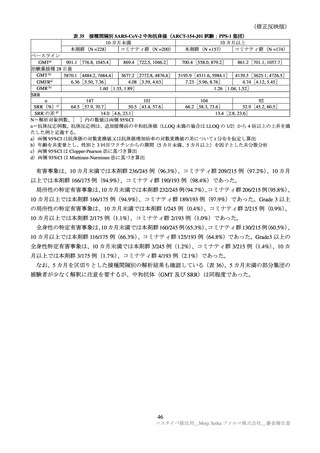
申請者は、ARCT-154-J01 試験において、追加接種時の最終接種からの接種間隔別の免疫原性及び安全
性について検討した。ARCT-154-J01 試験では、既承認のコミナティの 3 回目接種から 3 カ月以上経過し
た者を対象としており、主要解析対象集団(PPS-1)における接種間隔(3 回目接種から治験薬接種まで
の期間)の中央値[範囲]は 9.7[4.2, 14.0]カ月であった。PPS-1 における接種間隔別の免疫原性の結
果は表 35 のとおりであった。
45
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
7.R.5.2 接種対象について
申請者は、本剤の接種対象に関して、以下のように説明している。
(1)接種対象年齢について
本剤の初回免疫及び追加免疫の対象年齢について、ARCT-154-01 試験及び ARCT-154-J01 試験の対象
年齢を踏まえ 18 歳以上とし、用法・用量に関連する注意に設定した。
(2)本剤接種前のワクチン接種歴について
ARCT-154-J01 試験では、初回免疫(2 回接種)及び追加免疫 1 回接種を完了した被験者における、2
回目の追加免疫(以下、4 回目接種)について、ARCT-165-01 試験では、初回免疫(2 回接種)を完了し
た被験者における追加免疫 1 回目(以下、3 回目接種)について、有効性(免疫原性)及び安全性を検
討した。
ARCT-154-J01 試験及び ARCT-165-01 試験において、
治験薬接種 28 日後における起源株に対する GMR
及び SRR は同様であった。また、安全性についても、各試験の接種 1 カ月後までの安全性データから、
両試験で本剤の安全性プロファイルに大きな違いはなかった。これらの臨床試験において、試験前の
SARS-CoV-2 ワクチン接種回数の違いによらず、免疫原性及び安全性は同様であったこと、類薬である
既承認 RNA ワクチンの知見を踏まえると(JAMA 2023; 6:e232598、MMWR 2022;71:971-76.)
、本剤接種
前の SARS-CoV-2 ワクチン接種回数に特段の制限を設けることなく、本剤を追加接種することは可能と
考える。また、接種したワクチンの種類について、RNA ワクチン(コミナティ又はスパイクバックス)
以外の SARS-CoV-2 ワクチンを接種した者に対する本剤の接種に関するデータはない。英国の大規模研
究において、コミナティやスパイクバックスでは、接種歴についてワクチンの種類を問わず、SARS-CoV2 に対する中和抗体反応及び細胞性免疫反応を誘導したとの報告がある(Lancet 2021; 398: 2258–76.)
。こ
れらの既承認 RNA ワクチンにおけるデータより、本剤においても同様に接種済みワクチンの種類によ
らず、本剤の追加接種による有効性及び安全性が期待できると考えるものの、RNA ワクチン以外の
SARS-CoV-2 ワクチン接種歴がある者に対する本剤の接種に関するデータを有していないことから、そ
の旨を添付文書で注意喚起する。
機構は、以下のように考える。
申請者の説明はいずれも了承可能である。現時点における本邦での SARS-CoV-2 ワクチンの接種状況
に照らすと接種回数は年齢や職種等によっても異なっており一律ではないこと等から、SARS-CoV-2 ワ
クチンの初回免疫完了例であれば、それ以降の接種回数を制限することなく本剤の追加接種を使用可能
とすることには一定の意義があると判断した。
7.R.5.3 追加免疫時の接種間隔について
申請者は、ARCT-154-J01 試験において、追加接種時の最終接種からの接種間隔別の免疫原性及び安全
性について検討した。ARCT-154-J01 試験では、既承認のコミナティの 3 回目接種から 3 カ月以上経過し
た者を対象としており、主要解析対象集団(PPS-1)における接種間隔(3 回目接種から治験薬接種まで
の期間)の中央値[範囲]は 9.7[4.2, 14.0]カ月であった。PPS-1 における接種間隔別の免疫原性の結
果は表 35 のとおりであった。
45
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書