よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
工程の追加である。
非臨床試験用の原薬は製法 a、臨床試験用の原薬は製法 a 又は製法 b により製造され、申請製剤の原
薬は製法 b で製造される。なお、製法変更前後の原薬の規格試験で同等性/同質性が確認されている。
開発候補品 ARCT-021、ARCT-154(本剤)及び ARCT-165(変異株用ワクチン)の原薬(mRNA-2002、
mRNA-2105 及び mRNA-2106)にコードされる S タンパク質の種類と導入された変異は下表のとおりで
ある。
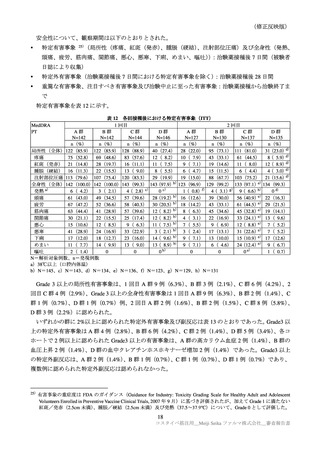
表 1 mRNA と製剤の名称、S タンパク質の種類及び変異
開発原薬
製剤の治験成分記号 コードされる S タンパク質遺伝子の種類及び変異 a)
mRNA-2002
起源株(WA1/2020 系統)
ARCT-021
起源株(WA1/2020 系統)に、以下の変異を含む。
mRNA-2105
ARCT-154(本剤) ・D614G(起源株 B1 系統の変異)
(ザポメラン)
・K986P、V987P、R682G、R683S、R685S
ベータ株(B1.351 系統)に、以下の変異を含む。
・D614G(起源株 B1 系統の変異)
mRNA-2106
ARCT-165
・K986P、V987P、R682G、R683S、R685S
a)VEEV レプリカーゼは全て同一のアミノ酸配列
主な用途
品質、非臨床、臨床
品質、非臨床、臨床
臨床
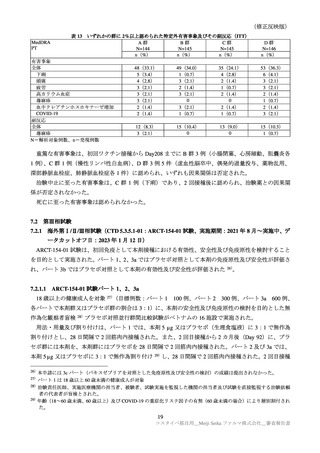
2.1.5 特性
2.1.5.1 構造及び特性
表 2 に示す特性解析が実施された。
表 2 特性解析における評価項目
試験方法
項目
一次構造
物理化学的性質
生物学的性質
RNA 配列
5′キャップ構造、ポリ A 鎖長分布
紫外吸収スペクトル
In vitro 生物活性(
)
サンガー配列決定法、
-HPLC 及び
紫外可視吸光度測定法
セルベースアッセイ(
及び
)
2.1.5.2 目的物質関連物質/目的物質由来不純物
目的物質由来不純物は 不純物A* とされ、原薬の規格及び試験方法により適切に管理されている。
なお、目的物質関連物質は特定されていない。
2.1.5.3 製造工程由来不純物
た。残留プラスミド DNA、
不純物B*
、 不純物C* 及び元素不純物とされ
不純物B*
製造工程由来不純物は、残留プラスミド DNA、
及び 不純物C* は、原薬の規格及び試験方法により適切に
管理されている。元素不純物は、製造工程において十分に除去されることが確認されている。
2.1.6 原薬の管理
原薬の規格及び試験方法として、性状、確認試験(
)
、pH、5′キャップ化率(
(
電気泳動及び
)
、ポリ A 鎖(
)
、残留プラスミド DNA(
)、純度試験[mRNA(電気泳動)
、
)及び
(紫外可視吸光度測定法)
、エンドトキシン、微生物限度及び力価(
(
)]
、含量
)が設定されている。
2.1.7 原薬の安定性
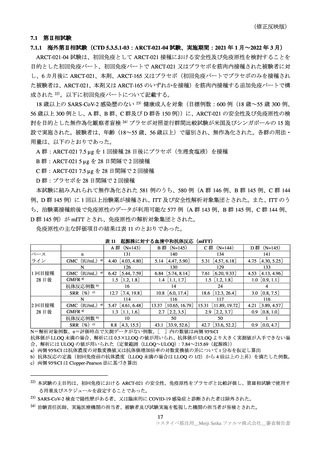
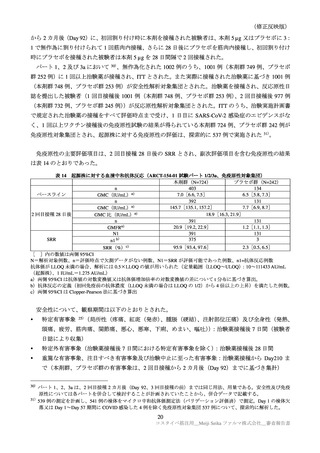
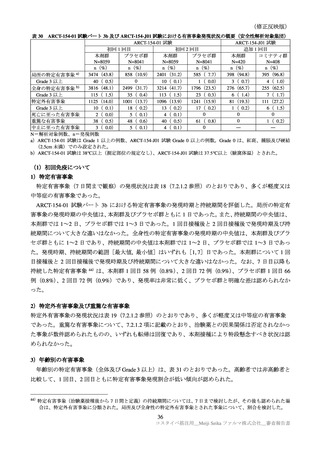
原薬の主な安定性試験の概略は、表 3 のとおりである。
4
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
*新薬承認情報提供時に置き換えた
工程の追加である。
非臨床試験用の原薬は製法 a、臨床試験用の原薬は製法 a 又は製法 b により製造され、申請製剤の原
薬は製法 b で製造される。なお、製法変更前後の原薬の規格試験で同等性/同質性が確認されている。
開発候補品 ARCT-021、ARCT-154(本剤)及び ARCT-165(変異株用ワクチン)の原薬(mRNA-2002、
mRNA-2105 及び mRNA-2106)にコードされる S タンパク質の種類と導入された変異は下表のとおりで
ある。
表 1 mRNA と製剤の名称、S タンパク質の種類及び変異
開発原薬
製剤の治験成分記号 コードされる S タンパク質遺伝子の種類及び変異 a)
mRNA-2002
起源株(WA1/2020 系統)
ARCT-021
起源株(WA1/2020 系統)に、以下の変異を含む。
mRNA-2105
ARCT-154(本剤) ・D614G(起源株 B1 系統の変異)
(ザポメラン)
・K986P、V987P、R682G、R683S、R685S
ベータ株(B1.351 系統)に、以下の変異を含む。
・D614G(起源株 B1 系統の変異)
mRNA-2106
ARCT-165
・K986P、V987P、R682G、R683S、R685S
a)VEEV レプリカーゼは全て同一のアミノ酸配列
主な用途
品質、非臨床、臨床
品質、非臨床、臨床
臨床
2.1.5 特性
2.1.5.1 構造及び特性
表 2 に示す特性解析が実施された。
表 2 特性解析における評価項目
試験方法
項目
一次構造
物理化学的性質
生物学的性質
RNA 配列
5′キャップ構造、ポリ A 鎖長分布
紫外吸収スペクトル
In vitro 生物活性(
)
サンガー配列決定法、
-HPLC 及び
紫外可視吸光度測定法
セルベースアッセイ(
及び
)
2.1.5.2 目的物質関連物質/目的物質由来不純物
目的物質由来不純物は 不純物A* とされ、原薬の規格及び試験方法により適切に管理されている。
なお、目的物質関連物質は特定されていない。
2.1.5.3 製造工程由来不純物
た。残留プラスミド DNA、
不純物B*
、 不純物C* 及び元素不純物とされ
不純物B*
製造工程由来不純物は、残留プラスミド DNA、
及び 不純物C* は、原薬の規格及び試験方法により適切に
管理されている。元素不純物は、製造工程において十分に除去されることが確認されている。
2.1.6 原薬の管理
原薬の規格及び試験方法として、性状、確認試験(
)
、pH、5′キャップ化率(
(
電気泳動及び
)
、ポリ A 鎖(
)
、残留プラスミド DNA(
)、純度試験[mRNA(電気泳動)
、
)及び
(紫外可視吸光度測定法)
、エンドトキシン、微生物限度及び力価(
(
)]
、含量
)が設定されている。
2.1.7 原薬の安定性
原薬の主な安定性試験の概略は、表 3 のとおりである。
4
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
*新薬承認情報提供時に置き換えた