よむ、つかう、まなぶ。
参考資料1 コスタイベ筋注用 審議結果報告書 (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43635.html |
| 出典情報 | 薬事審議会 血液事業部会安全技術調査会(令和6年度第2回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(修正反映版)
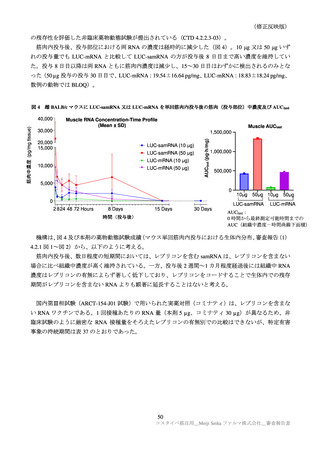
った。
2)特定外有害事象及び重篤な有害事象
特定外有害事象(表 22、7.2.2 参照)については、本剤群とコミナティ群の安全性プロファイルに大き
な差異はなく、重篤な有害事象について、7.2.2 項に記載のとおり、本剤群では認められておらず、本剤
接種により特段懸念すべき状況は認められなかった。
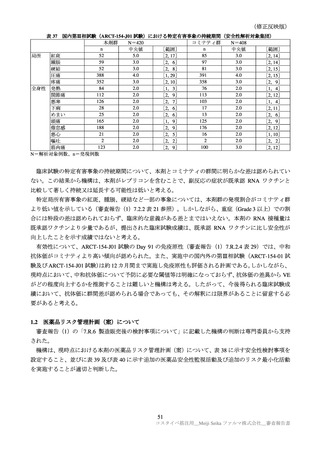
3)年齢別の有害事象
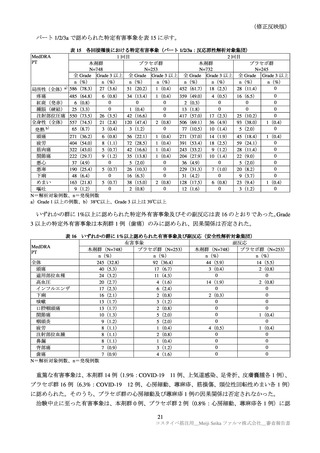
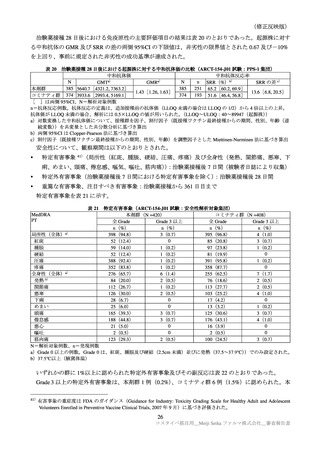
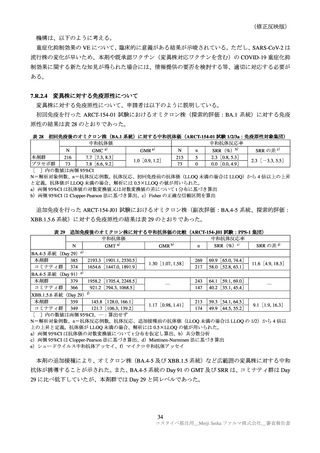
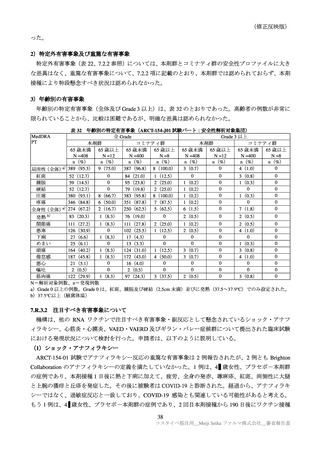
年齢別の特定有害事象(全体及び Grade 3 以上)は、表 32 のとおりであった。高齢者の例数が非常に
限られていることから、比較は困難であるが、明確な差異は認められなかった。
表 32
年齢別の特定有害事象(ARCT-154-J01 試験パート:安全性解析対象集団)
全 Grade
Grade 3 以上
本剤群
コミナティ群
本剤群
コミナティ群
65 歳未満
65 歳以上
65 歳未満
65 歳以上
65 歳未満
65 歳以上
65 歳未満
65 歳以上
N =408
N =12
N =400
N =8
N =408
N =12
N =400
N =8
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
0
0
3(0.7)
4(1.0)
局所性(全体)a) 389(95.3) 9(75.0) 387(96.8) 8(100.0)
0
0
0
0
紅斑
52(12.7)
84(21.0) 1(12.5)
3(0.8)
0
0
0
腫脹
59(14.5)
95(23.8) 2(25.0)
1(0.2)
1(0.3)
0
0
0
0
硬結
52(12.7)
79(19.8) 2(25.0)
1(0.2)
0
0
圧痛
380(93.1) 8(66.7) 383(95.8) 8(100.0)
1(0.2)
1(0.3)
0
0
0
疼痛
346(84.8) 6(50.0) 351(87.8) 7(87.5)
1(0.2)
) 274(67.2) 2(16.7) 250(62.5) 5(62.5)
a
0
0
6(1.5)
7(1.8)
全身性(全体)
MedDRA
PT
0
0
0
83(20.3)
1(8.3)
76(19.0)
2(0.5)
2(0.5)
発熱 b)
0
0
関節痛
111(27.2) 1(8.3) 111(27.8) 2(25.0)
1(0.2)
2(0.5)
0
0
0
悪寒
126(30.9)
102(25.5) 1(12.5)
2(0.5)
4(1.0)
0
0
0
0
0
下痢
27(6.6)
1(8.3)
17(4.3)
0
0
0
0
0
めまい
25(6.1)
13(3.3)
1(0.3)
0
0
頭痛
164(40.2) 1(8.3) 124(31.0) 1(12.5)
3(0.7)
3(0.8)
0
0
倦怠感
187(45.8) 1(8.3) 172(43.0) 4(50.0)
3(0.7)
4(1.0)
0
0
0
0
0
0
悪心
21(5.1)
16(4.0)
0
0
0
0
0
0
嘔吐
2(0.5)
2(0.5)
0
0
筋肉痛
122(29.9) 1(8.3)
97(24.3) 3(37.5)
2(0.5)
3(0.8)
N=解析対象例数、n=発現例数
a)Grade 0 以上の例数。Grade 0 は、紅斑、腫脹及び硬結(2.5cm 未満)並びに発熱(37.5~37.9℃)でのみ設定された。
b)37.5℃以上(腋窩体温)
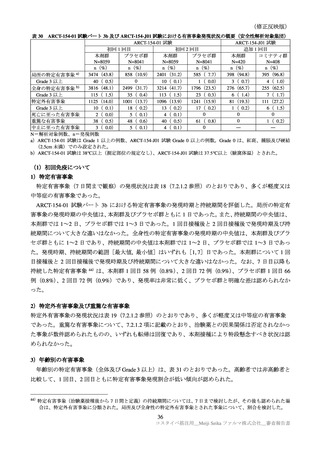
7.R.3.2 注目すべき有害事象について
機構は、他の RNA ワクチンで注目すべき有害事象・副反応として懸念されているショック・アナフ
ィラキシー、心筋炎・心膜炎、VAED・VAERD 及びギラン・バレー症候群について提出された臨床試験
における発現状況について検討を行った。申請者は、以下のように説明している。
(1)ショック・アナフィラキシー
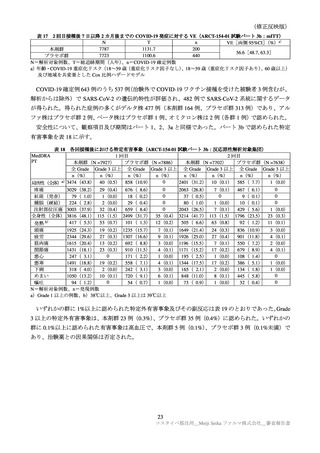
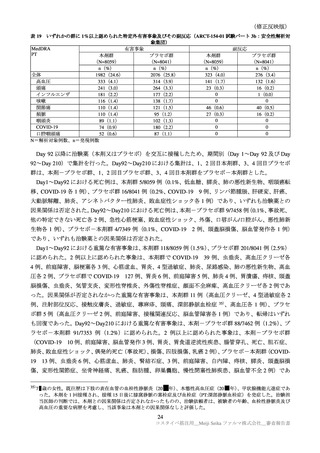
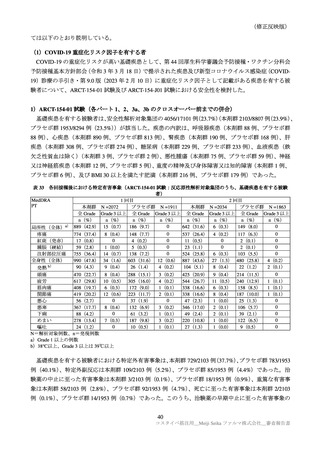
ARCT-154-01 試験でアナフィラキシー反応の重篤な有害事象は 2 例報告されたが、2 例とも Brighton
Collaboration のアナフィラキシーの定義を満たしていなかった。1 例は、4 歳女性、プラセボ-本剤群
の症例であり、本剤接種 1 日後に熱と下痢に加えて、疲労、全身の発赤、蕁麻疹、紅斑、両側性に大腿
と上腕の搔痒と丘疹を発症した。その後に被験者は COVID‐19 と診断された。経過から、アナフィラキ
シーではなく、過敏症反応と一致しており、COVID-19 感染とも関連している可能性があると考える。
もう 1 例は、4 歳女性、プラセボ-本剤群の症例であり、2 回目本剤接種から 190 日後にワクチン接種
38
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書
った。
2)特定外有害事象及び重篤な有害事象
特定外有害事象(表 22、7.2.2 参照)については、本剤群とコミナティ群の安全性プロファイルに大き
な差異はなく、重篤な有害事象について、7.2.2 項に記載のとおり、本剤群では認められておらず、本剤
接種により特段懸念すべき状況は認められなかった。
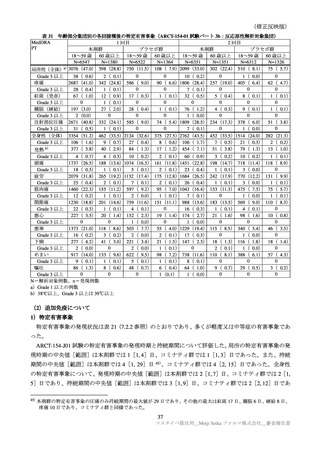
3)年齢別の有害事象
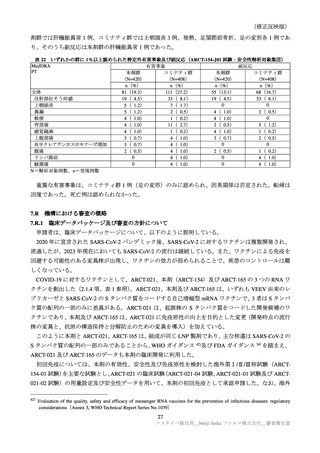
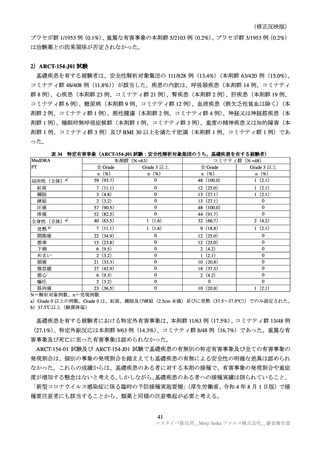
年齢別の特定有害事象(全体及び Grade 3 以上)は、表 32 のとおりであった。高齢者の例数が非常に
限られていることから、比較は困難であるが、明確な差異は認められなかった。
表 32
年齢別の特定有害事象(ARCT-154-J01 試験パート:安全性解析対象集団)
全 Grade
Grade 3 以上
本剤群
コミナティ群
本剤群
コミナティ群
65 歳未満
65 歳以上
65 歳未満
65 歳以上
65 歳未満
65 歳以上
65 歳未満
65 歳以上
N =408
N =12
N =400
N =8
N =408
N =12
N =400
N =8
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
n(%)
0
0
3(0.7)
4(1.0)
局所性(全体)a) 389(95.3) 9(75.0) 387(96.8) 8(100.0)
0
0
0
0
紅斑
52(12.7)
84(21.0) 1(12.5)
3(0.8)
0
0
0
腫脹
59(14.5)
95(23.8) 2(25.0)
1(0.2)
1(0.3)
0
0
0
0
硬結
52(12.7)
79(19.8) 2(25.0)
1(0.2)
0
0
圧痛
380(93.1) 8(66.7) 383(95.8) 8(100.0)
1(0.2)
1(0.3)
0
0
0
疼痛
346(84.8) 6(50.0) 351(87.8) 7(87.5)
1(0.2)
) 274(67.2) 2(16.7) 250(62.5) 5(62.5)
a
0
0
6(1.5)
7(1.8)
全身性(全体)
MedDRA
PT
0
0
0
83(20.3)
1(8.3)
76(19.0)
2(0.5)
2(0.5)
発熱 b)
0
0
関節痛
111(27.2) 1(8.3) 111(27.8) 2(25.0)
1(0.2)
2(0.5)
0
0
0
悪寒
126(30.9)
102(25.5) 1(12.5)
2(0.5)
4(1.0)
0
0
0
0
0
下痢
27(6.6)
1(8.3)
17(4.3)
0
0
0
0
0
めまい
25(6.1)
13(3.3)
1(0.3)
0
0
頭痛
164(40.2) 1(8.3) 124(31.0) 1(12.5)
3(0.7)
3(0.8)
0
0
倦怠感
187(45.8) 1(8.3) 172(43.0) 4(50.0)
3(0.7)
4(1.0)
0
0
0
0
0
0
悪心
21(5.1)
16(4.0)
0
0
0
0
0
0
嘔吐
2(0.5)
2(0.5)
0
0
筋肉痛
122(29.9) 1(8.3)
97(24.3) 3(37.5)
2(0.5)
3(0.8)
N=解析対象例数、n=発現例数
a)Grade 0 以上の例数。Grade 0 は、紅斑、腫脹及び硬結(2.5cm 未満)並びに発熱(37.5~37.9℃)でのみ設定された。
b)37.5℃以上(腋窩体温)
7.R.3.2 注目すべき有害事象について
機構は、他の RNA ワクチンで注目すべき有害事象・副反応として懸念されているショック・アナフ
ィラキシー、心筋炎・心膜炎、VAED・VAERD 及びギラン・バレー症候群について提出された臨床試験
における発現状況について検討を行った。申請者は、以下のように説明している。
(1)ショック・アナフィラキシー
ARCT-154-01 試験でアナフィラキシー反応の重篤な有害事象は 2 例報告されたが、2 例とも Brighton
Collaboration のアナフィラキシーの定義を満たしていなかった。1 例は、4 歳女性、プラセボ-本剤群
の症例であり、本剤接種 1 日後に熱と下痢に加えて、疲労、全身の発赤、蕁麻疹、紅斑、両側性に大腿
と上腕の搔痒と丘疹を発症した。その後に被験者は COVID‐19 と診断された。経過から、アナフィラキ
シーではなく、過敏症反応と一致しており、COVID-19 感染とも関連している可能性があると考える。
もう 1 例は、4 歳女性、プラセボ-本剤群の症例であり、2 回目本剤接種から 190 日後にワクチン接種
38
コスタイベ筋注用_Meiji Seika ファルマ株式会社_審査報告書