会議資料 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00031.html |
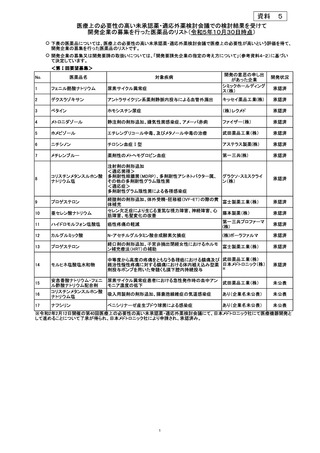
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第57回 ) |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
主要評価項目とされた、ベースラインから投与 24 カ月までの努力肺活量(forced vital
capacity、以下、
「FVC」
)の正常予測値に対する百分率(%)
(以下、
「%FVC」)の変化量[95%
信頼区間]は、MMF 群で 2.19[0.53, 3.84]、CYC 群で 2.88[1.19, 4.58]であり、2 群間で
統 計 学 的 な 有 意 な 差 は 認 め ら な か っ た ( p=0.24 、 robust joint model for
longitudinal measurements(Stat Med 2012; 31: 1707-21 18)))
。
被験薬投与との関連が予想され、試験実施計画書において予め有害事象発現時の対応が
規定されていた有害事象及び肺炎の発現状況は表 1 のとおりであった。重篤な有害事象は、
MMF 群 39%(27/69 例)
、CYC 群 30%(22/73 例)に認められ、そのうち MMF 群 3 例、
CYC 群 7 例については、被験薬との因果関係が否定されなかった。死亡は MMF 群 7%(5/69
例)、CYC 群 15%(11/73 例)に認められ、1 例を除く 15 例が SSc に起因するものと考えら
れた。死亡例のうち 3 例(MMF 群 1 例、CYC 群 2 例)は、被験薬の投与期間中に死亡し、
その他の死亡例(MMF 群 4 例、CYC 群 9 例)は他の理由で被験薬の投与を中止した 1~17
カ月後に死亡した。
表1
試験実施計画書において予め有害事象発現時の対応が規定されていた有害事象及び肺炎の発現状況
MMF 群(69 例)
CYC 群(73 例)
有害事象
件数
例数(%)
件数
例数(%)
貧血
18
8 (12%)
26
13 (18%)
肺炎
6
5 ( 7%)
4
4 ( 6%)
白血球減少症
5
4 ( 6%)
51
30 (41%)
好中球減少症
3
3 ( 4%)
7
5 ( 7%)
血尿
3
3 ( 4%)
2
2 ( 3%)
血小板減少症
0
0
7
4 ( 6%)
※2
主な組入れ基準:①Mahler Modified Dyspnea Index でグレード 2 以上の労作時呼吸困難を有する、②スクリ
ーニング時の%FVC が 45%以上 80%以下、かつベースライン時の%FVC が 45%以上 85%以下、③ベースライン
時の FVC がスクリーニング時の FVC の 10%以内、④SSc に起因すると判断される HRCT 上の所見を有する
2.
Tashkin DP et al. Improved cough and cough-specific quality of life in patients treated for
scleroderma-related interstitial lung disease: results of scleroderma lung study II. Chest 2017;
151: 813-20 19)
SLSⅡ試験 4)の成績から、MMF 及び CYC の SSc-ILD 患者における咳嗽に対する有効性
等について検討した。ベースライン時及び 24 カ月後の頻発する咳嗽を伴う患者の割合は、
それぞれ MMF 群で 63.2%(43/68 例)及び 46.2%(24/52 例)
、CYC 群で 60.3%(44/73 例)
及び 45.3%(24/53 例)であった。
安全性に係る記載はない。
3.
Volkmann ER et al. Mycophenolate mofetil versus placebo for systemic sclerosis-related
interstitial lung disease: an analysis of scleroderma lung studies I and II. Arthritis Rheumatol
2017; 69: 1451-60 15)
9
33 / 204