会議資料 (57 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00031.html |
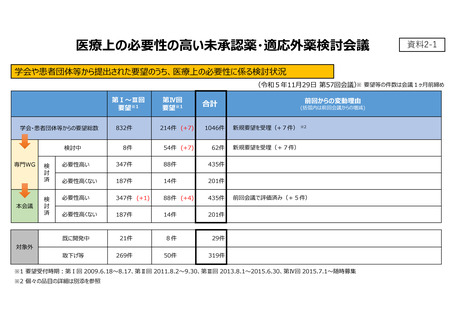
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第57回 ) |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
例)、重篤な有害事象は本剤群 5%(60/1251 例)及びプラセボ群 5%(67/1248 例)
、死亡は
本剤群 1%未満(1/1251 例)及びプラセボ群 1%未満(4/1248 例)
、投与中止例は本剤群 2%
(25/1251 例)及び 2%(27/1248 例)に認められた。
※2
主な選択基準:①出生時の性別が男性、②18 歳以上、③HIV-1 陰性、④HIV 感染のリスクが高い(以下の
いずれかを満たす:
(1)過去 6 カ月間に HIV 陽性の男性パートナー又は HIV 感染状況が不明な男性パートナ
ーとコンドームを使用しない肛門性交を行った、
(2)過去 6 カ月間に 4 名以上の男性パートナーと肛門性交
を行った、
(3)性感染症と診断されている、
(4)セックスワーカー)
3) Baeten JM et al. Antiretroviral Prophylaxis for HIV Prevention in Heterosexual Men and
Women. N Engl J Med 2012; 367: 399-410 6)
Partners-PrEP study:ケニア及びウガンダにおいて、一方が HIV 陽性、もう一方が HIV 陰
性の男女のカップルを対象に、HIV 感染の曝露前予防効果におけるテノホビル ジソプロキ
シルフマル酸塩(以下、
「TDF」)300 mg 又は本剤のプラセボに対する優越性を確認するこ
とを目的とした無作為化二重盲検並行群間比較試験が実施された。
被験者は、TDF 300 mg を 1 日 1 回経口投与する群(以下、
「TDF 群」)
、本剤群及びプラ
セボ群の 3 群に無作為に割り付けられた。無作為化された男女のカップル 4758 組(TDF 群
1589 組、本剤群 1583 組及びプラセボ群 1586 組)のうち、組入れ時に一方が HIV 陰性で無
作為化後 1 回以上 HIV 検査を受けた 4708 組(TDF 群 1572 組、本剤群 1568 組及びプラセ
ボ群 1568 組)が主要な有効性解析対象集団とされた。
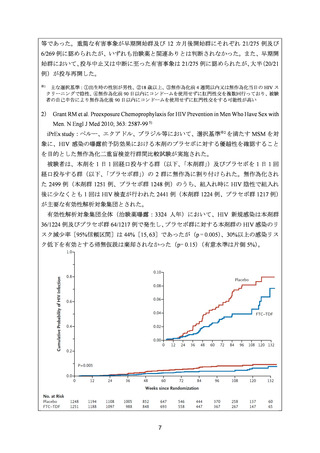
有効性解析対象集団(治験薬曝露:7830 人年)では無作為化後に 82 例の HIV-1 新規感
染が発生し、100 人年あたりの HIV-1 新規感染は TDF 群で 0.65 例、本剤群で 0.50 例、プラ
セボ群で 1.99 例であり、プラセボ群に対する本剤群の HIV-1 感染のリスク減少率[95%信
頼区間]は、75%[55, 87]
(p < 0.001)であった。また、女性及び男性において、プラセボ
群と比較した本剤群での HIV-1 感染の相対リスク減少率は、それぞれ 66%(p=0.005)及び
84%(p < 0.001)であった(Cox 比例ハザードモデル)
。
8
57 / 204