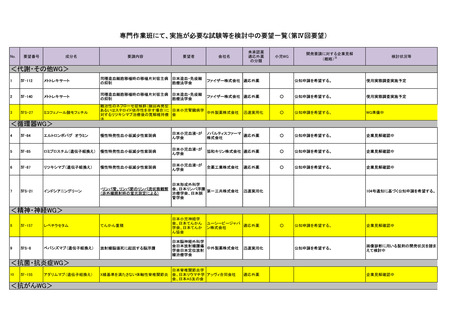
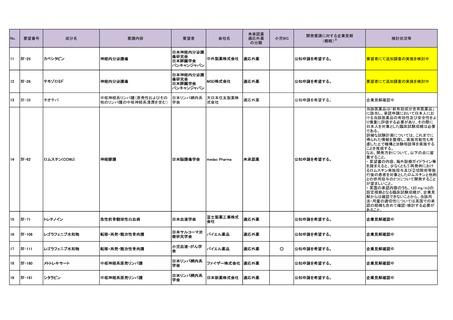
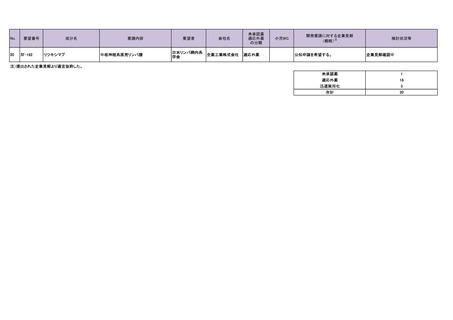
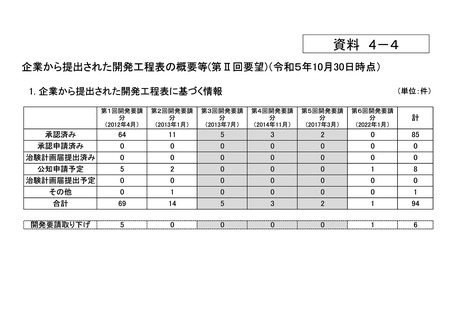
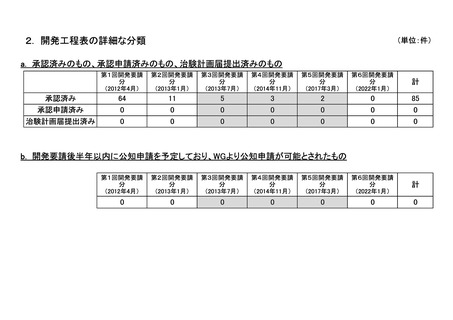
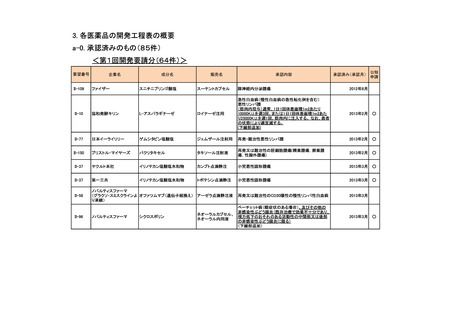
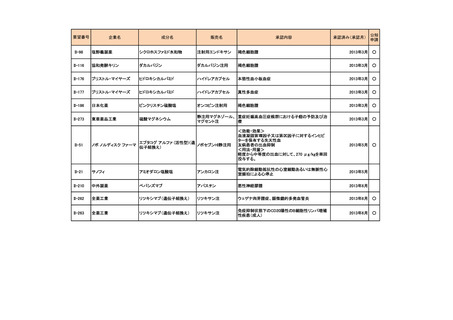
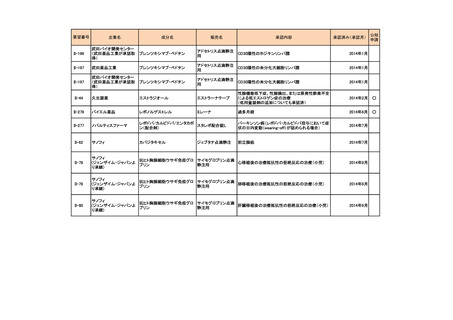
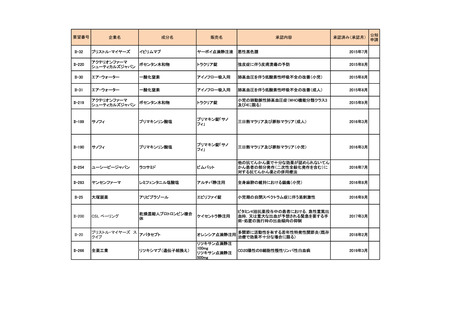
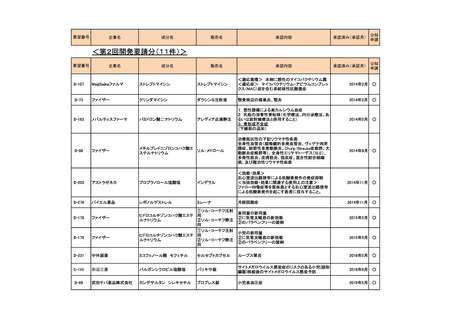
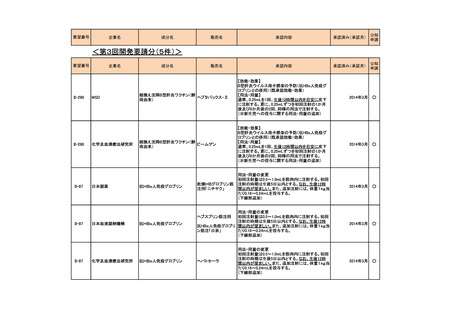
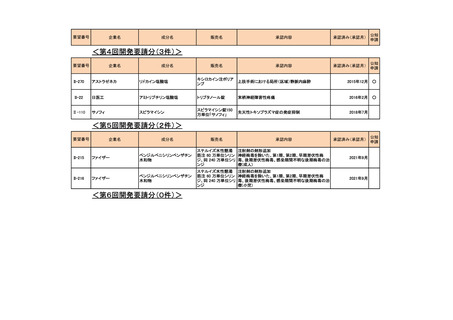
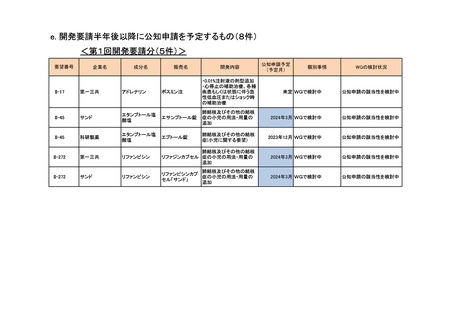
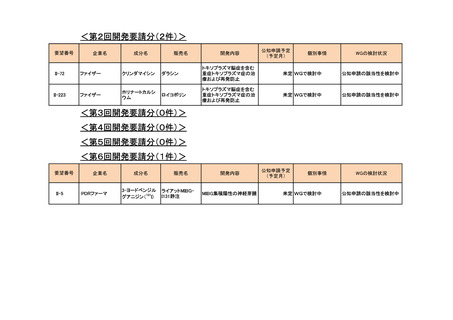
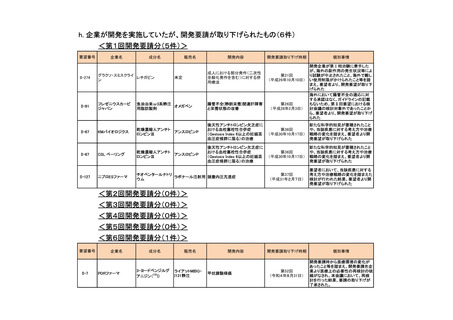
会議資料 (54 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00031.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第57回 ) |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
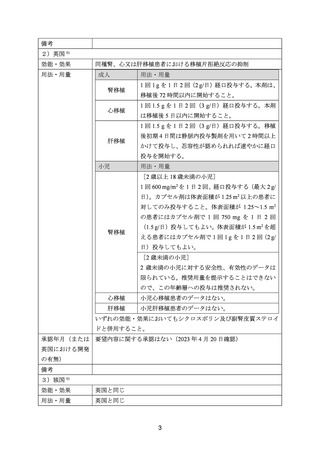
用法・用量
HIV-1 感染症の治療の推奨用量
本剤の推奨用量は、1 日 1 回 1 錠(TDF 300 mg 及び FTC 200 mg 含
有)経口投与。テノホビルの吸収を最適化するため、本剤は食事と
ともに服用することが推奨される。
PrEP の推奨用量
本剤は、HIV-1 陰性の成人に 1 日 1 回 1 錠(TDF 300 mg 及び FTC
200 mg 含有)を経口投与。テノホビルの吸収を最適化するため、本
剤は食事とともに服用することが推奨される。
承認年月(または豪 PrEP に対する適応:2016 年 5 月
州における開発の有
無)
備考
当該品目の本効能・効果の承認時は保険償還されていたが、2020 年
4 月に Gilead Sciences Pty Ltd からの申し出により保険償還の対象外
となった。
4.要望内容について企業側で実施した海外臨床試験成績について
企業により実施された海外臨床試験はない
5.要望内容に係る国内外の公表文献・成書等について
(1)無作為化比較試験、薬物動態試験等の公表論文としての報告状況
<文献の検索方法(検索式や検索時期等)
、検索結果、文献等の選定理由の概略等>
HIV 感染症の曝露前予防として本剤を 1 日 1 回経口投与した臨床試験について、米国ガ
イドライン 2)及び/又は英国ガイドライン 3)で引用された海外臨床試験 5 試験及び国内で実
施された国内臨床試験 1 試験に関する文献報告計 6 報 4), 5), 6), 7)~9)が選択された。なお、この
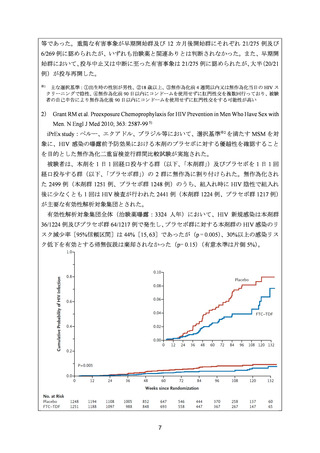
うち海外臨床試験 2 試験 7), 8)では本剤による HIV 感染症の曝露前予防に対する有効性は認
められなかったが、有効性とアドヒアランスには相関があることが報告されており 10)、当
該 2 試験の内服遵守率が低かったことが原因と考察されている。
5
54 / 204