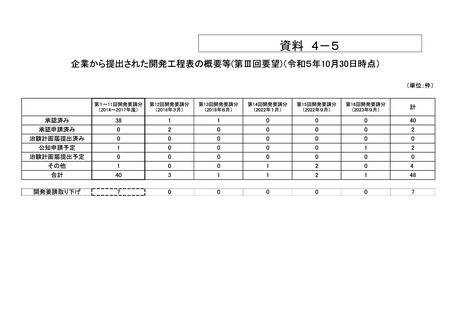
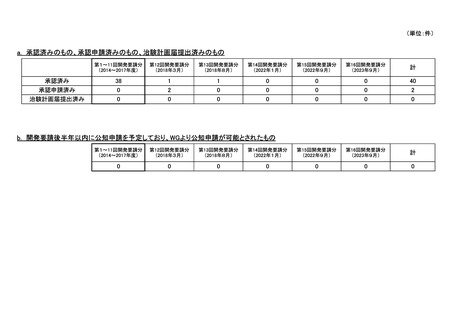
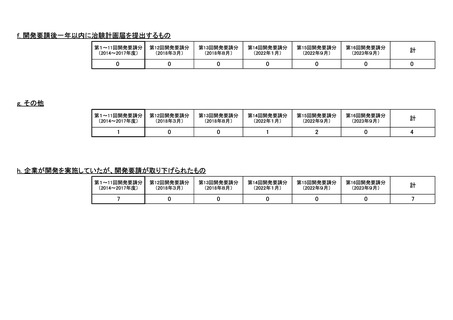
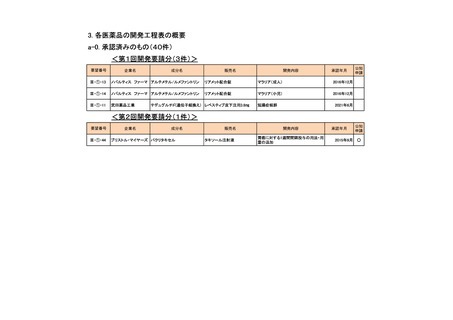
会議資料 (74 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00031.html |
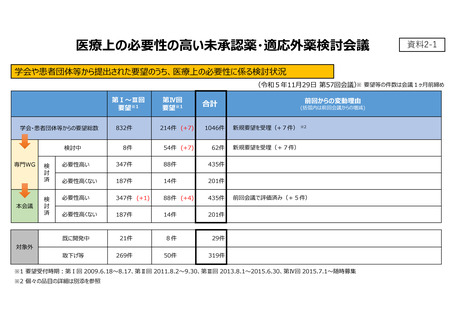
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第57回 ) |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Ann Oncol 2011; 22: 636-42 6)
②
Gynecol Oncol 2012; 125: 771 [abstract] 3)
Gynecol Oncol 2012; 127: 321-5 7)
Gynecol Oncol 2005; 99: 557-63 8)
備考
2)英国
ガイドライン名
① ESMO-ESGO-ESTRO Consensus Conference on Endometrial Cancer:
diagnosis, treatment and follow-up9)
② ESGO/ESTRO/ESP guidelines for the management of patients with
endometrial carcinoma10)
効能・効果
① 進行・再発の子宮体癌
(または効能・効果に関
② 進行・再発の子宮体癌
連のある記載箇所)
用法・用量
① カルボプラチン AUC 6 mg・min/mL 相当量*及びパクリタキセル
175 mg/m2、3 週間ごと、6 サイクル
(または用法・用量に関
連のある記載箇所)
② カルボプラチン AUC 5~6 mg・min/mL 相当量*及びパクリタキ
セル 175 mg/m2、3 週間ごと、6 サイクル
*:医療上の必要性の高い未承認薬・適応外薬検討会議 公知申請への該当性に
係る報告書:カルボプラチン(乳癌)において、海外で用いられている AUC
6 mg・min/mL 相当量について、本邦で実施した製造販売後特別調査(AUC 値
に基づく投与における安全性と有効性を確認するために実施された調査)に
おいて、15 例のほとんどが既承認の用量の範囲内(1 回 300~400 mg/m2)に
収まっていた旨が記載されており、要望された用量(1 回 300~400 mg/m2 投
与)は、海外で推奨されている用量(AUC 5~6 mg・min/mL 相当量)と同様
と考えられる。
ガイドラインの根拠
①
論文
Gynecol Oncol 2012; 125: 771 [abstract] 3)
②
Gynecol Oncol 2012; 125: 771 [abstract] 3)
Lancet Oncol 2019; 20: 1273-85 11)
N Engl J Med 2019; 380: 2317-26 12)
備考
3)独国
ガイドライン名
英国と同様
効能・効果
英国と同様
(または効能・効果に関
連のある記載箇所)
用法・用量
英国と同様
4
74 / 204