○診療報酬改定結果検証部会からの報告について 総-1-5-2 (263 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00222.html |
| 出典情報 | 中央社会保険医療協議会 総会(第563回 11/10)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
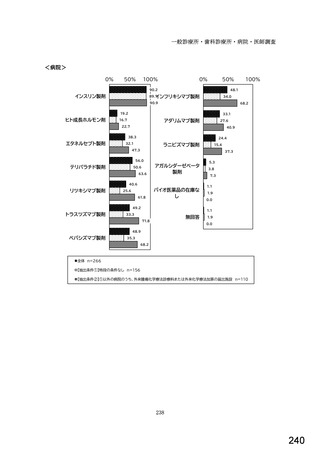
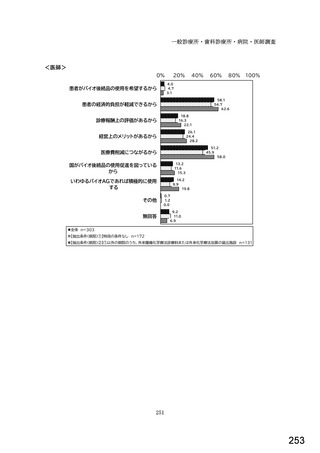
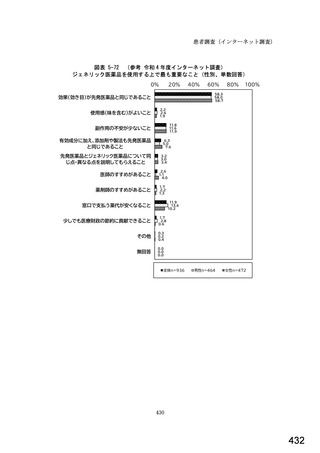
<医師>
0%
20%
40%
60%
80%
100%
44.3
44.6
43.9
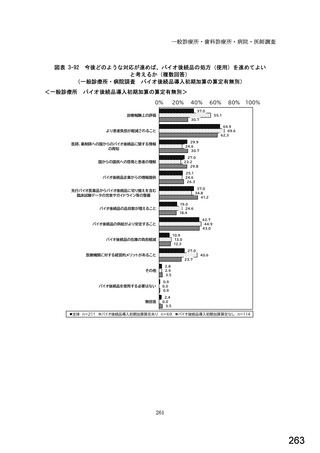
診療報酬上の評価
49.1
46.8
52.4
より患者負担が軽減されること
37.5
40.3
33.5
医師、薬剤師への国からのバイオ後続品に関する情報
の周知
33.5
32.2
35.4
国からの国民への啓発と患者の理解
18.4
21.0
14.6
バイオ後続品企業からの情報提供
38.3
35.2
42.7
先行バイオ医薬品からバイオ後続品に切り替えを含む
臨床試験データの充実やガイドライン等の整備
14.9
14.2
15.9
バイオ後続品の品目数が増えること
37.3
33.0
43.3
バイオ後続品の供給がより安定すること
9.8
10.3
9.1
バイオ後続品の在庫の負担軽減
28.2
25.8
31.7
医療機関に対する経営的メリットがあること
その他
2.0
1.7
2.4
バイオ後続品を使用する必要はない
1.3
1.7
0.6
無回答
0.5
0.9
0.0
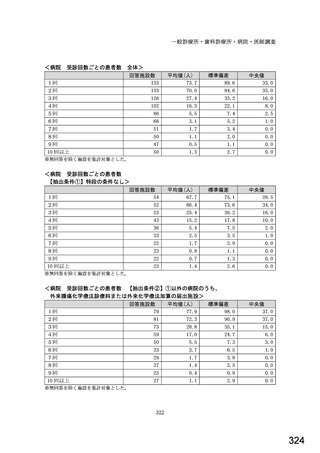
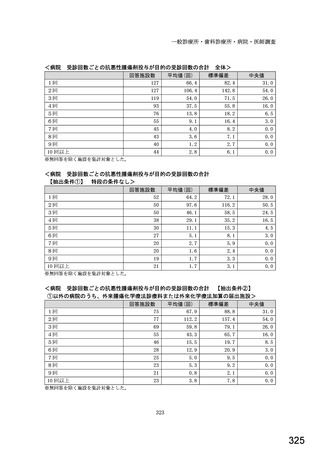
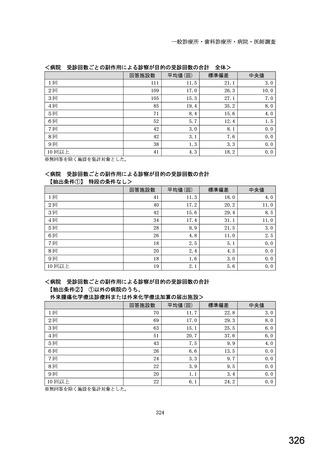
全体 n=397
【抽出条件(病院)①】特段の条件なし n=233
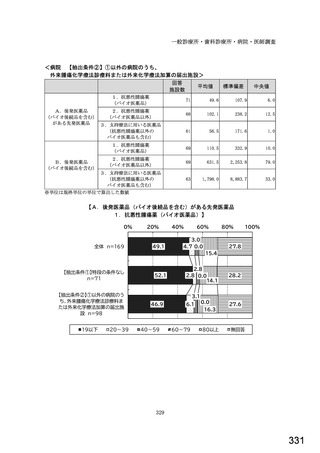
【抽出条件(病院)②】①以外の病院のうち、外来腫瘍化学療法診療料または外来化学療法加算の届出施設 n=164
260
262