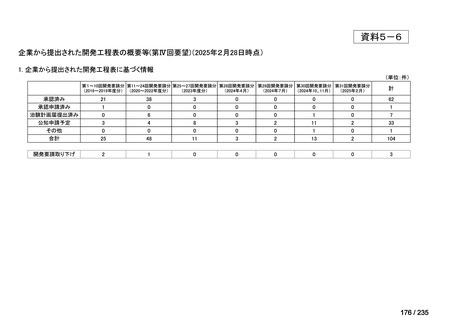
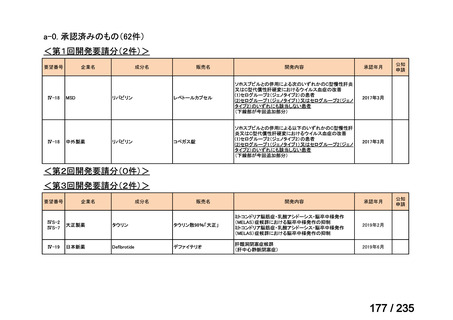
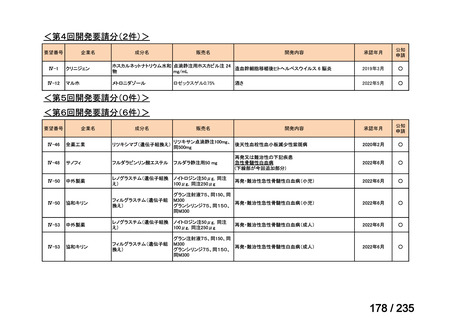
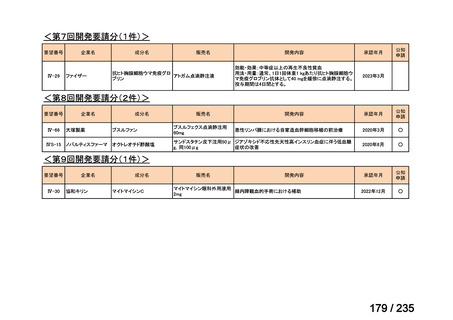
会議資料 (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00036.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第62回 3/13)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
<海外における臨床試験>
1) H. C. Maltezou et al、Piperacillin/Tazobactam Versus Cefotaxime Plus Metronidazole for
Treatment of Children with Intra-Abdominal Infections Requiring Surgery、Eur J Clin Microbiol
Infect Dis 2001; 20: 643-6 6)
腹腔内感染症が疑われ、手術を要する 0~14 歳の小児患者※1 を対象に、本薬+セフォタ
キシム(以下、
「CTX」)併用又はピペラシリン(以下、
「PIPC」)/タゾバクタム(以下、
「TAZ」)
投与時の有効性及び安全性を検討する無作為化二重盲検試験が実施された。
用法・用量は、本薬 7.5 mg/kg+CTX 50 mg/kg 又は PIPC 100 mg/kg/TAZ 12.5 mg/kg を 8 時
間毎に 5~14 日間静脈内投与することとされた。
無作為化された 70 例(本薬+CTX 群:35 例、PIPC/TAZ 群:35 例)のうち、アレルギー
性皮膚反応のため投与中止に至った 1 例(本薬+CTX 群)を除いた 69 例で臨床効果が評
価され、そのうち、感染部位からの病原体分離ができなかった 8 例を除いた 61 例(本薬+
CTX 群:31 例、PIPC/TAZ 群:30 例)で微生物学的効果が評価された。
有効性について、臨床効果の有効率は、本薬+CTX 群 100%(34/34 例)及び PIPC/TAZ
群 100%(35/35 例)、微生物学的効果の有効率は、本薬+CTX 群 100%(31/31 例)及び
PIPC/TAZ 群 97%(29/30 例)であった。
安全性について、本薬+CTX 群の 1 例において、試験薬との因果関係ありと判断された
中等度のアレルギー性皮膚反応により投与中止に至ったが、その他の被験者の忍容性は良
好であった。
※1
実際に組入れられた患者の年齢範囲は 2.5-14 歳であった。
2) Carl-Christian A. Jackson et al 、 Safety and Efficacy of Ceftolozane/Tazobactam Plus
Metronidazole Versus Meropenem From a Phase 2, Randomized Clinical Trial in Pediatric
Participants With Complicated Intra-Abdominal Infection、Pediatr Infect Dis J 2023; 42: 55762 7)
複雑性腹腔内感染症(以下、「cIAI」)と診断され、手術を要する生後 7 日齢以上 18 歳
未満の小児患者を対象に、セフトロザン(以下、「CTLZ」)/TAZ+本薬併用又はメロペネ
ム(以下、「MEPM」)投与時の有効性及び安全性を検討する無作為化二重盲検試験が実施
された。
用法・用量は、表 1 のとおりとされた。
表1
年齢区分別の CTLZ/TAZ、本薬及び MEPM の用法・用量
CTLZ/TAZ+本薬
CTLZ 1 g/TAZ 0.5 g+本薬 10 mg/kg を 8 時間毎
に 5~14 日間、静脈内投与
MEPM
6 歳以上 12 歳未満
2 歳以上 6 歳未満
3 カ月齢以上 2 歳未満
CTLZ 20 mg/kg/TAZ 10 mg/kg+本薬 10 mg/kg
を 8 時間毎に 5~14 日間、静脈内投与
MEPM 20 mg/kg を 8 時間毎に 5~14 日間、
静脈内投与
7 日齢以上 3 カ月齢未満
CTLZ 20 mg/kg/TAZ 10 mg/kg+本薬 10~15
mg/kg を 8 時間毎に 5~14 日間、静脈内投与
年齢
12 歳以上 18 歳未満
11
40 / 235