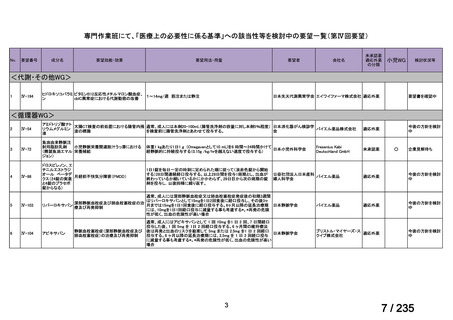
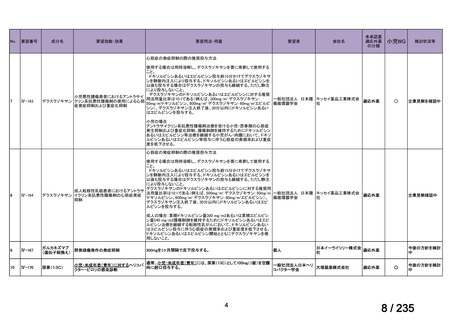
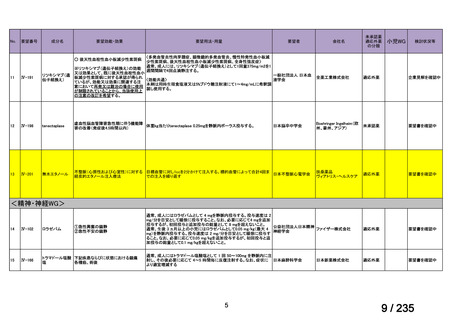
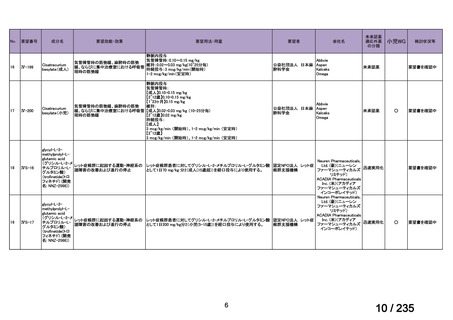
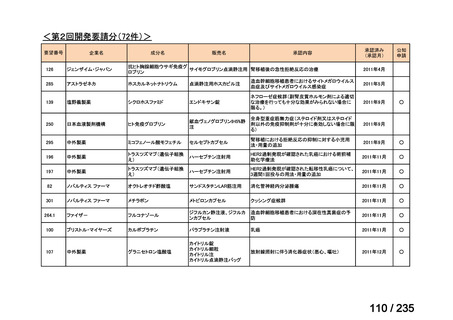
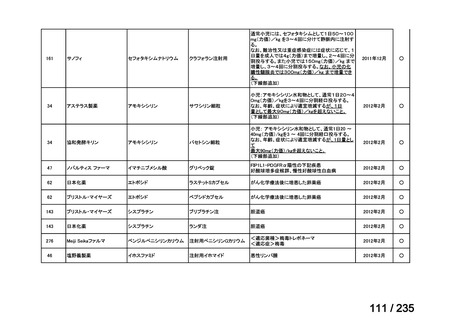
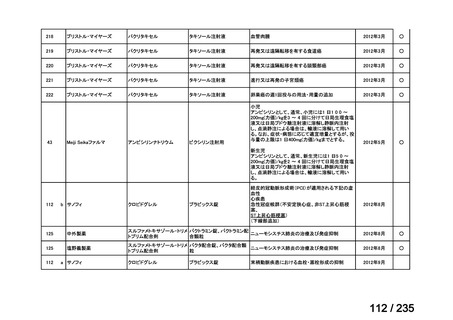
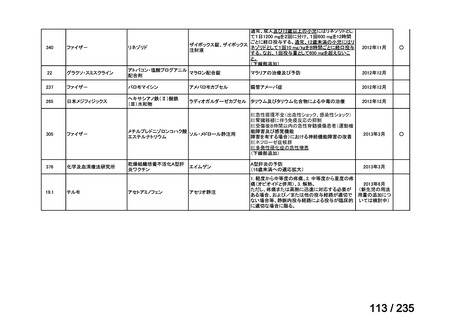
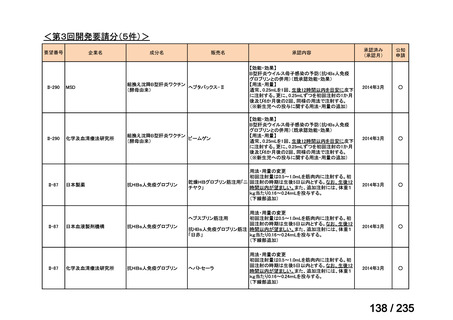
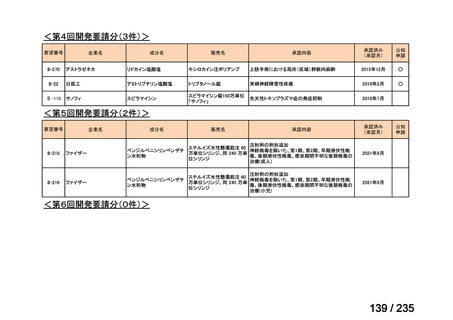
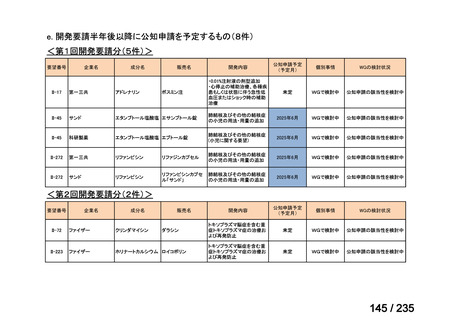
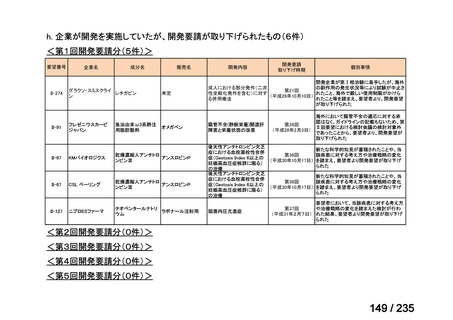
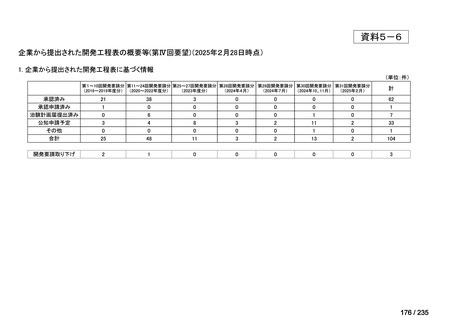
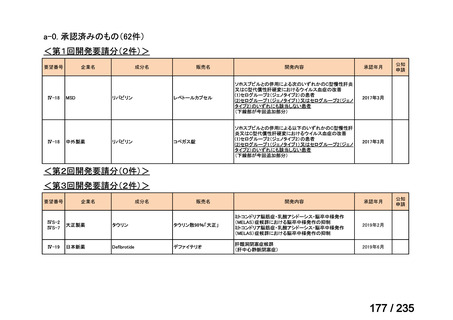
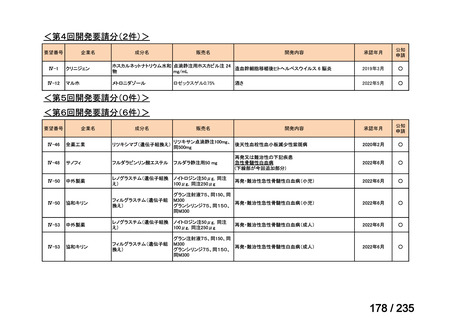
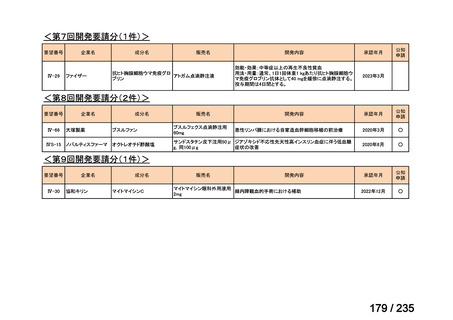
会議資料 (59 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00036.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第62回 3/13)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
効能・効果
該当なし
用法・用量
-
承認年月(または豪 開発の有無:不明
州における開発の有
無)
備考
-
(2) 欧米等6カ国での標準的使用状況について
1)米国
ガイドライン名
Neuroblastoma Treatment (PDQ®)–Health Professional Version (Updated:
April 30, 2024) 5)
効能・効果
再発又は難治性の高リスク神経芽腫
(または効能・効果に関
連のある記載箇所)
用法・用量
131
I-MIBG 単独投与又は他の抗悪性腫瘍薬との併用投与。131I-MIBG
(または用法・用量に関
治療に続いて幹細胞移植を実施する。
連のある記載箇所)
ガイドライン中に具体的な投与量は示されていない。ガイドライン
の根拠論文に記載されている用法・用量をそれぞれ【】内に示す。
ガイドラインの根拠
DuBois SG, et al.: Phase I Study of Vorinostat as a Radiation Sensitizer
論文
with
131
I-Metaiodobenzylguanidine (131I-MIBG) for Patients with
Relapsed or Refractory Neuroblastoma. Clin Cancer Res 2015; 21: 271521 6)
【131I-MIBG 296,444,555 又は 666 MBq/kg を投与(Day 3)。ボリ
ノスタット(Day 1~14)及び幹細胞移植(Day 17)を併用】
Polishchuk AL, et al.: Response, survival, and toxicity after iodine-131metaiodobenzylguanidine therapy for neuroblastoma in preadolescents,
adolescents, and adults. Cancer 2011; 117: 4286-93 7)
【1 回あたりの投与量の中央値 440.3 MBq/kg(96.2~688.2 MBq/kg)
、
累積投与量の中央値 658.6 MBq/kg(233.1~1343.1 MBq/kg)、投与回
数 1~4】
Matthay KK, et al.: Phase II study on the effect of disease sites, age, and
prior therapy on response to iodine-131-metaiodobenzylguanidine therapy
in refractory neuroblastoma. J Clin Oncol 2007 25: 1054-60.8)
【 幹 細 胞 移 植 併 用 の 場 合 は 666 MBq/kg 、 未 併 用 の 場 合 は
444 MBq/kg】
Matthay KK, et al.: Phase I dose escalation of iodine-1314
59 / 235