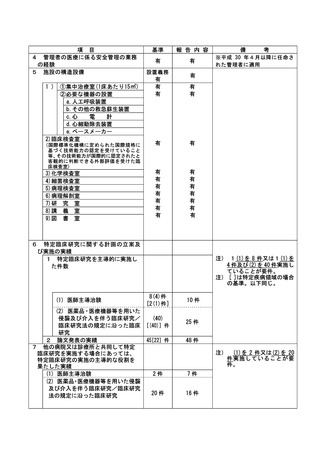
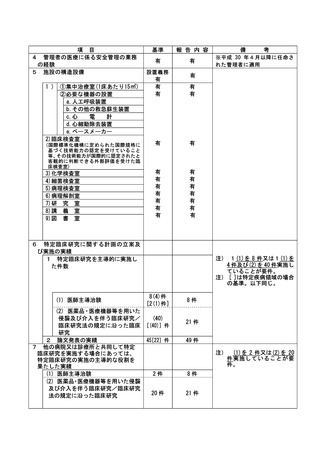
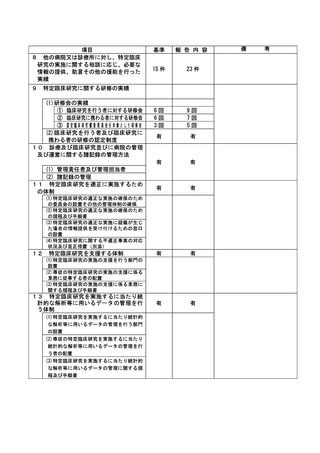
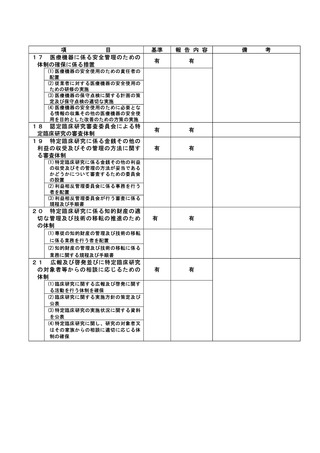
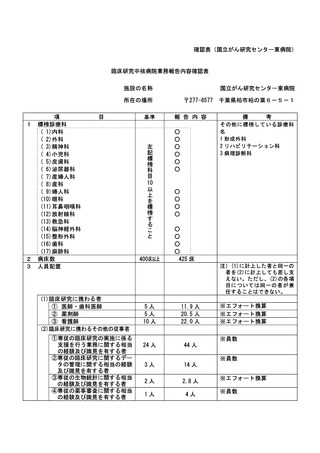
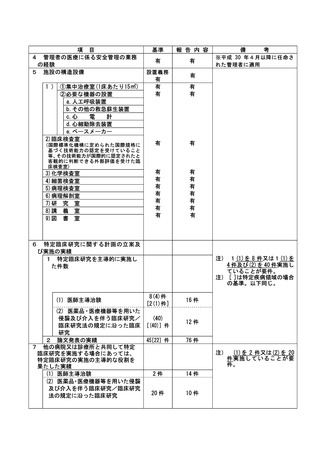
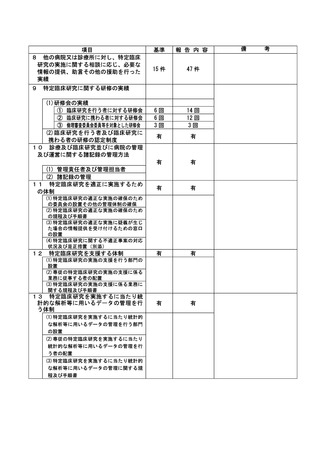
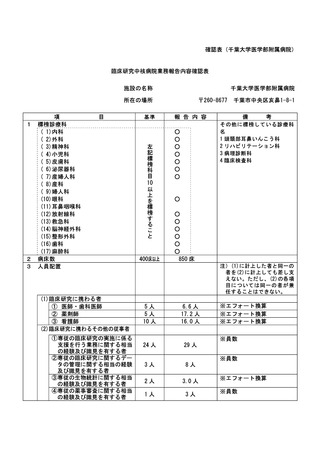
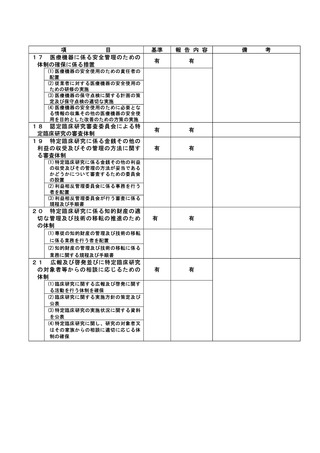
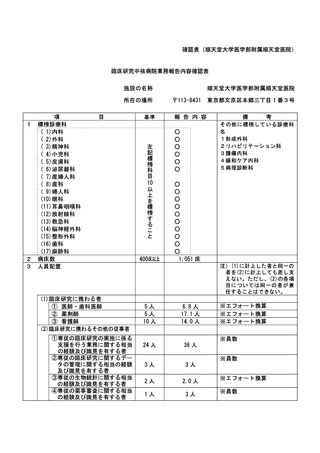
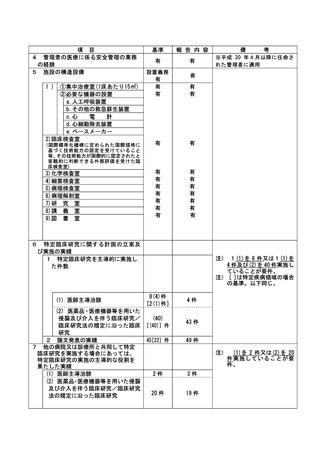
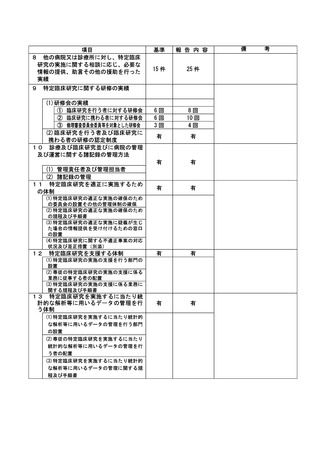
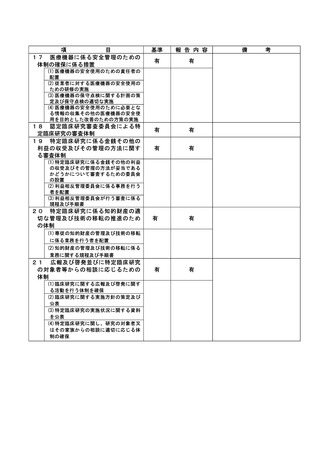
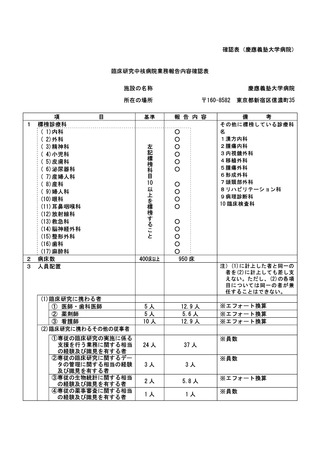
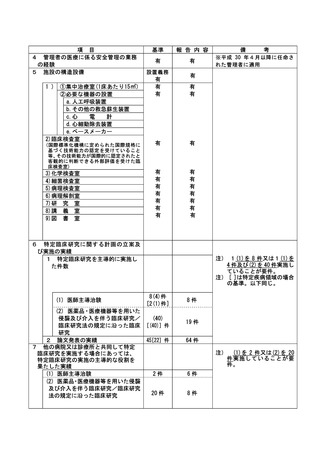
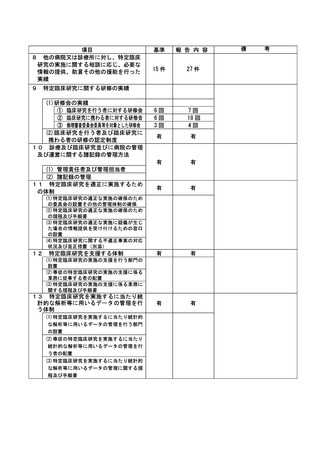
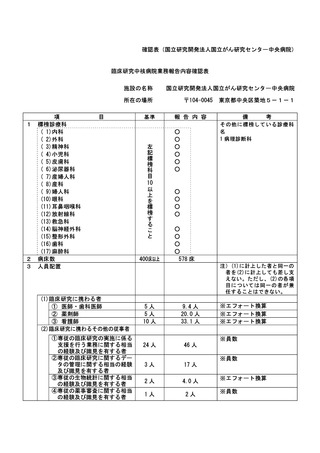
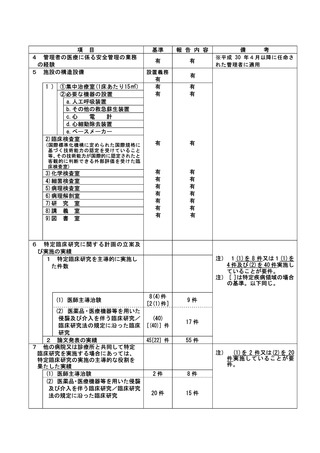
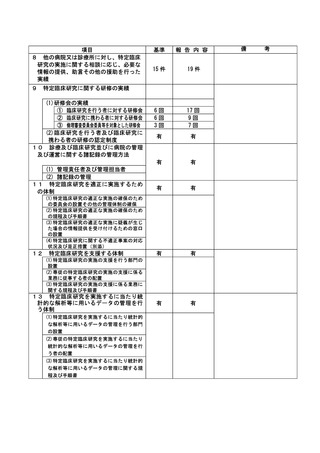
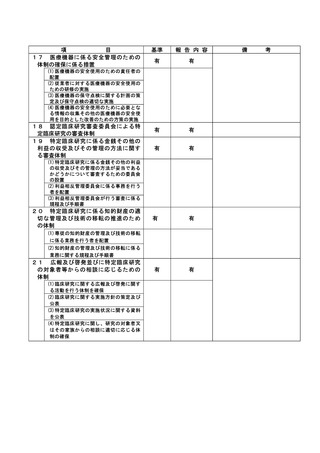
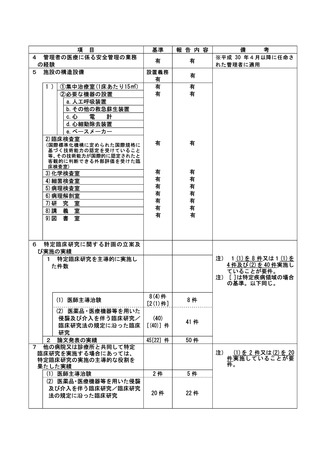
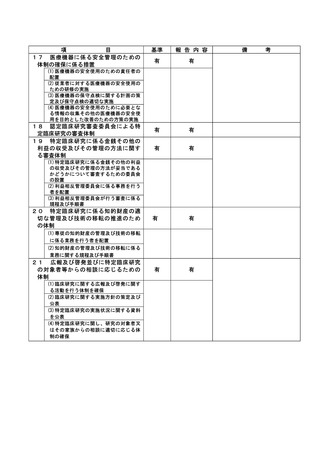
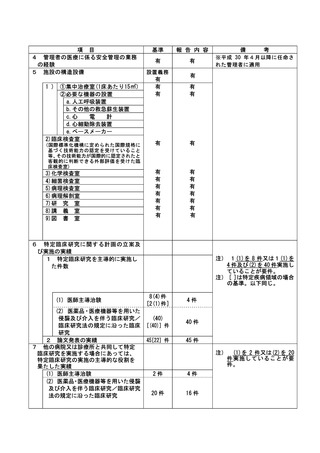
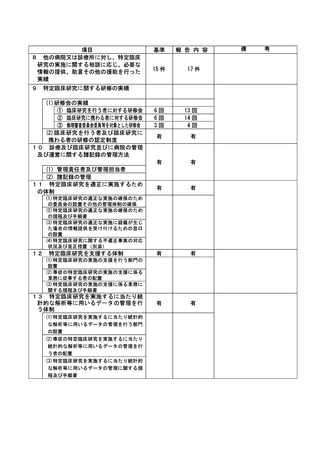
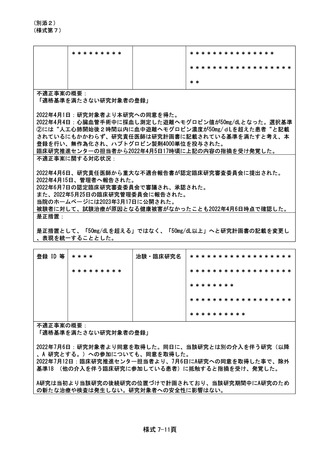
資料2:臨床研究中核病院業務報告内容確認表 (102 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
無の記載がされていなことを発見した。新 PM から担当 CRA 及び治験調整事務局に確認を行い、次回
SDV 時に担当 CRA がカルテを再確認することとなった。
2022/6/29 SDV を実施し、上記該当症例において、6 分間歩行検査実施前の Borg スケールおよび
靴、補助具の有無について記載されていないことを担当 CRA が確認した。未記載の項目について、
記録漏れか、実施漏れか、担当 CRA より治験分担医師へ確認することとなった。
2022/8/23 担当 CRA と治験分担医師が Web 面会を実施した。6 分間歩行検査実施前の Borg スケー
ルおよび靴、補助具の有無については、記録漏れか、実施漏れか特定することは難しいと判断さ
れ、すべて逸脱として扱うこととなった。
不適正事案に関する対応状況:
本治験の実施体制について改めて確認を行い、逸脱した理由として、治験分担医師の GCP および治
験実施計画書の理解不足ならびに遵守意識不足、6 分間歩行検査実施体制の整備不足、治験関係者
との情報共有や協力体制構築に対する、前任の PM および治験分担医師の理解不足が挙げられた。
逸脱判明後、該当症例のカルテの確認を行い、被験者の安全性に問題は発生していないことを確認
した。
是正措置:
新 PM および責任医師より治験分担医師(6 分間歩行検査実施者を含む)へ、治験実施計画書の再確
認を指示した。
6 分間歩行検査前に、治験分担医師より 6 分間歩行検査実施者へ記入項目の周知をメールにて行
う。また、検査施行後、6 分間歩行検査実施者以外の治験分担医師が、記録漏れがないか確認す
る。
2022 年 4 月に PM 交代があり、現 PM によるレビュー中に判明した事案であり、今後現 PM 下でより
一層の体制強化を図る。併せて、治験分担医師等に対して、GCP および治験実施計画書の遵守、治
験関係者との関係構築の重要性などについて今後も継続的に教育を行う。
登録 ID 等
*******
治験名
******************
******************
******************
不適正事案の概要:旧版の同意説明文書による文書同意取得
プレスクリーニング開始前の同意説明時に最新版(第 4 版)を使用せず、第 3 版にて文書同意を取
得した。経緯は、IRB にて、第 4 版が 3/22 に承認していたが、CRC は、3/22 に ICF が改訂されてい
たことを失念していた。被験者 A に 3/28 に第 3 版にて文書同意取得、被験者 B に 3/29 に第 3 版に
て文書同意取得、4/8 に第 4 版から第 5 版の改訂(個人情報保護法改訂に関する変更)について PI
確認。4/19 に CRA に最新版の ICF を依頼し、第 3 版を受領。最新版は第 4 版だったが、確認しない
まま ICF を受領していた。4/19 被験者 B へ第 4 版から第 5 版の変更点を説明口頭にて継続の意思を
確認。4/19 に本来なら IRB 承認された第 4 版を受領していなければいけないことに 4/26 に担当
CRC が気づき、本事象が発覚した。4/26IRB にて第 5 版が承認。
不適正事案に関する対応状況:
発覚後すぐに依頼者へ経緯を説明し、被験者の試験の進捗状況はプレスクリーニング検査中である
が、継続に問題ないことを確認した。5/17 被験者 B へ、本来なら 3/29 に第 4 版で同意説明を行わ
なければならなかったが、説明した同意書は第 3 版であったこと、また 4/19 に説明していたのは、
第 4 版→第 5 版の変更点であったことを伝え、これらを整理し、第 3 版→第 4 版の変更点をお伝え
し、最新版の ICF 第 5 版の説明を行い、同意書に署名をいただき、同意取得になった。被験者 A に
様式第 7-9
101