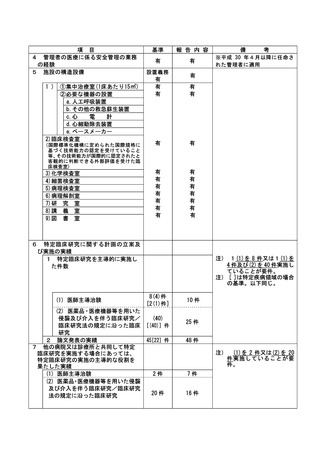
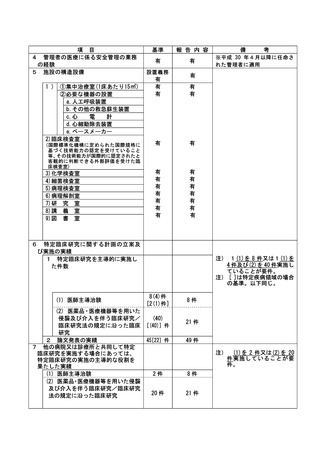
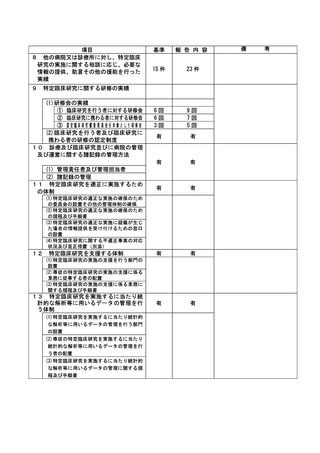
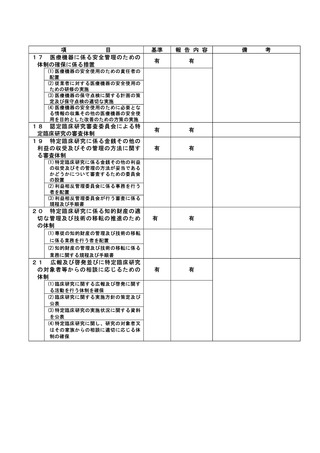
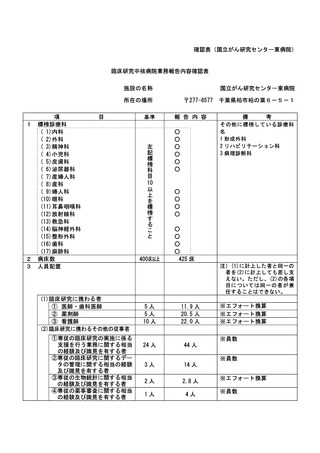
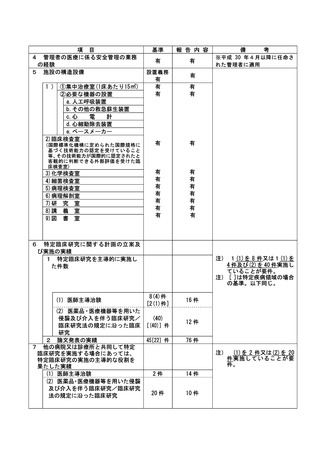
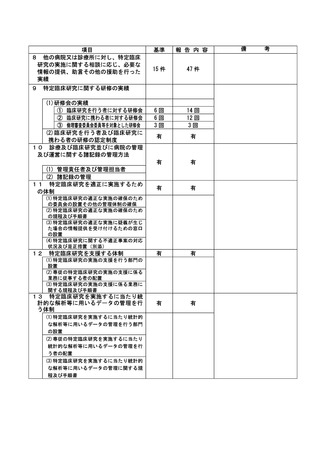
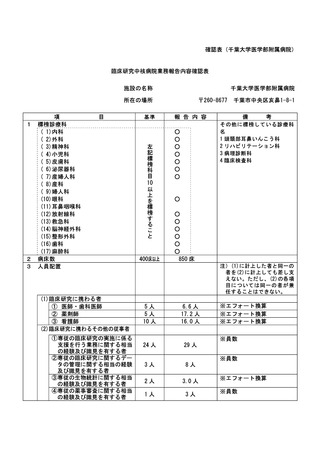
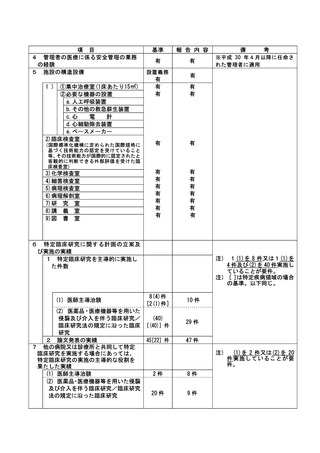
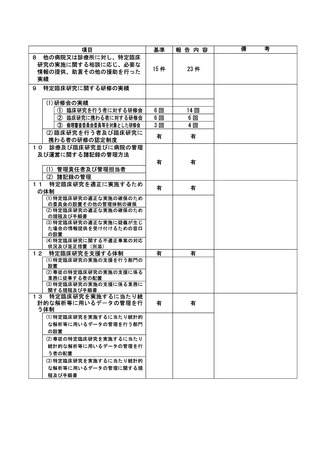
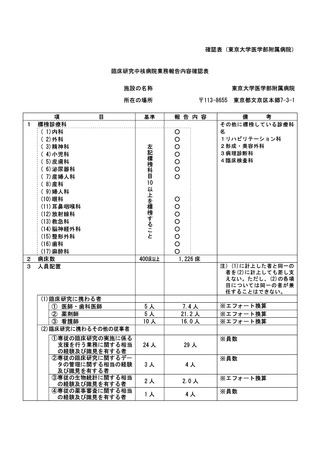
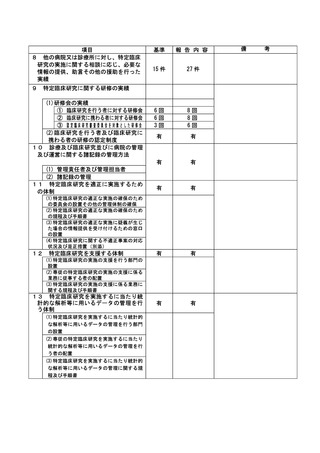
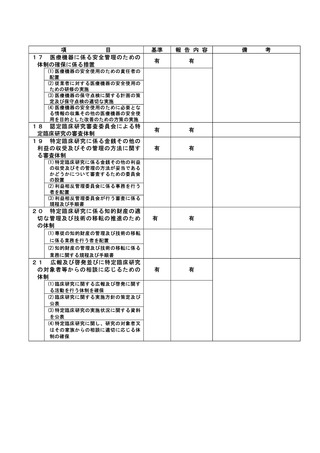
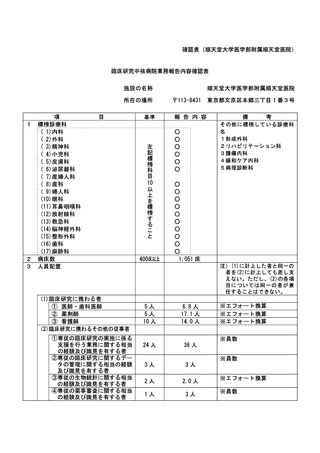
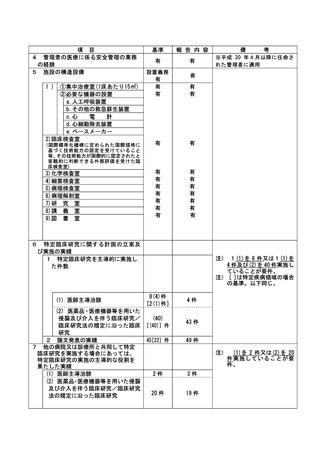
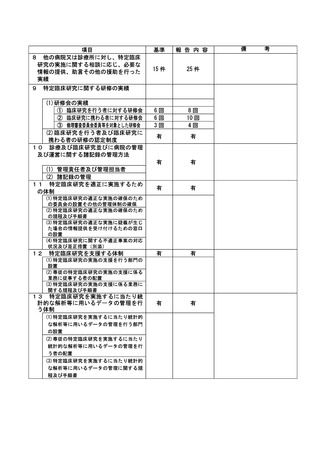
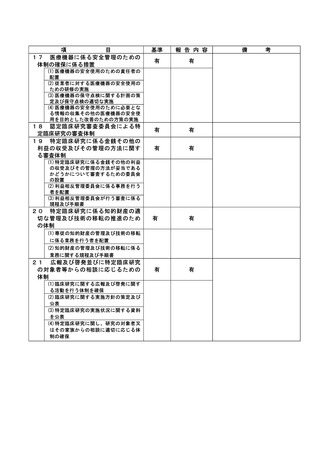
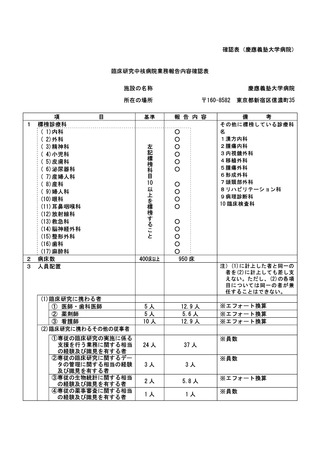
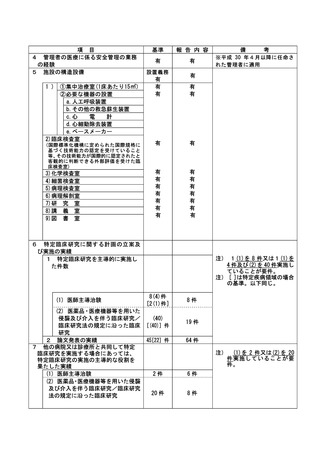
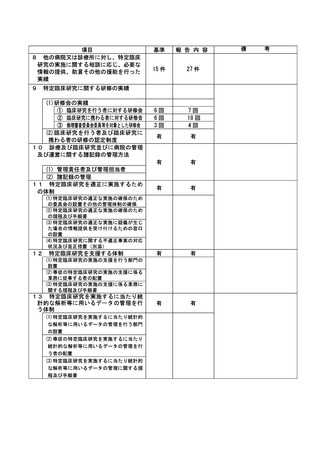
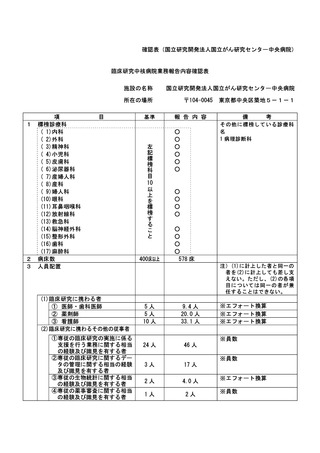
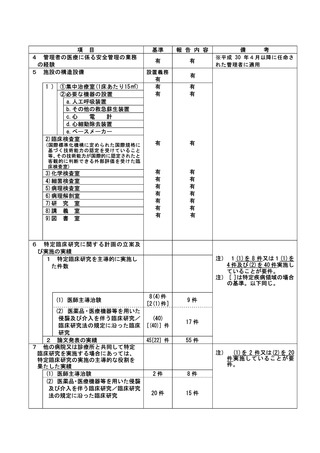
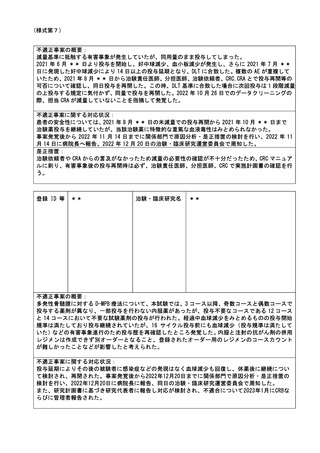
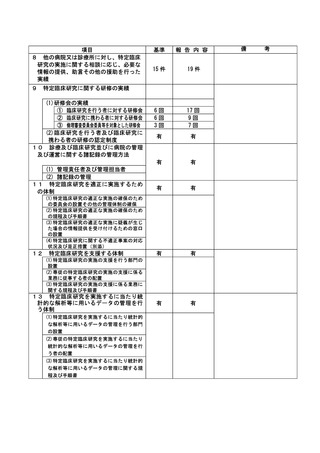
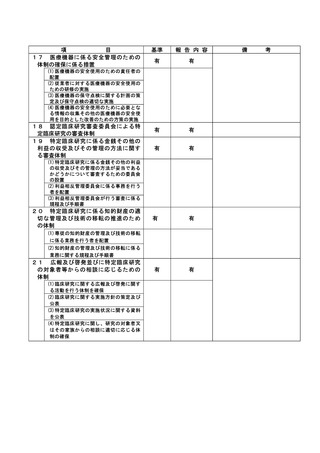
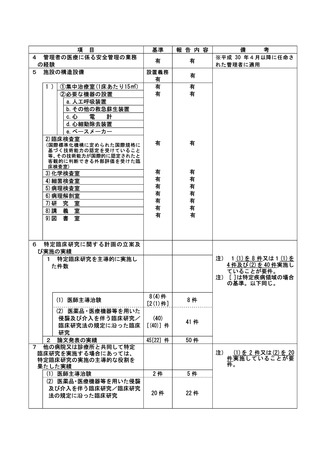
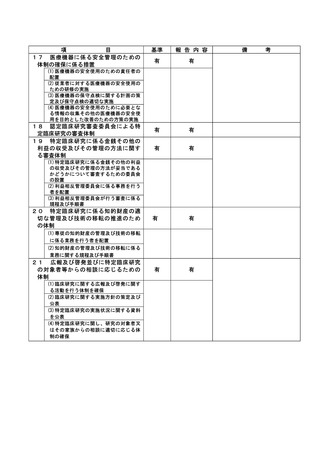
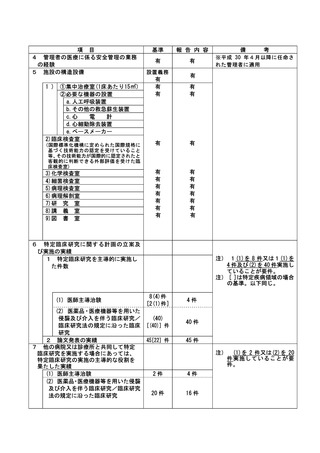
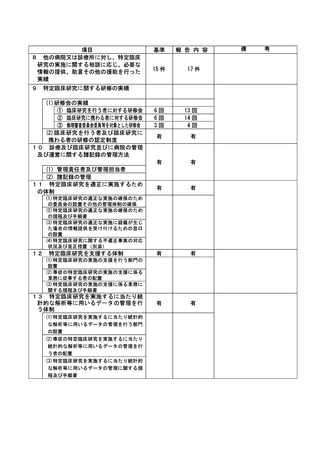
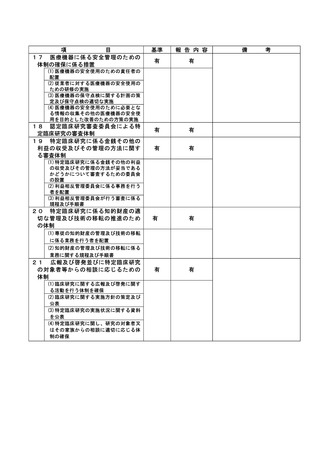
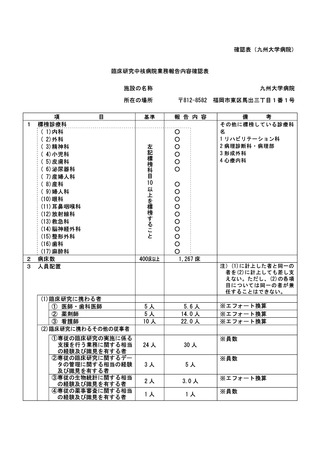
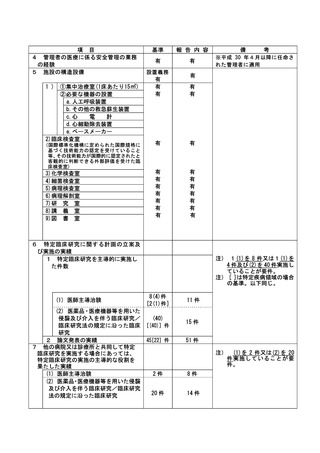
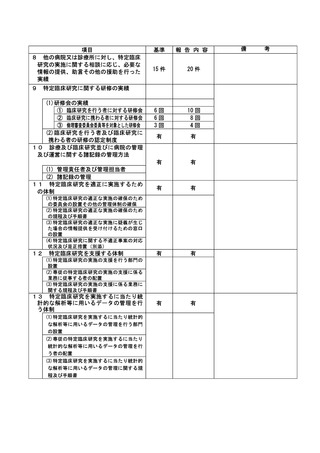
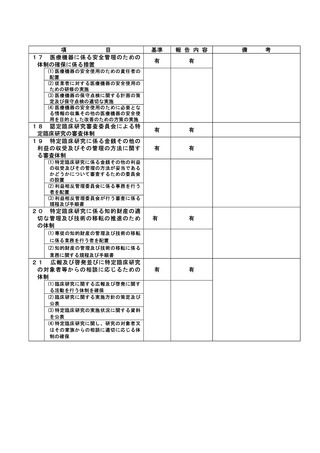
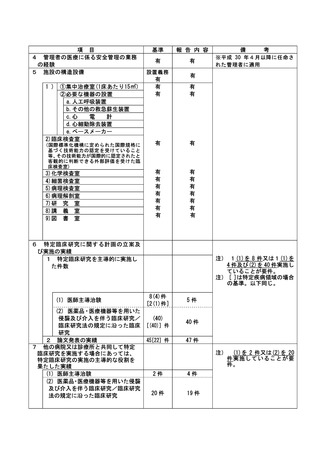
資料2:臨床研究中核病院業務報告内容確認表 (109 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2023/2/9
2023/3/8
2023/3/29
ること、厚労省の先進医療技術審査部会に観察研究の結果、本件の再発防止策の実施
状況について報告予定であることが報告された。
研究監視指導員より、特段問題ないことが報告された。
第 145 回先進医療技術審査部会
中止後の被験者保護のための観察研究結果についての報告について、報告され、特に
意見等はなかった。
阪大病院観察研究等倫理審査委員会
終了報告として報告された。
総括委員会開催・報告
研究監視指導について 2 年経過し、問題ないことから指導については終了する旨了承
された。
是正措置:
先進医療会議、先進医療会議先進医療技術審査部会、厚生科学審議会臨床研究部会宛てに、2021 年
2 月 12 日、以下の報告書を提出した。その後の、中止後の被験者保護および再発防止策の進捗状況
を記載する。
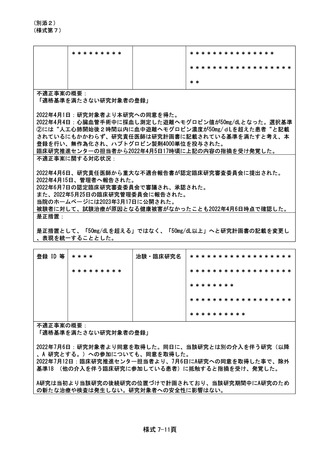
研究活動上の特定不正行為ならびに特定臨床研究「*********************
*********」(******)の先進医療取り下げに関する報告
①研究活動により得られたデータの共有、保存に関する組織としての体制整備
2016 年 8 月より、医学系研究科及び医学部附属病院では、チェック事項を細かく定め、論文に使
用した図表写真等の元データを責任著者が確認の上、バックアップデータを保管する体制を整備し
ている。しかし、筆頭著者が責任著者を兼ねていたことから、責任著者にかわり共著者が確認し署
名するよう「医学部附属病院における原著論文の確認に関する申合せ」を改訂し、2021 年 7 月 1 日
以降に投稿される論文より、本改訂に則り運用を開始した。また、その実効性担保は、年 1 回、研
究倫理教育副責任者が確認し、かつ医学系研究科長および医学部附属病院長に報告するとしてお
り、2021 年度は、7 月 29 日に医学系研究科長及び医学部附属病院長から各教室主任、各診療科長等
に通知し、原著論文の確認に関する申合せ改訂内容について周知徹底を行い、研究倫理教育副責任
者が、2022 年 2 月に確認を行い、問題は無かった。
②研究倫理に関する教育、指導の徹底
医学系研究科及び医学部附属病院に所属するすべての研究者については、以下の事項を継続して
実施している。
・すべての研究者を対象に、全研究者に対して毎年の臨床研究講習会を受講すること。
・すべての研究者を対象に、系統的に臨床研究に関して学ぶことができる阪大病院独自の elearning システム CROCO(Clinical Research Online Professional Certification Program at
Osaka University)を受講すること。受講の確認については、倫理審査委員会新規申請時に、委員会
事務局にて確認する体制を構築している。
・eAPRIN の e-learning より、「責任ある研究行為について」「研究における不正行為」「データ
の扱い」「共同研究 のルール」「オーサーシップ」「盗用」「公的研究資金の取扱い」「利益相
反」「研究における個人に関わる情報の取扱い」の 9 単元を 3 年ごとに受講すること(ただし、項
目は教員、大学院生、技術職員等によって異なる)
なお、今回の不正事案については、2021 年 3 月の全研究者を対象とする臨床研究講習会において、
元データの確認、データの研究者間の共有、データのトレーサビリティの確保、指導体制の確認の
必要性を含めて説明した。
③共同研究実施機関における適正な臨床研究実施支援体制の強化
阪大病院は、適正かつ効率的に多施設共同臨床研究を実施する体制を整備し、質の高い治験及び
臨床研究の推進を図ることを目的に、平成 29 年度より関西圏を中心とした OCR ネット(大阪臨床研
究ネットワーク)を構築し、現在 27 機関が参画している。2021 年 5 月 10 日に開催した年会におい
て(Web 開催)、阪大病院未来医療開発部臨床研究センター長から、「人を対象とする生命科学・
医学系研究に関する倫理指針」対応および注意点に関して説明し、具体的な運用等について、質疑
応答を行った。また、今回の不正事案および発生要因について説明し、元データの確認、データの
研究者間の共有、データのトレーサビリティの確保、指導体制の確認の必要性を確認事項として提
様式第 7-16
108