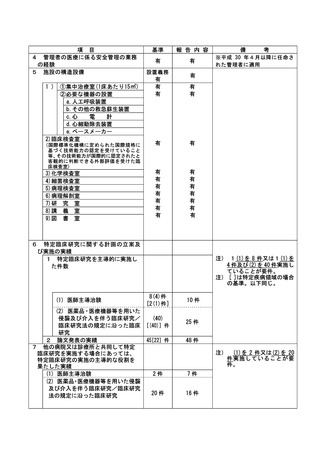
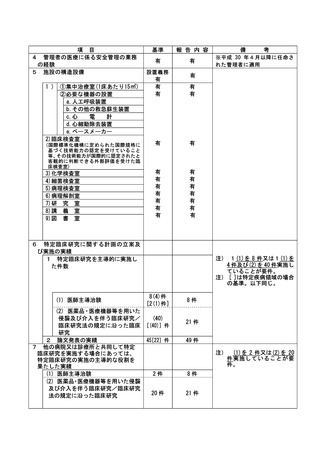
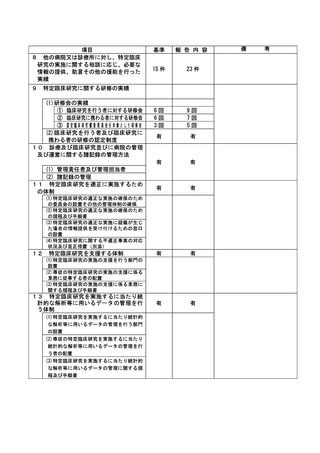
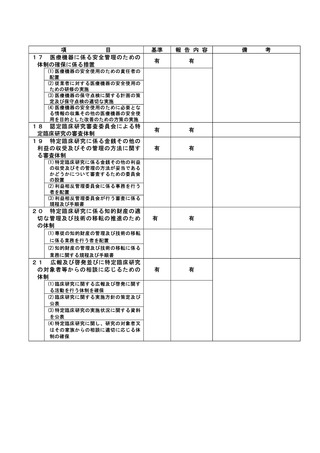
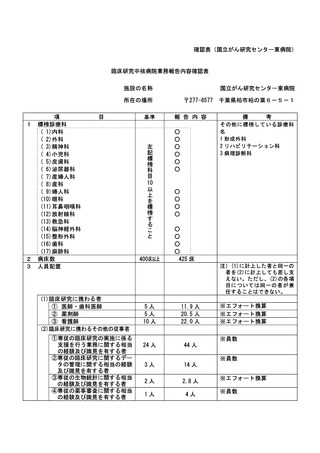
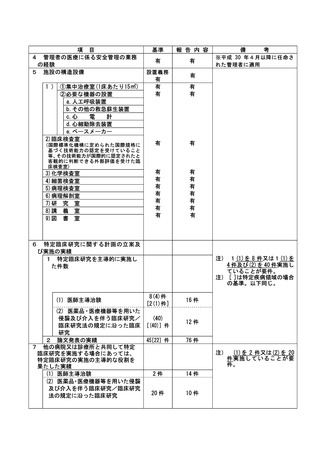
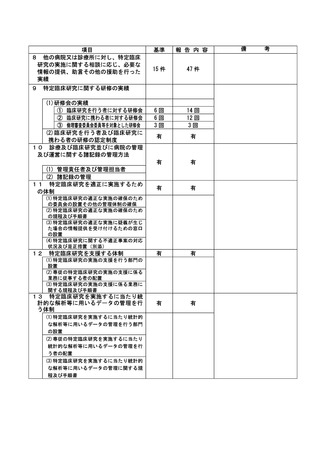
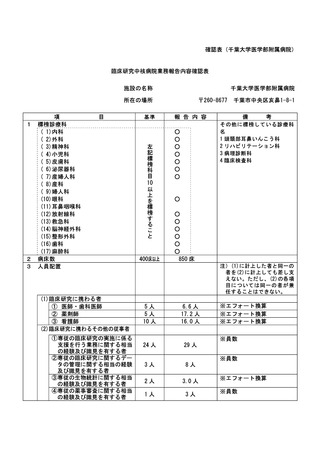
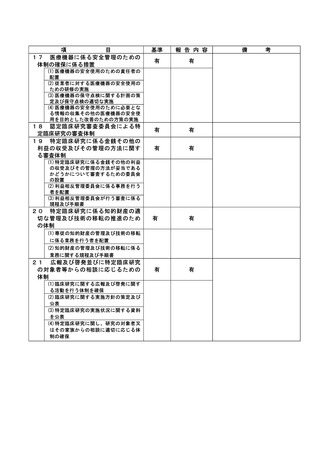
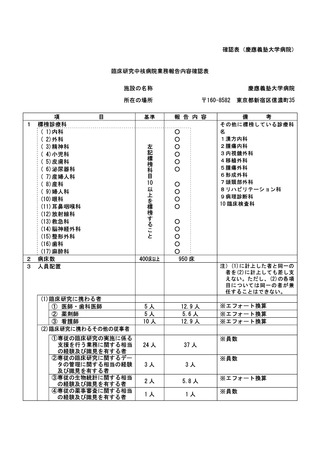
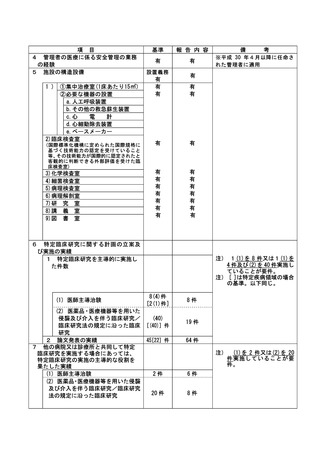
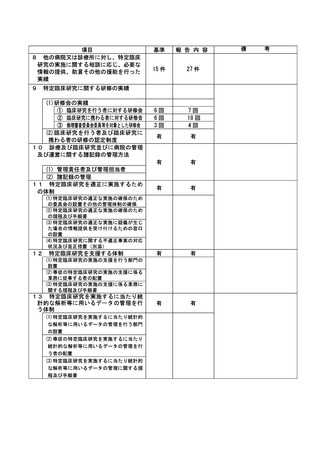
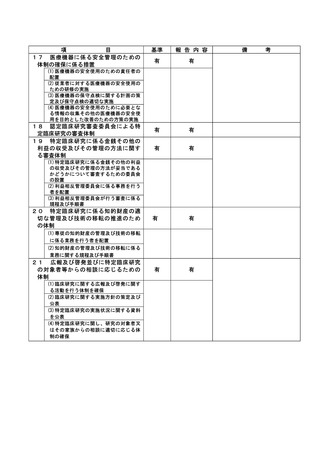
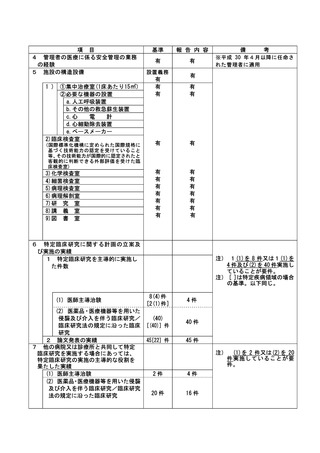
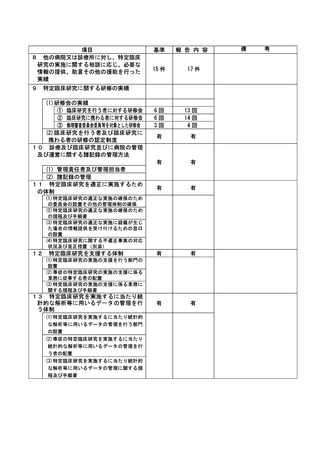
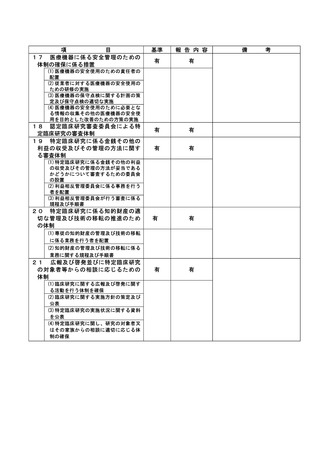
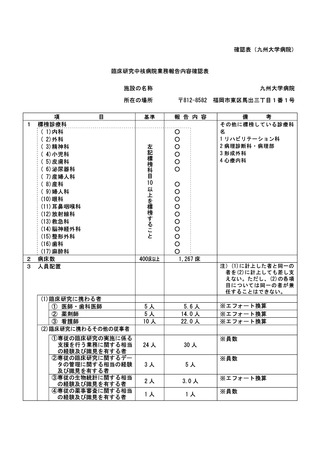
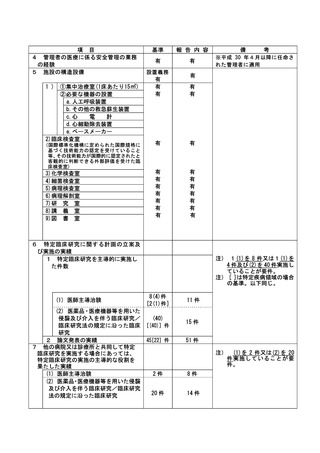
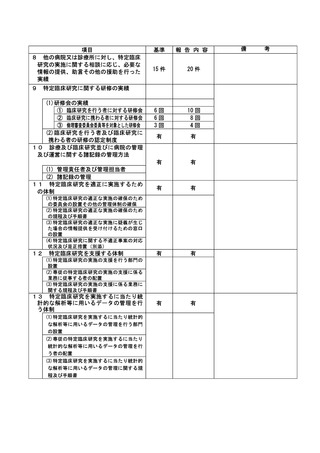
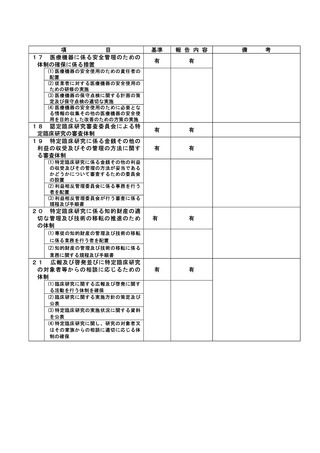
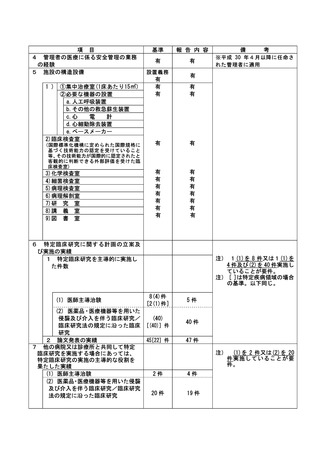
資料2:臨床研究中核病院業務報告内容確認表 (73 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
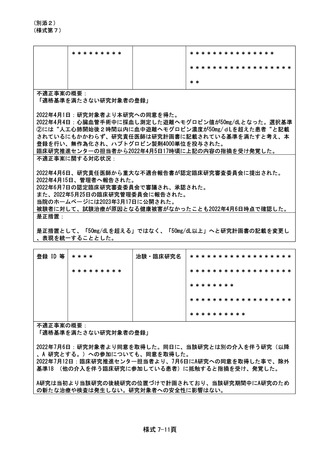
不適正事案の概要:
2022年6月**日と**日に治験用採血の検査会社に提出した際に、患者IDと氏名が記載された検体
処理時間記録表を一緒に送付した(個人情報の漏出)。
本記録表は本来臨床検査科より検体回収伝票の控えとともにCRC室へ返却されるものであり、CRC室
では記録表がないことには気づいていたが、次室内の捜索のみで臨床検査科への確認はされなかっ
た。その後、2022年6月13日に検査会社よりモニターを通じて記録表の受領についてCRC室に連絡が
あり判明した。
不適正事案に関する対応状況:
該当被験者に謝罪した。検査会社に個人情報が記載された記録表の回収とデータ削除を依頼し、個人
情報がすべて回収・削除されたことを確認した。
事案発覚後から 6 月 17 日までに関係部門で原因分析(伝票控えは CRC 室へ返却されるものであった
ため、CRC 室内での紛失と思い込んでしまったため、他の要因を疑わず、検査科とも共有をしなかっ
た)・是正措置の検討を行い、2022 年 6 月 17 日に病院長へ報告、2022 年 7 月 19 日の治験・臨床研
究運営委員会で周知した。
是正措置:
臨床検査科での手順を見直し、送付検体に同梱しない書類は伝票に混入しないよう別クリアファイ
ルに分けて管理することとした。CRC室では返却必要書類が不足していた場合は臨床検査科に確認を
行い所在を明らかにする手順について再確認を行った。
登録 ID 等
**
治験・臨床研究名
**
不適正事案の概要:
新たな侵襲・介入のある臨床試験において、2022年4月から約7か月間臨床試験登録を失念したまま
患者登録を行っていたことが、2022年9月に実施した院内の臨床試験を対象としたモニタリングにて
発覚した。発覚までに2例が登録されていた。
不適正事案に関する対応状況:
直ちに臨床試験登録を行った。
モニタリングでの指摘後関係部門で原因分析(研究者が臨床試験登録の必要性を認識していなかっ
た)・是正措置の検討を行い 2022 年 10 月 13 日に研究倫理指針に基づき病院長に報告、2022 年 10
月 18 日の治験・臨床研究運営委員会で周知した。
是正措置:
院内サーバーの臨床研究の手続き等を説明したページにおいて、臨床試験登録を行う必要がある試
験の種類とその手順に関する説明をわかりやすく改修した。
登録 ID 等
**
治験・臨床研究名
**
72