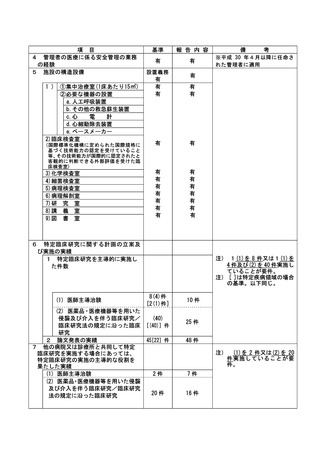
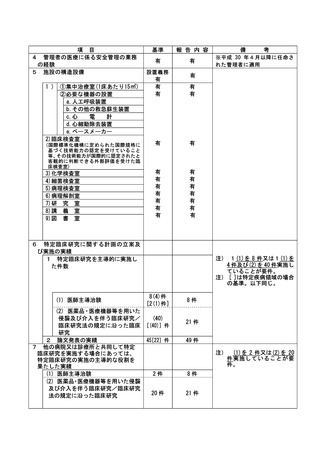
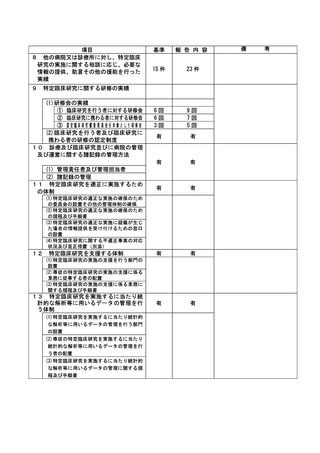
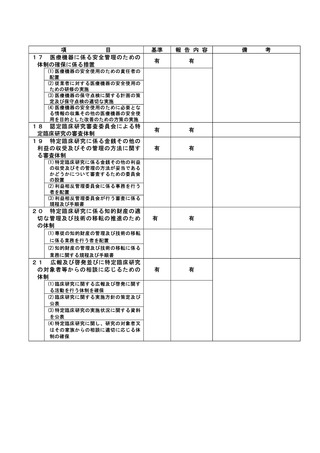
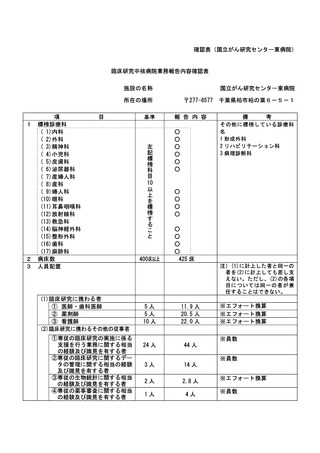
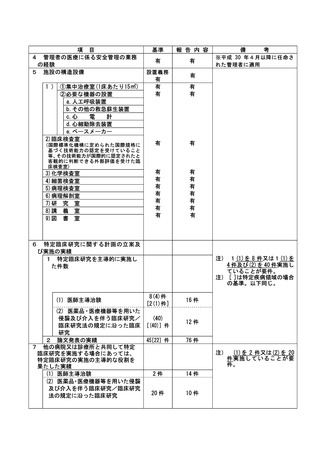
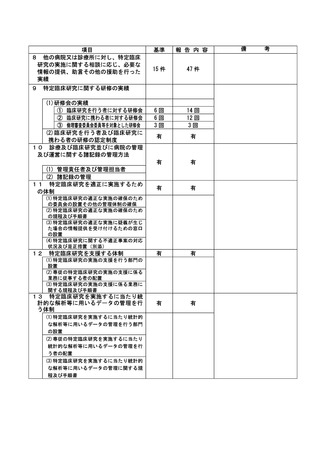
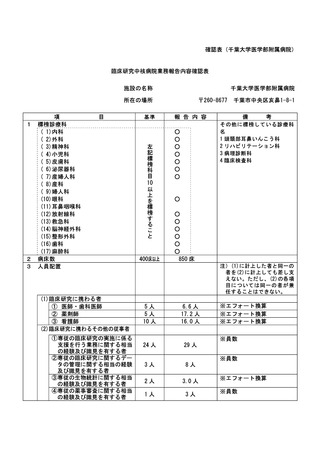
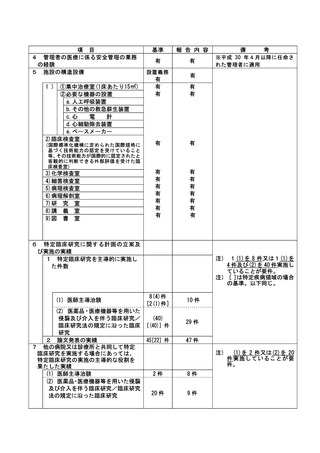
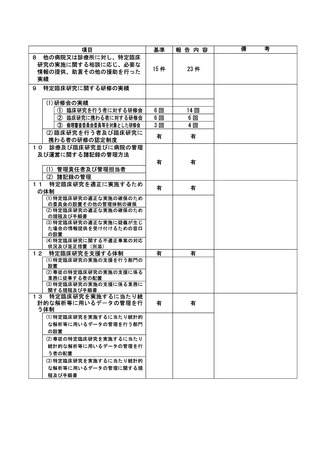
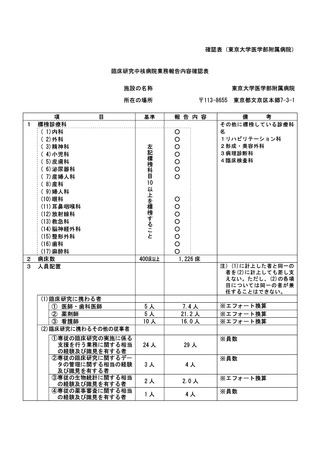
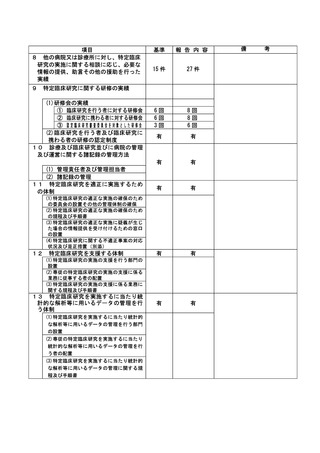
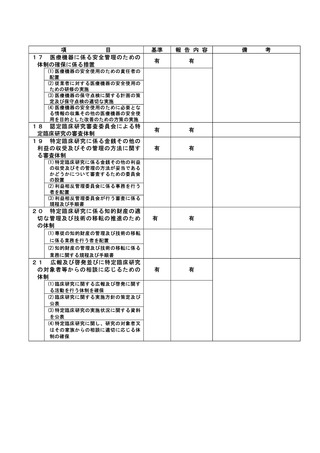
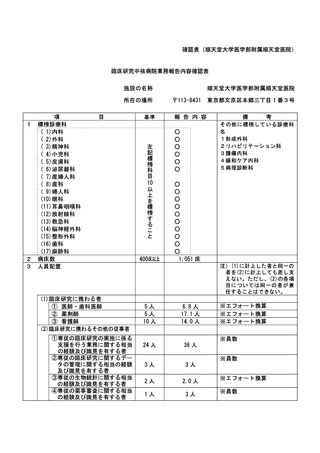
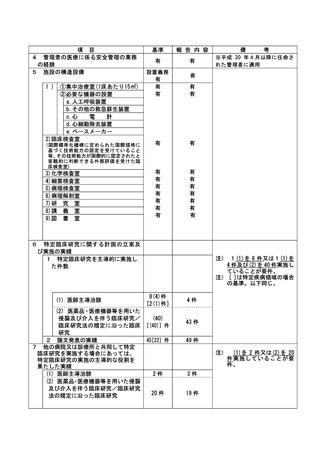
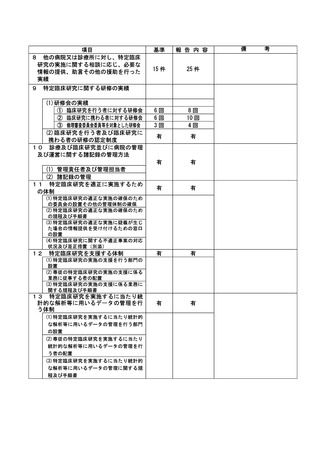
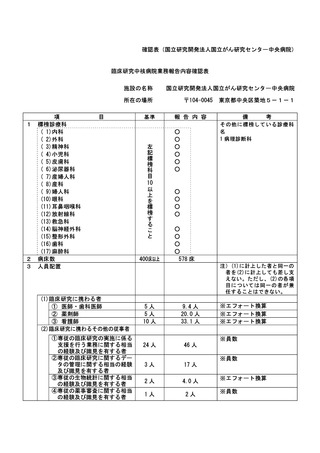
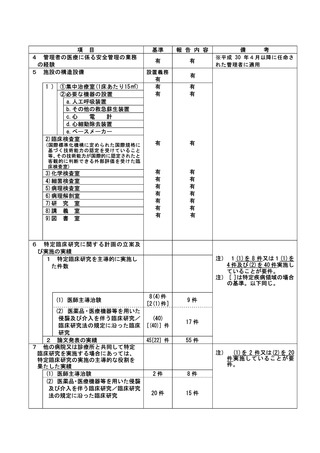
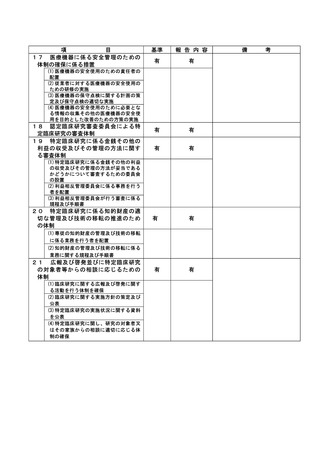
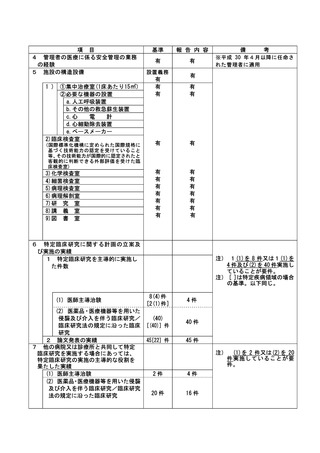
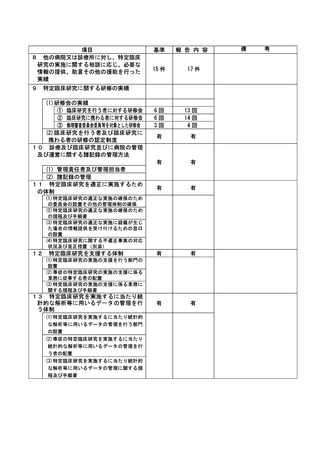
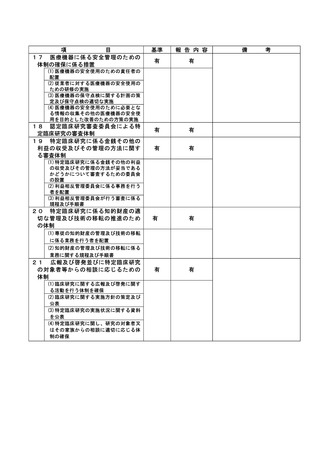
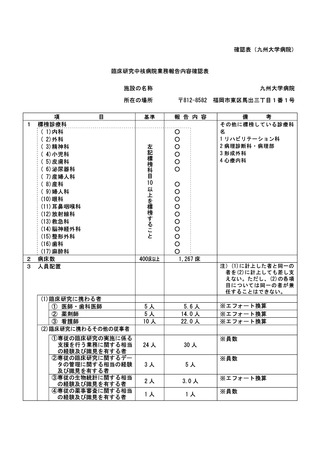
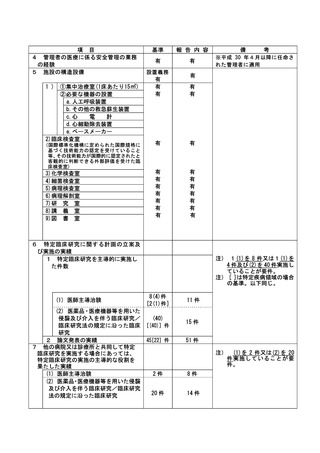
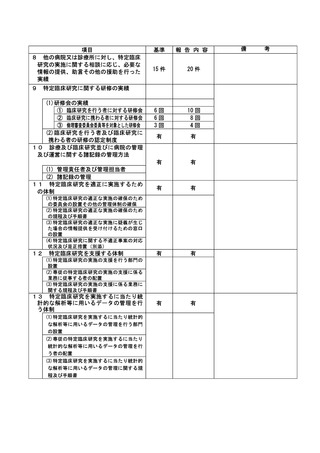
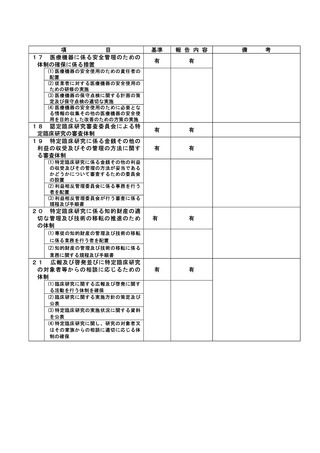
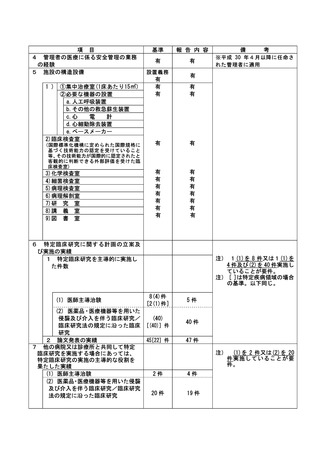
資料2:臨床研究中核病院業務報告内容確認表 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
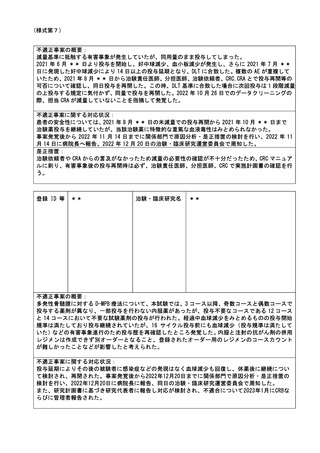
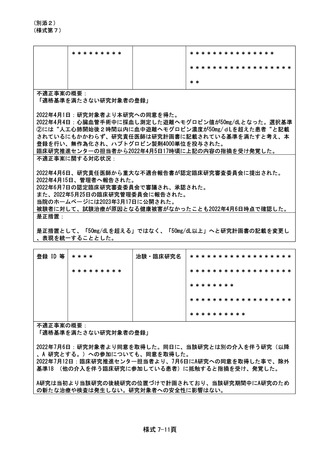
不適正事案に関する対応状況:
2022年10月19日に臨床研究適正実施推進部会の部会員(臨床研究支援部門長、研究企画室長及び
研究監査室長)が当該研究責任医師に不適合の内容、原因及び当該実施診療科としての再発防止策
に関してインタビューにて確認を行い、病院長及び副院長(研究担当)にその結果を報告した。
研究者に原因としては、外来での検体回収の手順は定められていたが、入院での回収の手順は定
められていいなかったことと考えられた(採取キット等に連絡先などの記載なし)。
本事案はその後、臨床研究適正実施推進部会(11月8日)、臨床研究管理委員会(11月16日)にて審
議された。
臨床研究管理委員会より「患者への対応の必要性、倫理的な観点から生命倫理専門家に確認する
など対応していただきたい」と指示あり。
生命倫理専門家より「試料の種類や情報がどうかに関わらず、対象者(患者)が提供してくれた
ものを無駄にしたことが問題であり、そのことへのお詫びは必要ではないかと考える」との見解で
、2022年11月22日研究者よりご存命の2名に電話にて連絡し状況を説明した旨が報告された。
本事案が発生した3症例中2例は現在当院に通院中、1例は亡くなられている。
是正措置:
発生当時(2017 年)の担当者が既に退職しており、経緯・詳細が一部不明であるため本事案に際
して研究責任者は再発防止策を策定していないが、現在の検体取扱いは以下の体制がとられており、
その後同様の事案は発生していないことを確認した。
・候補症例に研究補助者がサポートに入り、検体の収集までを一貫して実施している。
・被験者、看護師に検体の取扱いに関する説明を実施。
・採取キットは封筒に注意事項(回収等)を記載して交付している。また血液検体等は病棟に回収
用のボックスを設置し、回収することとした。
・電子カルテの掲示板に便の採取を依頼している旨、患者より預かったときの手順、担当者の連絡先
を記載している。
(注)1
2
不適正事案に関する調査の概要(方法、期間、結果等)を記載すること。
調査報告書その他関係書類が取りまとめられている場合は、添付すること。
30