・資料No1-1~1-5_第十八改正日本薬局方第一追補(案) (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00007.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和4年度第1回 7/26)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第十八改正日本薬局方第一追補
1
薄層板にスポットし,速やかにメタノール/酢酸アンモニウ
53
2
ム溶液(3→10)/酢酸(100)混液(20:1:1)を展開溶媒として
54
3
約10 cm展開した後,薄層板を風乾する.これに噴霧用ドラ
55
システムの再現性:標準溶液20 μL につき,上記の条
4
ーゲンドルフ試液を均等に噴霧し,風乾後,亜硝酸ナトリウ
56
件で試験を6回繰り返すとき,ヒルスチンのピーク
5
ム試液を均等に噴霧するとき,試料溶液から得た主スポット
57
面積の相対標準偏差は1.5%以下である.
6
7
以外のスポットは,標準溶液から得たスポットより濃くない. 58
である.
2) 定量用2 (qNMR純度規定)
白色の微細な結晶
59
ピークの単一性 本品1 mgをメタノール/希酢酸混液(7:
8
又は結晶性の粉末である.本品はエタノール(95)に溶けやす
60
3) 20 mLに溶かし,試料溶液とする.試料溶液20 μLにつき,
9
く,水に極めて溶けにくい.
61
次の条件で液体クロマトグラフィー〈2.01〉により試験を行
62
い,ヒルスチンのピークの頂点及び頂点の前後でピーク高さ
63
の中点付近の2時点を含む少なくとも3時点以上でのピーク
パラオキシ安息香酸ベンジル
C14H12O3
フィリンとイソリンコフィリンの分離度は1.5以上
10
融点〈2.60〉
11
含量
12
mol/L水酸化ナトリウム液20 mLを正確に加え,約70℃で1
64
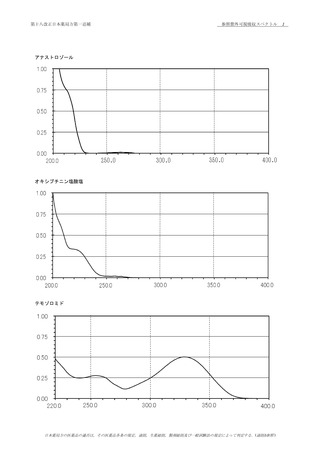
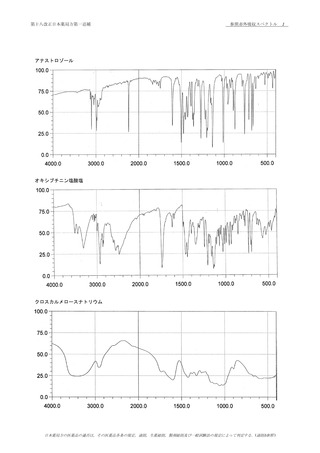
の吸収スペクトルを比較するとき,スペクトルの形状に差が
13
時間加熱した後,速やかに氷冷する.この液につき,過量の
65
ない.
14
水酸化ナトリウムを第二変曲点まで0.5 mol/L硫酸で滴定
66
15
〈2.50〉する(電位差滴定法).同様の方法で空試験を行う.
67
16
17
109 〜 114℃
99.0%以上.
定量法 本品約1 gを精密に量り,1
1 mol/L水酸化ナトリウム液1 mL=228.2 mg C14H12O3
69
カラム,カラム温度,移動相及び流量は「チョウトウコ
ウ」の定量法の試験条件を準用する.
検出器:フォトダイオードアレイ検出器(測定波長:
ヒルスチン,薄層クロマ
70
18
トグラフィー用.ただし,以下の定量用 1又は定量用2
71
19
(qNMR純度規定)の試験に適合するもの.なお,定量用2は
72
システムの性能:定量用リンコフィリン1 mgをメタノ
20
定量法で求めた含量で補正して用いる.
73
ール/希酢酸混液(7:3) 20 mLに溶かす.この液5
74
mLにアンモニア水(28) 1 mLを加え,50℃で2時間加
21
C22H28N2O3
68
試験条件
ヒルスチン,定量用
1) 定量用1
E 1 cm (245 nm):354 〜 389 [脱水物に換
245 nm,スペクトル測定範囲:220 〜 400 nm)
システム適合性
22
吸光度〈2.24〉
75
熱,又は還流冷却器を付けて10分間加熱する.冷後,
23
算したもの5 mg,メタノール/希酢酸混液(7:3),500
76
反応液1 mLを量り,メタノール/希酢酸混液(7:3)
24
mL].
77
を加えて5 mLとする.この液20 μLにつき,上記の
25
純度試験 類縁物質 本品5 mgをメタノール/希酢酸混
78
条件で操作するとき,リンコフィリン以外にイソリン
26
液(7:3) 100 mLに溶かし,試料溶液とする.この液1 mL
79
コフィリンのピークを認め,リンコフィリンとイソリ
27
を正確に量り,メタノール/希酢酸混液(7:3)を加えて正
80
28
確に50 mLとし,標準溶液とする.試料溶液及び標準溶液
81
定量法 ウルトラミクロ化学はかりを用い,本品5 mg及び
29
20 μLずつを正確にとり,次の条件で液体クロマトグラフ
82
核磁気共鳴スペクトル測定用1,4−BTMSB−d4 1 mgをそれ
30
ィー〈2.01〉により試験を行う.それぞれの液の各々のピ
83
ぞれ精密に量り,核磁気共鳴スペクトル測定用重水素化アセ
31
ーク面積を自動積分法により測定するとき,試料溶液のヒ
84
トン1 mLに溶かし,試料溶液とする.この液を外径5 mm
32
ルスチン以外のピークの合計面積は,標準溶液のヒルスチ
85
のNMR試料管に入れ,核磁気共鳴スペクトル測定用1,4−
33
ンのピーク面積より大きくない.
86
BTMSB−d4をqNMR用基準物質として,次の試験条件で核
87
磁気共鳴スペクトル測定法(〈2.21〉及び〈5.01〉)により,1H
34
1%
試験条件
ンコフィリンの分離度は1.5以上である.
35
検出器,カラム,カラム温度,移動相及び流量は「チ
88
NMRを測定する.qNMR用基準物質のシグナルをδ 0 ppm
36
ョウトウコウ」の定量法の試験条件を準用する.
89
とし,δ 6.70 〜 6.79 ppm付近のシグナルの面積強度A (水素
37
面積測定範囲:溶媒のピークの後からヒルスチンの保
90
数2に相当)を算出する.
91
ヒルスチン(C22H28N2O3)の量(%)
38
39
持時間の約1.5倍の範囲
システム適合性
40
検出の確認:標準溶液1 mLを正確に量り,メタノー
41
ル/希酢酸混液(7:3)を加えて正確に20 mL とす
42
る.この液20 μLから得たヒルスチンのピーク面積
43
が,標準溶液のヒルスチンのピーク面積の3.5 〜
44
6.5%になることを確認する.
45
システムの性能:定量用リンコフィリン1 mgをメタ
46
ノール/希酢酸混液(7:3) 20 mLに溶かす.この
47
液5 mLにアンモニア水(28) 1 mLを加え,50℃で2
48
時間加熱,又は還流冷却器を付けて10分間加熱す
49
る.冷後,反応液1 mLを量り,メタノール/希酢
50
酸混液(7:3)を加えて5 mLとする.この液20 μLに
51
52
92
=Ms × I × P/(M × N ) × 1.6268
93
M:本品の秤取量(mg)
94
Ms:核磁気共鳴スペクトル測定用1,4−BTMSB− d4の秤
95
取量(mg)
96
I:核磁気共鳴スペクトル測定用1,4−BTMSB− d4のシグ
97
ナルの面積強度を18.000としたときのシグナルの面積
98
99
100
強度A
N:Aに由来するシグナルの水素数
P:核磁気共鳴スペクトル測定用1,4−BTMSB−d4の純度
101
(%)
つき,上記の条件で操作するとき,リンコフィリン
102
試験条件
以外にイソリンコフィリンのピークを認め,リンコ
103
104
装置:1H共鳴周波数400 MHz以上の核磁気共鳴スペク
トル測定装置
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する.(通則5参照 )