・資料No1-1~1-5_第十八改正日本薬局方第一追補(案) (71 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00007.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和4年度第1回 7/26)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第十八改正日本薬局方第一追補
1
持時間の比は約0.1,約0.5及び約0.9であり,パラオ
45
(2)
2
キシ安息香酸プロピルとパラオキシ安息香酸ブチルの
46
新たに煮沸して冷却した水5 mL及びブロモクレゾールグリ
3
分離度は5.0以上であり,パラオキシ安息香酸イソブ
47
ーン・水酸化ナトリウム・エタノール試液0.1 mLを加える.
4
チルとパラオキシ安息香酸ブチルの分離度は1.5以上
48
この液に液の色が青色に変化するまで0.1 mol/L水酸化ナト
5
である.
49
リウム液を加えるとき,その量は0.1 mL以下である.
酸
(1)の液2 mLにエタノール(95) 3 mLを加えた後,
6
システムの再現性:標準溶液10 μLにつき,上記の条件
50
(3) 類縁物質 本品50.0 mgをメタノール2.5 mLに溶かし
7
で試験を6回繰り返すとき,パラオキシ安息香酸ブチ
51
た後,移動相を加えて正確に50 mLとする.この液10 mLを
8
ルのピーク面積の相対標準偏差は0.85%以下である.
52
正確に量り,移動相を加えて正確に100 mLとし,試料溶液
53
とする.この液1 mLを正確に量り,移動相を加えて正確に
54
20 mLとする.この液1 mLを正確に量り,移動相を加えて
55
正確に10 mLとし,標準溶液とする.試料溶液及び標準溶液
56
10 μLずつを正確にとり,次の条件で液体クロマトグラフィ
57
ー 〈2.01〉により試験を行う.それぞれの液の各々のピーク
58
面積を自動積分法により測定するとき,試料溶液のパラオキ
パラオキシ安息香酸プロピル
59
シ安息香酸プロピルに対する相対保持時間約0.3のパラオキ
Propyl Parahydroxybenzoate
60
シ安息香酸のピーク面積は,標準溶液のパラオキシ安息香酸
61
プロピルのピーク面積より大きくない(0.5%).ただし,パ
62
ラオキシ安息香酸のピーク面積は自動積分法により求めた面
63
積に感度係数1.4を乗じた値とする.また,試料溶液のパラ
64
オキシ安息香酸プロピル及びパラオキシ安息香酸以外のピー
65
クの面積は,標準溶液のパラオキシ安息香酸プロピルのピー
ク面積より大きくない(0.5%).また,試料溶液のパラオキ
9
◆
貯法
10
11
12
13
容器 密閉容器.◆
医薬品各条の部 パラオキシ安息香酸プロピルの条を次のよ
うに改める.
14
15
C10H12O3:180.20
66
16
Propyl 4-hydroxybenzoate
67
シ安息香酸プロピル以外のピークの合計面積は,標準溶液の
17
[94-13-3]
68
パラオキシ安息香酸プロピルのピーク面積の2倍より大きく
69
ない(1.0%).ただし,標準溶液のパラオキシ安息香酸プロ
70
ピルのピーク面積の1/5以下のピークは計算しない(0.1%).
18
本医薬品各条は,三薬局方での調和合意に基づき規定した医薬品
19
各条である.
71
72
20
なお,三薬局方で調和されていない部分のうち,調和合意におい
21
73
て,調和の対象とされた項中非調和となっている項の該当箇所は
22
74
「◆
23
75
することとした項は「
24
31
32
33
34
35
36
37
◇
」で囲むことにより示す.
の試験条件を準用する.
面積測定範囲:パラオキシ安息香酸プロピルの保持時間
の2.5倍の範囲
システム適合性
77
システムの性能は定量法のシステム適合性を準用する.
78
◇
検出の確認:標準溶液2 mLを正確に量り,移動相を
加えて正確に10 mLとする.この液10 μLから得たパ
80
ラオキシ安息香酸プロピルのピーク面積が,標準溶液
本品は無色の結晶又は白色の結晶性の粉末である.
81
のパラオキシ安息香酸プロピルのピーク面積の14 ~
本品はメタノール,エタノール(95)又はアセトンに溶けや
82
(C10H12O3) 98.0 ~ 102.0%を含む.
◆
76
検出器,カラム,カラム温度,移動相及び流量は定量法
79
本品は定量するとき,パラオキシ安息香酸プロピル
27
30
◇
品医療機器総合機構のウェブサイトに掲載している.
26
29
」で,調和の対象とされた項以外に日本薬局方が独自に規定
三薬局方の調和合意に関する情報については,独立行政法人医薬
25
28
◆
試験条件
性状
すく,水に極めて溶けにくい.◆
83
26%になることを確認する.◇
◇
システムの再現性:標準溶液10 μLにつき,上記の条
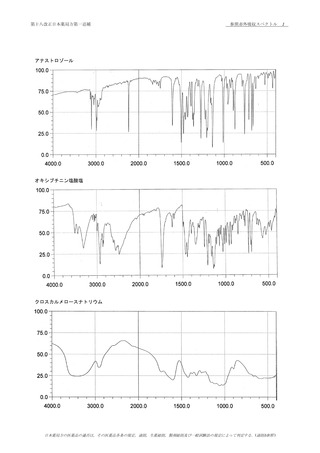
本品につき,赤外吸収スペクトル測定法 〈2.25〉の
84
件で試験を6回繰り返すとき,パラオキシ安息香酸プ
臭化カリウム錠剤法により試験を行い,本品のスペクトルと
85
ロピルのピーク面積の相対標準偏差は2.0%以下であ
本品の参照スペクトル又はパラオキシ安息香酸プロピル標準
86
品のスペクトルを比較するとき,両者のスペクトルは同一波
87
強熱残分〈2.44〉
数のところに同様の強度の吸収を認める.
88
定量法 本品及びパラオキシ安息香酸プロピル標準品約50 mg
89
ずつを精密に量り,それぞれメタノール2.5 mLに溶かし,
90
移動相を加えて正確に50 mLとする.それぞれの液10 mLを
正確に量り,それぞれに移動相を加えて正確に100 mLとし,
確認試験
融点〈2.60〉
96 ~ 99℃
純度試験
る.◇
0.1%以下(1 g).
38
(1) 溶状 本品1.0 gをエタノール(95)に溶かして10 mLと
91
39
するとき,液は澄明で,液の色はエタノール(95)又は次の比
92
試料溶液及び標準溶液とする.試料溶液及び標準溶液10 μL
40
較液より濃くない.
93
ずつを正確にとり,次の条件で液体クロマトグラフィー
比較液:塩化コバルト(Ⅱ)の色の比較原液5.0 mL,塩化鉄
94
〈2.01〉 により試験を行い,それぞれの液のパラオキシ安息
42
(Ⅲ)の色の比較原液12.0 mL及び硫酸銅(Ⅱ)の色の比較
95
香酸プロピルのピーク面積AT及びA Sを測定する.
43
原液2.0 mLをとり,薄めた希塩酸(1→10)を加えて1000
44
mLとする.
96
パラオキシ安息香酸プロピル(C10H12O3)の量(mg)
41
97
=MS × AT/A S
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する. (通則5参照 )