・資料No1-1~1-5_第十八改正日本薬局方第一追補(案) (62 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00007.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和4年度第1回 7/26)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第十八改正日本薬局方第一追補
1
サルポグレラート塩酸塩細粒
44
ステアリン酸
2
製剤均一性 〈6.02〉
45
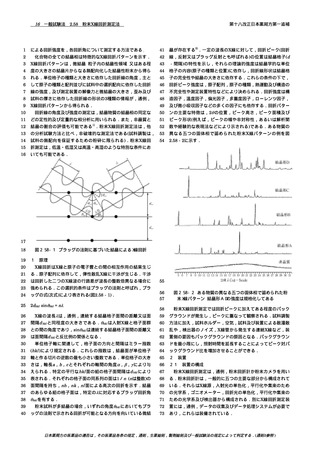
凝固点 装置は内径約25 mm,長さ約150 mmの試験管を,内
46
径約40 mm,長さ約160 mmの試験管の内側に取り付けた構
3
分包品は,次の方法により含量均一性試
験を行うとき,適合する.
4
本品1包をとり,内容物の全量を取り出し,移動相4V /5
47
造を持つものからなる.内側試験管は栓をし,その栓には最
5
mLを加え,超音波処理により粒子を小さく分散させた後,
48
小目盛りが0.2℃,全長約175 mmの温度計を水銀球◆の上端◆
6
1 mL中にサルポグレラート塩酸塩 (C24H31NO6 ・HCl)約1
49
が試験管の底から約15 mmの位置にくるように固定する.
7
mgを含む液となるように移動相を加えて正確にV mLとし,
50
内側試験管の栓は,更に下端に外径約18 mmの輪が直角に
8
遠心分離する.上澄液5 mLを正確に量り,移動相を加えて
51
取り付けられたガラス製又は他の適切な材料からなるかき混
9
正確に50 mLとし,試料溶液とする.以下定量法を準用する. 52
ぜ棒を通す穴を開けたものとする.1 Lのビーカーの中央に
53
上記のようにジャケットを取り付けた構造を持つ内側試験管
54
を取り付け,そのビーカーには,適切な冷却液を上部から
55
20 mm以内まで満たす.試料をあらかじめ加温して溶かし,
56
内側試験管に温度計の水銀球が十分にかくれるまで入れ,急
57
速に冷却し,おおよその凝固点を求める.内側試験管をおお
10
11
12
13
サルポグレラート塩酸塩(C24H31NO6・HCl)の量(mg)
=MS × AT/AS × V /50
MS:脱水物に換算したサルポグレラート塩酸塩標準品の
秤取量(mg)
58
よその凝固点よりも約5℃高い温度の浴に入れ,最後の少量
本品を粉末とし,サルポグレラート塩酸塩
59
の結晶のほかは全て溶けるまで放置する.ビーカーに予想し
15
(C24H31NO6・HCl)約0.25 gに対応する量を精密に量り,移
60
た凝固点よりも5℃低い温度の水又は飽和食塩水を満たし,
16
動相200 mLを加え,超音波処理により粒子を小さく分散さ
61
内側試験管を外側試験管に取り付ける.幾らかの種結晶が存
17
せる.この液に移動相を加えて正確に250 mLとし,遠心分
62
在することを確認し,結晶が析出し始めるまで十分にかき混
18
離する.上澄液5 mLを正確に量り,移動相を加えて正確に
63
ぜる.結晶が析出する際の最高温度を読み取り,凝固点とす
19
50 mLとし,試料溶液とする.別にサルポグレラート塩酸塩
64
る.
20
標準品(別途「サルポグレラート塩酸塩」と同様の方法で水
65
21
分〈2.48〉を測定しておく)約50 mgを精密に量り,移動相を
66
試料をあらかじめ加温して溶かし,試料容器Bの標線Cまで
22
加えて正確に50 mLとする.この液5 mLを正確に量り,移
67
入れ,浸線付温度計Fの浸線Hを試料のメニスカスに合わせ
23
動相を加えて正確に50 mLとし,標準溶液とする.試料溶液
68
た後,急速に冷却し,おおよその凝固点を求める.試料容器
24
及び標準溶液10 μLずつを正確にとり,次の条件で液体クロ
69
Bをおおよその凝固点よりも約5℃高い温度の浴に入れ,最
25
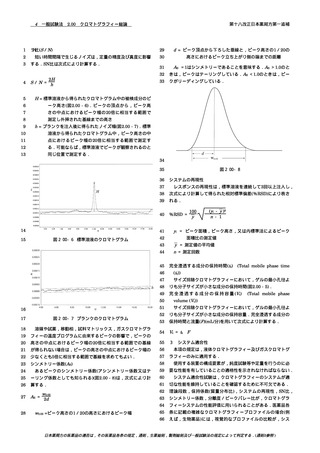
マトグラフィー 〈2.01〉により試験を行い,それぞれの液の
70
後の少量の結晶のほかは全て溶けるまで放置する.Dに予想
26
サルポグレラートのピーク面積AT及びASを測定する.
71
した凝固点よりも5℃低い温度の水又は飽和食塩水を満たし,
72
BをAに取り付ける.幾らかの種結晶が存在することを確認
73
し,結晶が析出し始めるまで十分にかき混ぜる.結晶が析出
74
する際の最高温度を読み取り,凝固点とする.
14
27
定量法
サルポグレラート塩酸塩(C24H31NO6・HCl)の量(mg)
28
=MS × AT/AS × 5
29
MS:脱水物に換算したサルポグレラート塩酸塩標準品の
30
31
32
秤取量(mg)
75
76
また,凝固点測定法 〈2.42〉に規定する装置も使用できる.
凝固点は,ステアリン酸50は53 ~ 59℃,ステアリン酸
70は57 ~ 64℃及びステアリン酸95は64 ~ 69℃である.
試験条件
「サルポグレラート塩酸塩」の定量法の試験条件を準用
33
する.
34
システム適合性
77
医薬品各条の部 ステアリン酸マグネシウムの条を次のよう
78
に改める.
35
システムの性能:標準溶液10 μLにつき,上記の条件で
79
ステアリン酸マグネシウム
36
操作するとき,サルポグレラートのピークの理論段数
80
Magnesium Stearate
37
及びシンメトリー係数は,それぞれ5000段以上,1.8
38
以下である.
39
システムの再現性:標準溶液10 μLにつき,上記の条件
81
40
で試験を6回繰り返すとき,サルポグレラートのピー
82
ク面積の相対標準偏差は1.0%以下である.
83
なお,三薬局方で調和されていない部分のうち,調和合意におい
84
て,調和の対象とされた項中非調和となっている項の該当箇所は
85
「◆
86
することとした項は「
41
42
43
医薬品各条の部 ステアリン酸の条凝固点の項を次のように
改める.
87
88
本医薬品各条は,三薬局方での調和合意に基づき規定した医薬品
各条である.
◆
」で,調和の対象とされた項以外に日本薬局方が独自に規定
◇
◇
」で囲むことにより示す.
三薬局方の調和合意に関する情報については,独立行政法人医薬
品医療機器総合機構のウェブサイトに掲載している.
89
本品は植物又は動物由来の固体混合脂肪酸のマグネシウム
90
塩で,主としてステアリン酸マグネシウム及びパルミチン酸
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する. (通則5参照 )