・資料No1-1~1-5_第十八改正日本薬局方第一追補(案) (54 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00007.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和4年度第1回 7/26)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
医薬品各条
医薬品各条名
19 .
純度試験において削除する項目
(859)
ロベンザリットナトリウム
重金属,ヒ素
(860)
ロラゼパム
重金属,ヒ素
(861)
黄色ワセリン
重金属,ヒ素
(862)
白色ワセリン
重金属,ヒ素
(863)
ワルファリンカリウム
重金属
1
2
3
4
5
35
とする.この液1 mLを正確に量り,移動相Aを加えて正確
36
に100 mLとし,標準溶液とする.試料溶液及び標準溶液10
37
μLずつを正確にとり,次の条件で液体クロマトグラフィー
38
〈2.01〉 により試験を行う.試料溶液の類縁物質のピーク面
39
積 AT及び標準溶液のアナストロゾールのピークの面積 ASを
アナストロゾール
40
自動積分法により測定し,次式により計算するとき,試料溶
Anastrozole
41
液のアナストロゾールに対する相対保持時間約0.63の類縁物
42
質A及び相対保持時間約2.2の類縁物質Bはそれぞれ0.2%以
43
下,その他の個々の類縁物質は0.1%以下であり,その他の
44
類縁物質の合計量は0.2%以下,類縁物質の合計量は0.5%以
45
下である.
46
類縁物質の量(%)=MS/MT × AT/AS
47
MS:アナストロゾール標準品の秤取量(mg)
MT:本品の秤取量(mg)
医薬品各条の部 アトロピン硫酸塩注射液の条の次に次の二
条を加える.
6
7
C17H19N5:293.37
48
8
2,2'-[5-(1H-1,2,4-Triazol-1-ylmethyl)benzene-1,3-diyl]bis(2-
9
49
methylpropanenitrile)
50
検出器,カラム,カラム温度,移動相A,移動相B,移
[120511-73-1]
51
動相の送液及び流量は定量法の試験条件を準用する.
10
11
12
13
14
15
16
本品は定量するとき,アナストロゾール(C17H19N5) 98.0
~102.0%を含む.
52
53
試験条件
面積測定範囲:試料溶液注入後40分間
システム適合性
54
検出の確認:標準溶液1 mLを正確に量り,移動相Aを
本品は白色の結晶性の粉末又は粉末である.
55
加えて正確に20 mLとする.この液10 μLから得たア
本品はアセトニトリルに極めて溶けやすく,メタノール又
56
ナストロゾールのピーク面積が,標準溶液のアナスト
57
ロゾールのピーク面積の3 ~ 7%になることを確認す
性状
はエタノール(99.5)に溶けやすく,水に極めて溶けにくい.
本品は結晶多形が認められる.
58
る.
17
確認試験
18
(1)
19
20
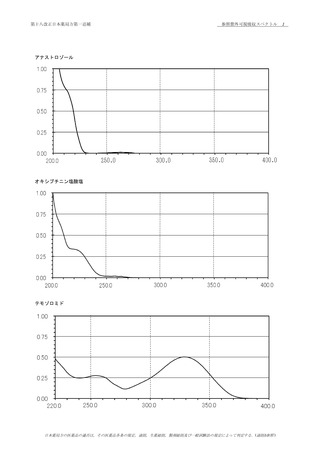
のスペクトルと本品の参照スペクトル又はアナストロゾール
21
62
標準品について同様に操作して得られたスペクトルを比較す
22
63
システムの再現性:標準溶液10 μLにつき,上記の条件
るとき,両者のスペクトルは同一波長のところに同様の強度
23
64
で試験を6回繰り返すとき,アナストロゾールのピー
の吸収を認める.
24
65
(2)
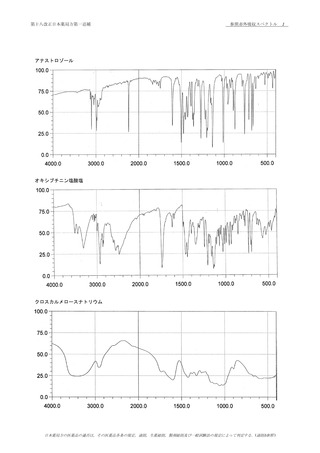
本品につき,赤外吸収スペクトル測定法 〈2.25〉の臭
25
66
水分〈2.48〉
化カリウム錠剤法により試験を行い,本品のスペクトルと本
26
67
強熱残分〈2.44〉
品の参照スペクトル又はアナストロゾール標準品のスペクト
27
ルを比較するとき,両者のスペクトルは同一波数のところに
68
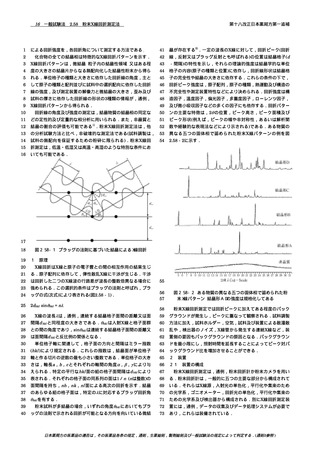
定量法 本品及びアナストロゾール標準品約25 mgずつを精密
28
に量り,それぞれに液体クロマトグラフィー用アセトニトリ
同様の強度の吸収を認める.
69
70
ル20 mLを加えて超音波処理して溶かし,移動相Aを加えて
71
正確に50 mLとし,試料溶液及び標準溶液とする.試料溶液
72
及び標準溶液10 μLずつを正確にとり,次の条件で液体クロ
73
マトグラフィー 〈2.01〉により試験を行い,それぞれの液の
74
アナストロゾールのピーク面積AT及びASを測定する.
75
アナストロゾール(C17H19N5)の量(mg)=MS × AT/AS
59
システムの性能:標準溶液10 μLにつき,上記の条件で
本品のメタノール溶液(1→50000)につき,紫外可視
60
操作するとき,アナストロゾールのピークの理論段数
吸光度測定法 〈2.24〉により吸収スペクトルを測定し,本品
61
及びシンメトリー係数は,それぞれ1500段以上,1.4
29
純度試験 類縁物質 本品約50 mgを精密に量り,液体クロマ
30
トグラフィー用アセトニトリル10 mLを加え,超音波処理し
31
て溶かした後,移動相Aを加えて正確に25 mLとし,試料溶
32
液とする.別にアナストロゾール標準品約50 mgを精密に量
33
り,液体クロマトグラフィー用アセトニトリル10 mLを加え,
34
超音波処理して溶かした後,移動相Aを加えて正確に25 mL
以下である.
ク面積の相対標準偏差は2.0%以下である.
0.3%以下(50 mg,電量滴定法).
0.1%以下(1 g).
日本薬局方の医薬品の適否は,その医薬品各条の規定,通則,生薬総則,製剤総則及び一般試験法の規定によって判定する. (通則5参照 )