よむ、つかう、まなぶ。
資料1-2 令和5年度研究事業実施方針(案)の概要【AMED研究】 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26761.html |
| 出典情報 | 厚生科学審議会科学技術部会(第130回 7/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
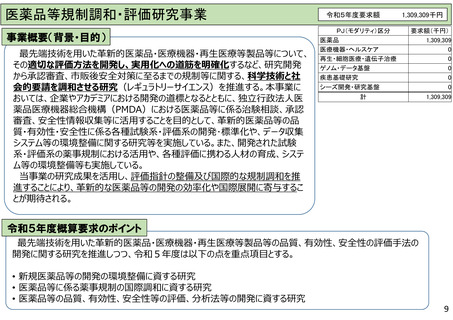
医薬品等規制調和・評価研究事業
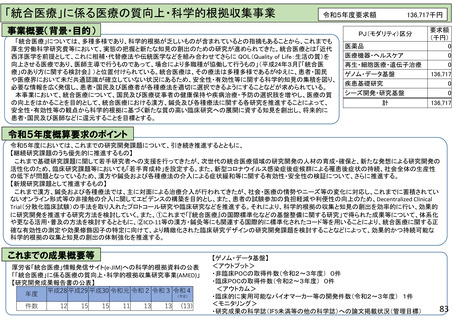
事業概要(背景・目的)
最先端技術を用いた革新的医薬品・医療機器・再生医療等製品等について、
その適切な評価方法を開発し、実用化への道筋を明確化するなど、研究開発
から承認審査、市販後安全対策に至るまでの規制等に関する、科学技術と社
会的要請を調和させる研究(レギュラトリーサイエンス)を推進する。本事業に
おいては、企業やアカデミアにおける開発の道標となるとともに、独立行政法人医
薬品医療機器総合機構(PMDA)における医薬品等に係る治験相談、承認
審査、安全性情報収集等に活用することを目的として、革新的医薬品等の品
質・有効性・安全性に係る各種試験系・評価系の開発・標準化や、データ収集
システム等の環境整備に関する研究等を実施している。また、開発された試験
系・評価系の薬事規制における活用や、各種評価に携わる人材の育成、システ
ム等の環境整備等も実施している。
当事業の研究成果を活用し、評価指針の整備及び国際的な規制調和を推
進することにより、革新的な医薬品等の開発の効率化や国際展開に寄与するこ
とが期待される。
令和5年度要求額
PJ(モダリティ)区分
医薬品
医療機器・ヘルスケア
再生・細胞医療・遺伝子治療
ゲノム・データ基盤
疾患基礎研究
1,309,309千円
要求額(千円)
1,309,309
0
0
0
0
シーズ開発・研究基盤
計
0
1,309,309
令和5年度概算要求のポイント
最先端技術を用いた革新的医薬品・医療機器・再生医療等製品等の品質、有効性、安全性の評価手法の
開発に関する研究を推進しつつ、令和5年度は以下の点を重点項目とする。
• 新規医薬品等の開発の環境整備に資する研究
• 医薬品等に係る薬事規制の国際調和に資する研究
• 医薬品等の品質、有効性、安全性等の評価、分析法等の開発に資する研究
9
事業概要(背景・目的)
最先端技術を用いた革新的医薬品・医療機器・再生医療等製品等について、
その適切な評価方法を開発し、実用化への道筋を明確化するなど、研究開発
から承認審査、市販後安全対策に至るまでの規制等に関する、科学技術と社
会的要請を調和させる研究(レギュラトリーサイエンス)を推進する。本事業に
おいては、企業やアカデミアにおける開発の道標となるとともに、独立行政法人医
薬品医療機器総合機構(PMDA)における医薬品等に係る治験相談、承認
審査、安全性情報収集等に活用することを目的として、革新的医薬品等の品
質・有効性・安全性に係る各種試験系・評価系の開発・標準化や、データ収集
システム等の環境整備に関する研究等を実施している。また、開発された試験
系・評価系の薬事規制における活用や、各種評価に携わる人材の育成、システ
ム等の環境整備等も実施している。
当事業の研究成果を活用し、評価指針の整備及び国際的な規制調和を推
進することにより、革新的な医薬品等の開発の効率化や国際展開に寄与するこ
とが期待される。
令和5年度要求額
PJ(モダリティ)区分
医薬品
医療機器・ヘルスケア
再生・細胞医療・遺伝子治療
ゲノム・データ基盤
疾患基礎研究
1,309,309千円
要求額(千円)
1,309,309
0
0
0
0
シーズ開発・研究基盤
計
0
1,309,309
令和5年度概算要求のポイント
最先端技術を用いた革新的医薬品・医療機器・再生医療等製品等の品質、有効性、安全性の評価手法の
開発に関する研究を推進しつつ、令和5年度は以下の点を重点項目とする。
• 新規医薬品等の開発の環境整備に資する研究
• 医薬品等に係る薬事規制の国際調和に資する研究
• 医薬品等の品質、有効性、安全性等の評価、分析法等の開発に資する研究
9