よむ、つかう、まなぶ。
資料1-2 令和5年度研究事業実施方針(案)の概要【AMED研究】 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26761.html |
| 出典情報 | 厚生科学審議会科学技術部会(第130回 7/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
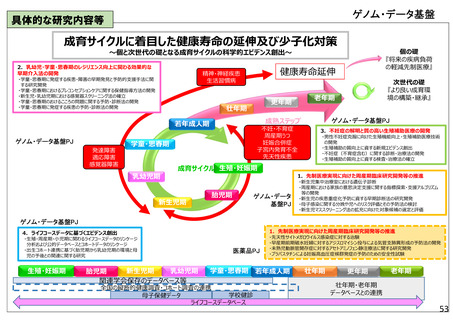
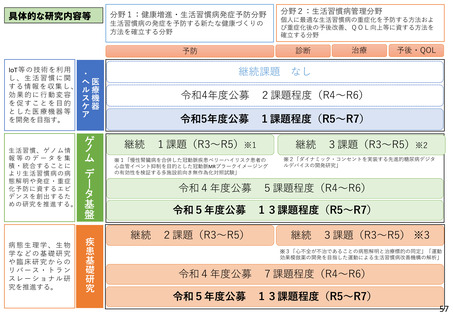
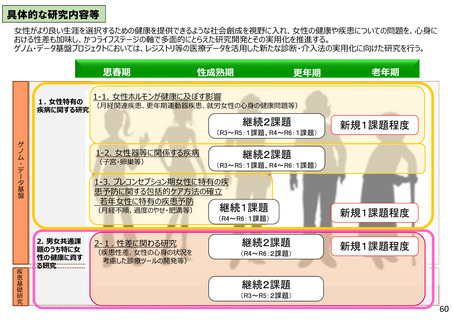
具体的な研究内容等
<医薬品プロジェクト>
日本で生み出された基礎研究の成果を薬事承認につなげ、革新的な医薬品を創出するため、科学性及び倫理性が十分に担保されうる
質の高い臨床研究・医師主導治験等を支援する。
<支援に係る主なコンセプト>
①患者ニーズの高いもの
臨床研究・医師主導治験
の実施を支援
疾患の希少性、不採算性等を総合的に考慮し、公益性の高いも
のを支援
(臨床研究・医師主導治験の)プロトコール作成
特定臨床研究
医師主導治験(新有効成分、新効能、新用法用量医薬品)
医師主導治験(小児対象)
②疾患登録システム(患者レジス
トリ)等の活用
疾患登録システムを、薬事承認申請に利用可能な比較対照群等
に利活用する、臨床研究・医師主導治験を支援
③ Decentralized Clinical Trial
(DCT)等の新しい手法の活用
デジタルデバイス、オンライン診療等の新しい技術や訪問診療
等を活用し、被験者の安全性やデータの信頼性を担保しつつ、
被験者や関係者の負担を軽減し得る新しい手法を活用した臨床
試験(Decentralized Clinical Trial;分散化臨床試験)を支援
当面優先して議論する課題 令和2年度まとめ(令和3年3月29日医薬品開発協議会)抜粋
Ⅱ.本協議会で指摘された課題や現状認識 2.新たなテクノロジーや開発手法を活用した研究の推進体制
創薬基盤の技術として、(略)リアルワールドデータ(RWD)の活用、(略)Virtual Clinical Trial、AI創薬など、世界的にも非常に競合の激しい新規の技術や開
発手法が登場している。これらの新たなテクノロジーや開発手法を活用するためには、従来の化学系・生物系の研究者や企業のみではなく情報工学などを含めた学
際的な研究チームや新規モダリティに対応可能な製造体制等の検討が必要となってくる。
Ⅳ.今後の検討について 2.新たなテクノロジーや開発手法を活用した研究の推進体制
RWDについては、CINによるレジストリの構築や利用に向けた基盤整備、MID-NETの安全対策への活用などが進んでいるが、引き続きデータ基盤の構築及びデジ
タルヘルステクノロジーを活用していく手法の開発や課題について検討を進めると共に、市販後調査等を含め企業資金(利用料等)を活用したデータ利活用の体制
を作ることが必要である。
6
<医薬品プロジェクト>
日本で生み出された基礎研究の成果を薬事承認につなげ、革新的な医薬品を創出するため、科学性及び倫理性が十分に担保されうる
質の高い臨床研究・医師主導治験等を支援する。
<支援に係る主なコンセプト>
①患者ニーズの高いもの
臨床研究・医師主導治験
の実施を支援
疾患の希少性、不採算性等を総合的に考慮し、公益性の高いも
のを支援
(臨床研究・医師主導治験の)プロトコール作成
特定臨床研究
医師主導治験(新有効成分、新効能、新用法用量医薬品)
医師主導治験(小児対象)
②疾患登録システム(患者レジス
トリ)等の活用
疾患登録システムを、薬事承認申請に利用可能な比較対照群等
に利活用する、臨床研究・医師主導治験を支援
③ Decentralized Clinical Trial
(DCT)等の新しい手法の活用
デジタルデバイス、オンライン診療等の新しい技術や訪問診療
等を活用し、被験者の安全性やデータの信頼性を担保しつつ、
被験者や関係者の負担を軽減し得る新しい手法を活用した臨床
試験(Decentralized Clinical Trial;分散化臨床試験)を支援
当面優先して議論する課題 令和2年度まとめ(令和3年3月29日医薬品開発協議会)抜粋
Ⅱ.本協議会で指摘された課題や現状認識 2.新たなテクノロジーや開発手法を活用した研究の推進体制
創薬基盤の技術として、(略)リアルワールドデータ(RWD)の活用、(略)Virtual Clinical Trial、AI創薬など、世界的にも非常に競合の激しい新規の技術や開
発手法が登場している。これらの新たなテクノロジーや開発手法を活用するためには、従来の化学系・生物系の研究者や企業のみではなく情報工学などを含めた学
際的な研究チームや新規モダリティに対応可能な製造体制等の検討が必要となってくる。
Ⅳ.今後の検討について 2.新たなテクノロジーや開発手法を活用した研究の推進体制
RWDについては、CINによるレジストリの構築や利用に向けた基盤整備、MID-NETの安全対策への活用などが進んでいるが、引き続きデータ基盤の構築及びデジ
タルヘルステクノロジーを活用していく手法の開発や課題について検討を進めると共に、市販後調査等を含め企業資金(利用料等)を活用したデータ利活用の体制
を作ることが必要である。
6