令和7年度厚生労働省予算案の主要事項 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/wp/yosan/yosan/25syokanyosan/index.html |
| 出典情報 | 令和7年度厚生労働省所管予算案関係(12/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和7年度当初予算案
医薬局医薬安全対策課
(内線2751、2749)
53 百万円(11百万円)※()内は前年度当初予算額
1 事業の目的
• 後発医薬品の普及は医療費の削減において重要であり、引き続き推進していく必要があるが、品質管理問題に端を発し、その安全性に対
して国民の信頼が揺らいでおり、普及を推進する上で大きな障壁となっている。
• 国民の後発医薬品への懸念は、先発医薬品と比べてその安全性が遜色ないかという点が大きい。安全性の確保については、適切な製造管
理のみならず、添付文書改訂時の医療機関への周知活動等リスク最小化に関する取組みの実施等、種々の因子が影響するが、同一成分を
多数の製造販売業者が上市する後発医薬品の特徴からも、製造販売業者による横断的な対応には限界がある。
• リアルワールドデータを用いて、実臨床における後発医薬品の副作用の発生状況等を製造販売業者横断的に監視することで、客観性の高
い安全性情報を入手・解析し、科学的根拠に基づきその安全性について説明することも重要である。
• 後発医薬品は数量ベースで80%を超え、抗がん剤、抗血栓薬、糖尿病治療薬などの使用者が多い領域も含め引き続き多数の新規成分が上
市されていることから、品目数を増やし、調査を加速することで、後発医薬品の信頼性の回復に資する。
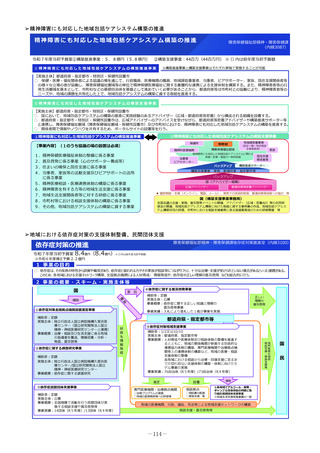
2 事業の概要・スキーム・実施主体等
本事業の範囲
後発医薬品
医療情報データベースを
活用した安全性評価
適正使用の推進に向けて市販後の
• リアルワールドデータを活用して安全性
等に関する科学的なエビデンスを効率的
に収集
更なる安全性情報の集積が課題
新薬と比べて、製薬企業による追加の
安全性情報の収集には限界がある
• 科学的なエビデンスにより、医薬品に対する
漠然とした不安の払しょく
後発医薬品に対する不安
• 医療現場への適正使用に繋がる情報提供
• 後発医薬品への切り替え拒否
• 適正使用に資する情報の不足による
特定の背景を有する患者への処方控え
安全・安心な
薬剤治療環境の実現
医療費の高騰、後発医薬品の開発低下、治療機
会の逸失、不適正使用による副作用被害
等
◎
医薬品の適正使用の推進により、安心して
薬剤治療を受けられる社会の実現
事業の概要:
医療情報データベースMID-NETを活用し、後発
医薬品の安全性に関して、検査値情報等を含む副作用
発現状況等に係る情報を収集・評価し、公表する。
実施主体:独立行政法人医薬品医療機器総合機構
(PMDA)
補助金
補助率:1/2
国
PMDA
事業実績:
令和4年度 1調査
令和5年度 1調査
令和6年度 1調査
ジェネリック医薬品等の承認申請に係るデータの適合性調査の
体制強化事業
令和7年度当初予算案
医薬局
医薬品審査管理課
(内線2737)
12百万円(12百万円)※()内は前年度当初予算額
1 事業の目的
○ 近年の医薬品の品質不良・供給不安については、後発品市場において、共同開発(※)や外部への製造委託などの
導入・活用による多数企業の参入が進み、少量多品目生産構造が生じたことが一因と指摘されている。
(※)製造販売申請に必要な品質試験等のデータについて、ある企業が取得したデータを他の複数企業間で共有し、同じデータを用いて各社が
申請を行うこと。後発品については、平成17年の改正薬事法施行にあわせ、認められるようになった。ただし、委託元の企業自身が、委託
先のデータの信頼性や製造・品質管理の体制について、十分に把握し、責任を負うことが必須。
○
本事業では、品質・供給問題の発生を未然に防止するため、後発品の承認審査に当たり、以下の確認を実施する。
・適合性調査において、開発・製造を他社に委託する製品について、委託元(申請者)が委託先における製品デー
タの信頼性や製造・品質管理の状況を確認するための体制や実際の確認状況について、確認する。
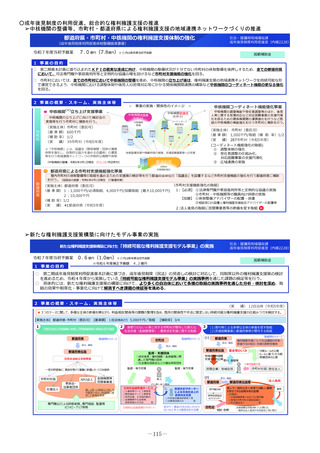
2 事業の概要・スキーム
承認申請
3 実施主体等
後発品企業
実施主体:PMDA
費用内訳:
・人件費(2名):補助率50/100
適合性調査を
強化
委託先における製品データの信頼性や製造・品
質管理の状況を適切に確認しているか
実績
後発医療用医薬品適合性調査件数(新規)(令和5年度):106件
-29-