『規制改革実施計画』(令和5年6月16日閣議決定) (80 ページ)
出典
| 公開元URL | https://www8.cao.go.jp/kisei-kaikaku/kisei/publication/p_index.html#program |
| 出典情報 | 令和5年 規制改革実施計画(6/16)《内閣府》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
c
b の取組その他の取組によって、
変更計画
確認手続制度における変更計画の確認申請
から確認完了に係る審査の標準的事務処理
期間を新たに設定することとし、その際、医
薬品、医療機器等の品質、有効性及び安全性
の確保等に関する法律(昭和 35 年法律第 145
号)における医療機器の各類型に応じた申請
区分ごとの一部変更承認申請に係る標準的
事務処理期間(4か月から6か月)より短い
期間で設定する方向で、具体的な方策を検討
し、結論を得る。
d
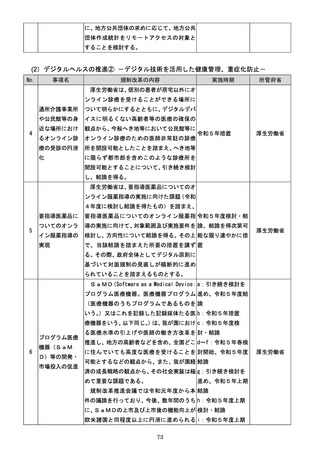
厚生労働省は、SaMDのライフサイク
ルの短期性を踏まえ、事業者が迅速に保険償
還を受けられることで、革新的なSaMDの
開発を可能とする観点から、SaMDについ
ては保険外併用療養費制度の活用も含めた
新たな仕組みを設ける方向で、保険適用の在
り方を検討する。
・第一段階の承認後、事業者の選択に基づき
保険外併用療養費制度の活用等を可能と
することにより、保険診療において使用で
きることとし、臨床現場で活用されながら
第二段階の承認に向けた迅速なデータ収
集を可能にする。
・臨床現場での一定期間の使用実績を踏ま
えて償還価格の柔軟な見直しを行う。
e
厚生労働省は、上市後の使用実績に応じ
て性能が継続的に向上していく可能性があ
るというSaMDの特性を踏まえ、保険点数
を決定した後であっても、事業者の任意の時
点における申込みに基づき、一定期間内の申
請により当該保険点数の再評価を複数回実
施することを可能とする方向で、現行のチャ
レンジ申請制度に関する特例の創設等を含
め、検討する。なお、申請に対する厚生労働
省の審査は、事業者のアップデートの実態に
即した頻度で開催可能とする方向で、厚生労
働省における所要の体制整備を含め、検討す
る。
f
SaMDの保険対象期間が経過した後も
継続的に患者が当該製品を利用する場合や
75