よむ、つかう、まなぶ。
別紙1○【先進医療会議】先進医療Bに係る新規技術の科学的評価等について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00053.html |
| 出典情報 | 先進医療会議(第117回先進医療会議、第142回先進医療技術審査部会 12/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2. 試験治療の実施は、登録の確認後とする旨を明示すること。
3. 「5.研究の方法」の節の「予測しない有害事象」については、定義が明らか
となるように記すこと。
4. 「1 年毎に(略)主要評価項目および副次的評価項目について、解析される。」
については解析結果をどう取り扱うのか、別途定める中間解析との違いを明
確にすること。事前に定めたタイミング・方針に沿わずに試験進捗中の結果
を ad hoc に対外的に公表することは不適切であること、仮に適切な手続きを
とって公表する場合であっても先進医療技術審査部会への報告が必要となる
ことについて、念のために申し添える。
5. 臨床研究保険に関して、各協力医療機関がカバーされる契約となっているの
か否か、および、協力医療機関が追加された場合にどのような対応を取るこ
とになるのかを明示すること。
6. 「7.臨床研究実施期間と目標症例数」の記載について、非劣性マージンに相
当する情報が記載されていないが、非劣性マージンを含めて 0.75 という数値
を設定したということだと推察する。それで正しければその旨追記すること。
【1~16の総評】
総合評価
適
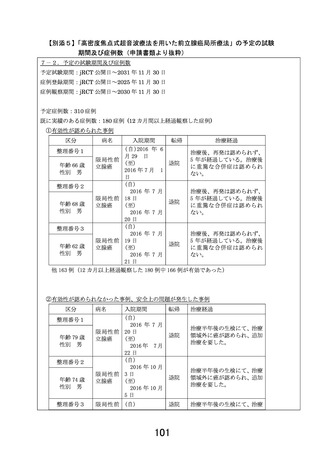
予定症例数 310 例
条件付き適
継続審議
予定試験期間
不適
jRCT 公開日~2029 年 12
月、(登録期間:~2024
年 6 月、観察期間:~2029
年 6 月)
実施条件: 上記、各評価者の「実施条件欄」に記載の各指摘事項について、全て適切に
改訂が加えられること。
コメント欄(不適とした場合は、その理由を必ず記載ください。)
(修正すれば適となる場合は、修正内容を記載ください。)
13
3. 「5.研究の方法」の節の「予測しない有害事象」については、定義が明らか
となるように記すこと。
4. 「1 年毎に(略)主要評価項目および副次的評価項目について、解析される。」
については解析結果をどう取り扱うのか、別途定める中間解析との違いを明
確にすること。事前に定めたタイミング・方針に沿わずに試験進捗中の結果
を ad hoc に対外的に公表することは不適切であること、仮に適切な手続きを
とって公表する場合であっても先進医療技術審査部会への報告が必要となる
ことについて、念のために申し添える。
5. 臨床研究保険に関して、各協力医療機関がカバーされる契約となっているの
か否か、および、協力医療機関が追加された場合にどのような対応を取るこ
とになるのかを明示すること。
6. 「7.臨床研究実施期間と目標症例数」の記載について、非劣性マージンに相
当する情報が記載されていないが、非劣性マージンを含めて 0.75 という数値
を設定したということだと推察する。それで正しければその旨追記すること。
【1~16の総評】
総合評価
適
予定症例数 310 例
条件付き適
継続審議
予定試験期間
不適
jRCT 公開日~2029 年 12
月、(登録期間:~2024
年 6 月、観察期間:~2029
年 6 月)
実施条件: 上記、各評価者の「実施条件欄」に記載の各指摘事項について、全て適切に
改訂が加えられること。
コメント欄(不適とした場合は、その理由を必ず記載ください。)
(修正すれば適となる場合は、修正内容を記載ください。)
13