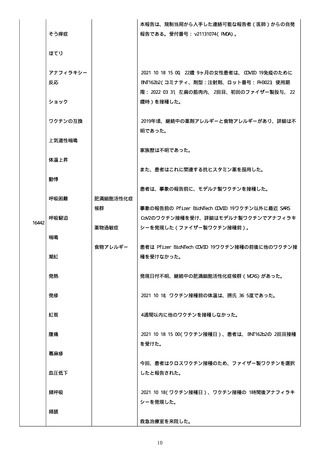
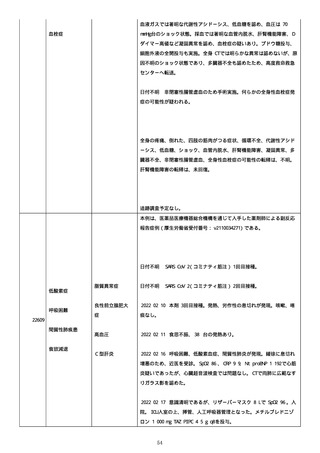
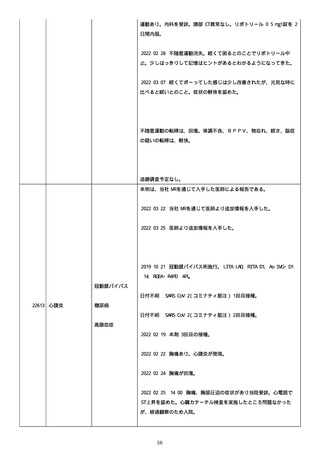
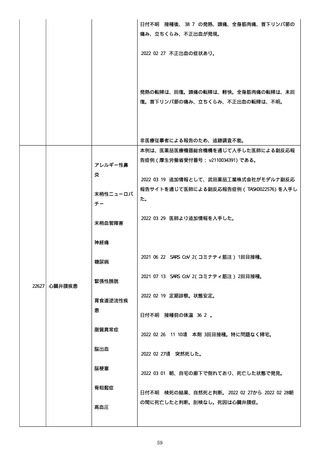
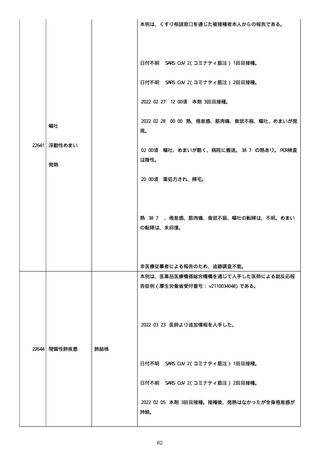
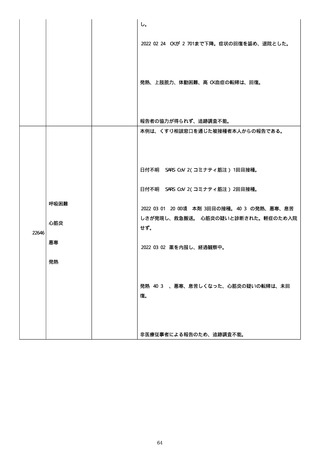
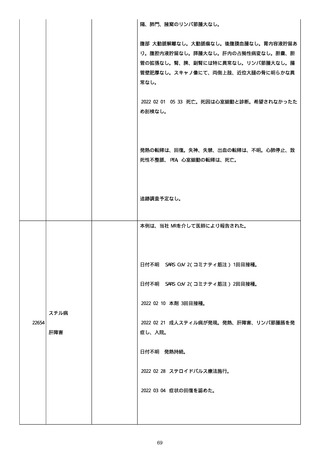
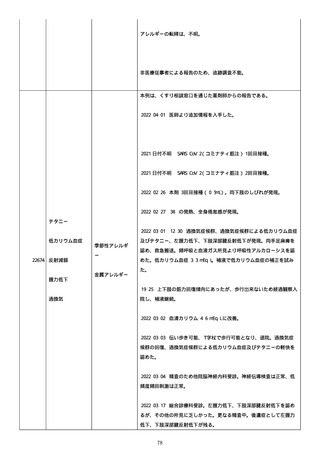
資料1-2-3-6 薬機法に基づく製造販売業者からの副反応疑い報告状況について(交互接種に係る報告症例・基礎疾患等及び症例経過 (255 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00046.html |
| 出典情報 | 第82回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第8回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(8/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
入院中、ステロイドパルスを行い複視は改善傾向であった
が、不十分であったため 2 回目のステロイドパルスを実施。その後、プ
レドニン 60 mg から内服開始し、漸減した。
2022/05/06 症状の増悪なく改善傾向であり、プレドニン 30 mg まで減
量したところで退院。症状の軽快を認めた。外来フォローとした。
眼球運動制限、複視、急性散在性脳脊髄炎、MOG 抗体関連疾患の増悪の
転帰は、軽快。
追跡調査予定あり。
【臨床症状】
・炎症性脱髄が原因と推定される。
・これまでに中枢神経系の脱髄疾患である視神経炎の既往がある。
・臨床的に多巣性の中枢神経系の障害(事象)である。
・中枢神経系に帰することのできる限局性または多発性所見として、
2022/03/29 に脳神経の単一または複数の異常、深部腱反射の変化(反射
減弱または亢進、反射の非対称性)、小脳の機能障害(運動失調症、測
定障害、小脳性眼振など)のいずれかが発現。
【疾患の経過】
・発症から最終観察までの期間は 1 か月
・疾患の単相パターンを示すには観察期間が不十分であり、発症後の観
察期間が 3 か月以内である。
【鑑別診断】
・病気を説明できる、他の明らかな急性感染症や他の疾患が存在する。
255