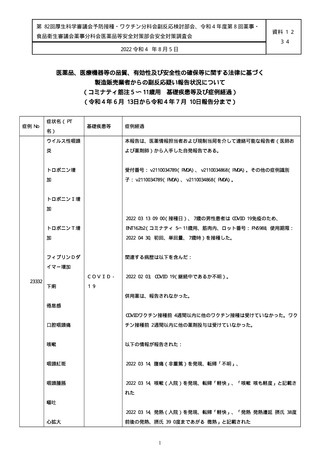
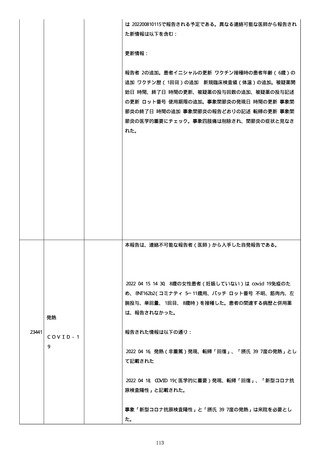
資料1-2-3-4 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注5~ 11歳用・集計対象期間における基礎疾患等及び症例経過) (41 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00046.html |
| 出典情報 | 第82回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第8回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(8/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
吐剤を使用するも症状軽快せず、二次病院へ搬送された。他の症状(呼吸器症
状、神経症状、皮膚症状)はなく、患者の状態はアナフィラキシーとして評価
されなかった。
2022/06/07、追加報告:
原疾患/合併症は不明であった。
特記事項:
患者は病院に救急搬送され、入院せず帰宅した。
報告医師は事象を非重篤とし、事象と bnt162b2 との因果関係は関連ありと評価
した。他要因(他の疾患等)の可能性はなかった。
報告医師は事象と BNT162b2 との因果関係を評価不能とした。
報告医師は、以下の通りコメントした:
接種直後にからの症状発現であり、ワクチン接種によるアレルギー反応と考え
ます。1 回目接種後、無治療で軽快したが、3 日目に吐き気があったとのこと。
追加情報(2022/06/07):
これは、ライセンスパートナーメディセオを経由し連絡可能な同医師から入手
した自発追加報告である。
更新された情報:
主要な報告者の同 CC 報告者は FU#2 の新たな仲介者のため追加、関連する病歴
の「なし」を削除、患者の接種経路に「筋肉内」を追加、事象「嘔吐」は原資
料記載通りに「嘔吐症」から「嘔吐反応」に更新、終了時刻を「2022/05/14」
から「2022/05/13」に更新した。
41